Новые лекарственные средства в лечении заболеваний сопр и пародонта
Опубликовано: 02.05.2024
Воспалительно-деструктивные заболевания пародонта являются одной из наиболее сложных и распространенных форм патологии и основной причиной потери зубов среди взрослого населения. Распространенность патологии среди населения нашей страны остается на довольно высоком уровне: у 13—16-летних подростков заболевание пародонта обнаруживается в 70—86,6% случаев, в возрасте 17—25 лет — в 68%, в возрасте 34—45 лет — в 81%; у рабочих промышленных предприятий — почти в 100% случаев [1]. Современный уровень научных знаний об этио-патогенезе пародонтита определяет микрофлору зубной бляшки и зубного налета (биопленки) в качестве доминирующего этиологического фактора. Получены данные о роли анаэробной и смешанной бактериальной флоры в развитии заболеваний пародонта, позволившие выделить группу так называемых пародонтопатогенных бактерий, которые продуцируют некротизирующие ферменты (коллагеназу, эластазу, фибринолизин, гиалуронидазу и др.), экзотоксины, приводящие к нарушению целостности эпителиальных тканей, что способствует активной деструкции пародонтальных тканей и играет основополагающую роль в генезе пародонтита. Стоит отметить, что пародонтопатогены обладают анаэробным типом дыхания, отличаются высокими адгезивными, инвазивными и токсическими свойствами по отношению к тканям пародонта, способны разрушать иммуноглобулины [2, 3]. В настоящее время из пародонтального кармана изолировано около 500 видов бактерий, но лишь несколько из них признаны пародонтопатогенными: Aggregatibacter actinomycetemcomitans, Porphyromonas gingivalis, Tanerella forshytensis, Campylobacter rectus, Eikenella corrodens, Prevotella intermedia, Fusobacterium nucleatum, Treponema denticola. У лиц со здоровым пародонтом относительная частота встречаемости пяти основных типов пародонтопатогенов в норме не превышает 6% [4, 5]. Хронический пародонтит следует рассматривать как многофакторное заболевание, так как на тяжесть заболеваний пародонта влияют такие местные факторы, как окклюзионная травма, чрезмерное потребление мягкой пищи, уменьшение секреции слюны, нависающие края пломб, наличие ортодонтических аппаратов, аномалии расположения зубов, аномальное прикрепление уздечек губ и языка, мелкое преддверие рта, травматические повреждения. Важную роль в возникновении и развитии заболеваний пародонта играют и общие факторы: нарушение режима питания, курение, гиподинамия, патология внутренних органов и систем, изменения водно-солевого обмена, иммунологические, сосудистые, гормональные и метаболические сдвиги, хроническая интоксикация и гипоксия, ревматические и эндокринные заболевания, нарушения липидного обмена, иммунные нарушения [3, 6—8]. В настоящее время доказано, что лечение воспалительных заболеваний пародонта должно быть комплексным, этиопатогенетическим, индивидуализированным, обоснованным, последовательным. Выбор средств и методов в каждой клинической ситуации зависит от нозологической формы, степени тяжести заболевания и окклюзионных взаимоотношений зубов у конкретного больного [6]. Комплексная терапия должна быть направлена на причину, патогенез заболевания и ликвидацию его отдельных проявлений, что подразумевает применение разных средств, их комбинаций и способов для достижения целей лечения, в связи с чем выделяют этиотропную, патогенетическую и саногенетическую терапию. Большинство из существующих средств наряду с положительными клиническими эффектами обладает и такими отрицательными свойствами, как возможное угнетающее действие на ткани пародонта и его защитные механизмы, участившиеся аллергические реакции организма на лекарственные препараты, полученные химическим путем [4]. Кроме того, клинический опыт свидетельствует о быстрой инактивации большинства препаратов в условиях влажной, биологически активной среды ротовой полости. Основой лечения заболеваний пародонта является проведение качественного инструментального удаления минерализованных и неминерализованных зубных отложений с полированием поверхности корней зубов, что способствует более быстрой нормализации микрофлоры полости рта, минимизирует общее воздействие препарата на организм пациента, позволяет избежать побочных эффектов со стороны органов и систем, создает максимальную местную концентрацию препарата без значимого повышения его уровня в системной циркуляции, ведет к исчезновению клинических признаков воспаления и увеличению сроков ремиссии [9—11]. В пародонтологии средства для местного применения используют в нескольких формах: растворы, полоскания, эликсиры, спреи, мази, пасты, порошки, эмульсии, гели, повязки, клеевые и адгезивные композиции (пленки, нити, чипы), в состав которых включены вещества различных фармакологических групп, и др. Среди них особое место занимают средства локальной доставки с пролонгированным высвобождением лекарственных препаратов, которые обеспечивают длительное эффективное лечение на месте инфекции в гораздо меньших дозах [10]. Выбор методов, средств и последовательность видов лечения определяются особенностями клинического течения и тяжестью процесса. В современной стоматологии большой интерес вызывают методы лечения с выраженным положительным эффектом и минимумом побочных воздействий. К одному из таких методов можно отнести фитотерапию. Лекарственные растительные препараты редко вызывают нежелательные побочные реакции со стороны организма, они менее токсичны и хорошо переносятся больными независимо от возраста, их действие отличается мягкостью, редким возникновением аллергических реакций со стороны организма, что позволяет при необходимости принимать их длительно без вреда для больного, так как к ним не развивается устойчивая адаптация микро- и макроорганизма. Лекарственные средства растительного происхождения обладают разнообразными фармакологическими свойствами: противовоспалительным, антимикробным, ранозаживляющим, обезболивающим, десенсибилизирующим, кровоостанавливающим, кератопластическим, противоотечным, иммуностимулирующим. Они получили широкое применение в стоматологии, так как нетоксичны и обладают выраженным лечебным эффектом, более физиологическим действием [4, 9]. Несмотря на большой опыт применения лекарственных средств растительного происхождения, в стоматологии и сегодня идет постоянный поиск новых соединений, оригинальных по своему строению и фармакологическому эффекту.
В исследовательских работах была отмечена высокая действенность комбинированного препарата стоматофит, являющегося экстрактом из смеси лекарственного сырья: коры дуба, цветков ромашки, травы арники, листьев шалфея, травы тимьяна обыкновенного, травы мяты перечной, корневища аира, — при лечении воспалительных заболеваний паро-донта и слизистой оболочки полости рта (СОПР). Благодаря своему составу стоматофит обладает противовоспалительным, антибактериальным, вяжущим и спазмолитическим действиями [12]. Пародонтоцид представлен серией лекарственных форм: зубная паста, гель, спрей, раствор для полоскания полости рта. В состав названных средств входят эфирные масла шалфея мускатного, мяты перечной, гвоздики, душицы, фенилсалицилат, тимол, аллантоин. Благодаря сочетанию этих веществ у препарата обнаруживаются противовоспалительные, антибактериальные и дезодорирующие эффекты [13]. В исследовании «Клиническое обоснование выбора коллагеновых пластин Farmadont при лечении заболеваний пародонта» одной из задач было проведение сравнительного анализа эффективности лечения заболеваний пародонта с применением коллагеновых пластин и традиционной терапии. Farmadont III — коллагеновые пластины против кровоточивости десны с подорожником, алоэ и зверобоем. После проведенного комплексного лечения с применением данного препарата отмечено улучшение клинического статуса. Достоверно снизились показатели индексов OHI-S, РМА, PI. Уменьшились воспалительные явления в тканях пародонта, о чем свидетельствуют существенные положительные изменения всех клинических индексов [14]. Эфирные масла (лаванда, масло эвкалипта, масло перечной мяты и масло шалфея) обладают бактерицидным, за исключением лаванды, действием, ингибируют адгезию P. gingivalis, а также S. mutans [15]. Целью работы A. Araghizadeh было определить ингибирующую активность in vitro экстракта зеленого чая на некоторых клинически изолированных кариесогенных и пародонтопатогенных бактериях. Двадцать штаммов каждого из S. mutans, Aggregatibacter actinomycetemcomitans, Porphyromonas gingivalis и Prevotella intermedia были выделены из кариозных зубов и пародонтальных карманов пациентов с кариесом зубов и заболеваниями пародонта. В результате все клинические патогены S. mutans (100%) были чувствительны к экстракту зеленого чая в концентрациях 6,25, 12,5, 25 и 50 мг/мл, пародонтопатогены A. actinomycetemcomitans, P. intermedia, P. gingivalis (100%) были чувствительны к 12,5, 25 и 50 мг/мл этой выдержки. Таким образом, результаты показали, что экстракт зеленого чая проявляет сильную антибактериальную активность у S. mutans, A. actinomycetemcomitans, P. gingivalis и P. intermedia, поэтому может использоваться в средствах для полоскания рта или чистки зубов в целях профилактики кариеса и заболеваний пародонта [16]. В 2012 г. проведено исследование для оценки краткосрочных клинических и микробиологических эффектов коммерчески доступного геля и порошка, содержащего Acacia arabica, и сравнения их влияний с гелем, содержащим 1% хлоргексидина. Предпосылкой явилась потребность в антибляшечном агенте, который можно использовать ежедневно, без побочных эффектов антибактериальных химических веществ, таких как хлоргексидин. Результаты показали, что гель Acacia arabica и порошок клинически значительно улучшают показатели индекса GI и зубного налета, это улучшение было сопоставимо с эффектом от применения геля с 1% хлоргексидином. Из этого следует, что и гель Acacia arabica, и порошок могут быть полезными фитосоставами для контроля десневого налета у пациентов с гингивитом [17]. Проведено сравнительное исследование эффективности полосканий полости рта раствором трифалы с 0,2% раствором хлоргексидина у пациентов с заболеваниями пародонта (2014). Оба агента, используемые в исследовании, явились эффективными противовоспалительными и антимикробными препаратами. В данном клиническом исследовании при сравнении группы трифалы с группой хлоргексидина статистически значимого различия не было (р>0,05). Это означало, что эффективность трифала в полости рта была схожа с таковой 0,2% CHX. Таким образом, на основе этих данных раствор трифала можно считать альтернативой хлоргексидину [18]. Алоэ вера — лекарственное растение с противовоспалительным, противомикробным, антидиабетическим и иммуномодулирующим свойствами. Обнаружено, что штаммы S. mutans наиболее чувствительные к гелю Алоэ вера в концентрации 12,5 мкг/мл, тогда как A. actinomycetemcomitans, P. gingivalis и B. fragilis были менее чувствительными, причем концентрация составляла 25—50 мкг/мл (р
Как известно, в полости рта пища подвергается механической обработке (измельчается, растирается). Чем тщательней пища измельчена, тем лучше она подготовлена для дальнейшей обработки. Зубы являются основной частью жевательного аппарата.
Новейшие достижения, используемые в медицинской технике, позволяют эффективно и безболезненно лечить и, в случае необходимости, удалять зубы. Кроме специальных стоматологических материалов применяются лекарственные средства разных фармакологических групп (смотри соответствующие разделы): местноанестезирующие, анальгезирующие, противовоспалительные, витамины и другие, а при микробных поражениях полости рта – антибиотики и прочие антибактериальные препараты. Большое значение имеет не только своевременное лечение заболеваний полости рта, но и лекарственная профилактика, а также гигиеническая обработка ротовой полости.
В арсенале стоматологических средств есть препараты, предназначенные для самых маленьких пациентов – это, например, средства, облегчающие болезненный процесс прорезывания зубов ( Дентинокс ). Созданы средства и для пожилых пациентов, в том числе способствующие приспособлению к ношению зубных протезов. Некоторые из них улучшают состояние поврежденных протезом участков слизистой оболочки полости рта, другие – фиксацию протеза на челюсти.
Патологические состояния, с которыми наиболее часто имеет дело врач-стоматолог в своей практике – это, прежде всего, кариес, заболевания пародонта и слизистой оболочки полости рта.
Пародонтопатия – это собирательное название разнообразных заболеваний пародонта воспалительного, дистрофического и опухолевого характера, возникающих в результате действия внешних и внутренних факторов. Частота возникновения пародонтопатии у взрослого населения достигает почти 80%. Процесс может быть как поверхностным, так и глубоким, и очень редко встречаются дистрофические формы, которые со временем осложняются воспалением и получили название смешанной пародонтопатии.
Причины возникновения пародонтопатий до сих пор полностью не выяснены. Считается, что большую роль в их возникновении играет инфекционно-воспалительное заболевание пародонта – пародонтит. Источником инфекции при пародонтите может быть зуб, придаточные пазухи носа, дыхательные пути и др. Большое значение придается и патологическим процессам в полости рта: нарушение нормального прикуса, наличие твердых зубных отложений (так называемый зубной камень) и другие. Кроме этого, пародонтопатия часто возникает на фоне несбалансированного питания (дефицит микроэлементов, белков и другое).
Среди заболеваний слизистой оболочки полости рта наиболее часто встречается стоматит. Он может быть инфекционным (вирусная, бактериальная, грибковая инфекция), аллергическим, в том числе афтозный стоматит (афты – небольшие изъязвления слизистой оболочки полости рта), травматическим. В последнем случае в качестве травмирующего фактора могут выступать острые края зубов или зубные протезы.
Лечение заболеваний полости рта – процесс длительный, требующий применения комплексной терапии (как местной, так и общей). В настоящее время одним из средств, применяемых при местном консервативном лечении воспалительных заболеваний пародонта и слизистой оболочки полости рта является препарат Холисал .
Показано, что при некоторых поражениях пародонта Холисал способствует полному излечению или значительно улучшает состояние пациентов. Препарат уменьшает выраженность воспалительных явлений, устраняет неприятные субъективные ощущения. Кроме того, Холисал понижает содержание в слюне белка и активность ферментов (кислой и щелочной фосфатазы, лейцинаминопептидазы).
Противовоспалительная и обезболивающая активность, а также антибактериальное и противогрибковое действие обусловливают возможность применения Холисала не только при пародонтопатиях, но и при других заболеваниях полости рта.
Основные средства, применяемые в стоматологии, перечислены ниже. С подробной информацией по этим препаратам можно ознакомиться на сайте www.rlsnet.ru.
Дентинокс (лидокаин+полидоканол+ромашки экстракт) местноанестезирующее, противовоспалительное местное, антисептическое гель; р-р Dentinox (Германия)
Калгель (лидокаин+цетилпиридиния хлорид) антисептическое, местноанестезирующее гель зубн. GlaxoSmithKline (Великобритания)
Лакалют Актив (стоматологическое средство) антисептическое, противовоспалительное, гемостатическое, противокариозное, повышающее резистентность зубной эмали к воздействию кислот паста зубн. Arcam (Германия)
Лакалют Актив форте (стоматологическое средство) противовоспалительное, гемостатическое, антисептическое, противокариозное, повышающее резистентность зубной эмали к воздействию кислот пор.зубн. Arcam (Германия)
Лакалют Антиплак (стоматологическое средство) антисептическое, освежающее, удаляющее зубной налет, противокариозное р-р стомат. Arcam (Германия)
Лакалют детская зубная паста “Kapt’n Blaubar” (стоматологическое средство) антисептическое, повышающее резистентность зубной эмали к воздействию кислот, противокариозное паста зубн. Arcam (Германия)
Лакалют Сенситив (стоматологическое средство) антисептическое, противокариозное, повышающее резистентность зубной эмали к воздействию кислот паста зубн. Arcam (Германия)
Лакалют спрей для полости рта (стоматологическое средство) антисептическое, освежающее, противокариозное, удаляющее зубной налет спрей Arcam (Германия)
Лакалют Уайт (стоматологическое средство) противокариозное, повышающее резистентность зубной эмали к воздействию кислот, отбеливающее, удаляющее зубной налет паста зубн. Arcam (Германия)
Лакалют Флуор (стоматологическое средство) противокариозное, повышающее резистентность зубной эмали к воздействию кислот, удаляющее зубной налет, отбеливающее паста зубн. Arcam (Германия)
Лакалют Фреш (стоматологическое средство) антисептическое, удаляющее зубной налет, противокариозное, освежающее р-р стомат. Arcam (Германия)
Метрогил Дента (метронидазол+хлоргексидин) антибактериальное, противопротозойное (трихомонацидное), антисептическое гель д/десен Unique (Индия)
Себидин (аскорбиновая кислота+хлоргексидин) антибактериальное (бактерицидное), антисептическое табл.д/рассас. GlaxoSmithKline (Великобритания)
Тантум Верде (бензидамин) противовоспалительное, анальгезирующее, местноанестезирующее р-р наружн.; спрей доз. CSC (Италия), произв.: Angelini Francesco (Италия)
На современном этапе развития стоматологии при лечении воспалительных заболеваний пародонта предусмотрен комплексных подход, цель которого - ликвидация воспалительных процессов в пародонте, восстановление структурных и функциональных свойств элементов пародонтального комплекса, повышение местных и общих факторов защиты, что достигается сочетанием этиотропной, патогенетической и симптоматической терапии [3,7,10,1,16,24,25,31].
Общее лечение предусматривает использование нестероидных препаратов: салицилатов, препараты пиразолона, производных ряда органических кислот: индолуксусной (индометацин, сулиндак), фенилуксусной (вольтарен), пропионовой (мефенаминовая кислота, понстан, опири, клотам), которые оказывают сочетанное противовоспалительное, болеутоляющее и жаропонижающее действие [2].
В общем лечении воспалительных заболеваний пародонта для подавления стойких субгингивальных патогенов применяют антибиотики [27,29,30,33]. Эти препараты применяют по строгим показаниям: гноетечение из пародонтальных карманов, абсцедирование, свищи, прогрессирующая деструкция костной ткани альвеолярного отростка, интоксикация, состояние до и после хирургического вмешательства. Доказано, что назначение антибактериальных препаратов изменяет микрофлору над- и поддесневой зубной бляшки, меняет клиническую картину пародонтита в сторону стабилизации процесса, замедляет воспалительную резорбцию костной ткани, однако приводит к формированию устойчивых к ним форм микрофлоры полости рта [13].
Антибиотики и другие противовоспалительные средства оказывают бактерицидное и бактериостатическое действие на микробное население пародонтальных карманов и полости рта. При этом происходит массовое недифференцированное и бесконтрольное уничтожение микрофлоры всего биотопа полости рта и, в первую очередь, сапрофитной микрофлоры. Кроме того, антибиотикотерапия приводит к селекции множественно устойчивых вариантов возбудителей, способствующих генерализации воспалительного процесса. Длительное назначение этих препаратов может привести к развитию дисбактериоза из-за подавления нормальной микрофлоры пациента. В связи с этим наиболее часто при пародонтите для подавления патогенных микроорганизмов субгингивальной бляшки применяют антибактериальные препараты местного действия - антисептики [8].
Широко известна высокая эффективность местного применения в качестве антисептика раствора хлоргексидина [34]. Хлоргексидин, будучи катионом, вступает во взаимодействие с бактериями, притягивая отрицательно заряженные мембранные компоненты. К отрицательным свойствам хлоргексидина относят раздражающее и аллергезирующее действие, окрашивание зубов, пломб и языка, неприятный вкус, расстройство вкусовой чувствительности, десквамацию эпителия полости рта [13].
В комплексной терапии больных хроническим пародонтитом существенное значение отводится хирургическим методам. Главная цель пародонтальной хирургии заключается в создании оптимальных функциональных условий для тканей пародонта: ликвидация пародонтальных карманов на фоне оптимизации условий для регенерации тканей пародонта [4,6].
Для оптимизации условий остеорепарации в настоящее время используются различные остеопластические материалы: на основе биологически активного стекла, гидроксиапатита, сульфата кальция, трикальций фосфата, костного коллагена и сульфатированных гликозаминогликанов [19,32,35]. Каждый из перечисленных препаратов достаточно эффективен, но вероятность его отторжения все же высока [36].
К основным хирургическим вмешательствам при заболеваниях пародонта относят кюретаж, гингивотомия, гингивэктомия, лоскутные операции и пластика десен. Вспомогательные хирургические вмешательства предполагают проведение по показаниям пластики уздечек губ, языка, вестибулопластики, рассечение мощных соединительнотканных тяжей [6,11].
В настоящее время общепринятыми методами местного лечения заболеваний пародонта являются профессиональная гигиена полости рта, лечение кариеса и его осложнений, удаление зубов, не подлежащих лечению, восстановление контактных пунктов, полировка пломб, удаление нерациональных ортопедических конструкций, индивидуальное пришлифовывание, хирургические методы лечения.
На сегодняшний день не вызывает сомнений взаимосвязь между распространенностью воспалительных заболеваний пародонта, тяжестью их течения и уровнем гигиены полости рта [26,23,28]. Из большого количества профилактических методов наиболее перспективными являются ультразвуковая обработка и чистка зубов методом пескоструйной обработки. М.В. Рыжкова (2008) разработала критерии оценки снижения активности воспалительного процесса на уровне зубодесневого соединения с использованием результатов исследования цитологического состава и уровня цитокинов (ИЛ-8 и ИЛ-1В) десневой жидкости, позволяющих судить о качестве и эффективности проводимых гигиенических мероприятий. Проведение повторных курсов профессиональной гигиены полости рта автор рекомендует проводить пациентам с катаральным гингивитом не позднее чем через 6 месяцев после проведения профилактических мероприятий, а пациентам без признаков патологии пародонта и с пародонтитом легкой степени тяжести - не позднее чем через год [22].
Мардахаева В.Н. (2009) на основании показателей микроциркуляции установила характер и степень гемодинамических изменений при гигиенической чистке зубов, что позволило автору определить продолжительность проведения процедуры в зависимости от состояния пародонта и вида зубной щетки с целью повышения эффективности профилактики и лечения начальных воспалительных заболеваний пародонта.
В литературе отмечена эффективность электроактивированных водных растворов. Исследователями разработана методика использования анолита и католита, заключающаяся в ирригации полости рта раствором анолита и затем католита (по 5 минут) с помощью ирригатора AQUAJETLD-A7 на протяжении семи визитов и прием католита внутрь два раза в день, что позволило получить быстрый противовоспалительный эффект, контролируемый клиническими и лабораторными методами исследования [14,15].
Сравнительный анализ эффективности стандартной терапии, комбинированного применения стандартной терапии и электроактивированных водных растворов и самостоятельного применения электроактивированных водных растворов, по разработанной авторами методике при хроническом генерализованном пародонтите легкой и средней степени выявил не только высокую эффективность электроактивированных водных растворов, как в отношении микробной флоры полости рта, так и процессов восстановления поврежденных тканей пародонта, но и преимущества перед традиционной терапией [12,1].
Исследованиями в области молекулярной биологии отечественными и зарубежными авторами установлена ведущая роль основных компонентов межклеточного матрикса - гликозаминогликанов в процессах метаболизма построения тканей пародонта. Многочисленные исследования установили их ведущую роль в репарации пародонтальных тканей. Сравнительная оценка результатов лечения с использованием традиционных методов и комплексного лечения с применением гелевого сорбента - сульфатированного гликозамингликана - «Гелевин», проведенная с учетом общей продолжительности лечения, стабилизации воспалительного процесса в пародонте, частоты и характера рецидивов, длительности ремиссий, изменений показателей цитограммы и перекисного окисления липидов, свидетельствует о положительном воздействии и высокой эффективности сорбента «Гелевин» в комплексной терапии больных хроническим генерализованным пародонтитом легкой и средней степени тяжести в фазе обострения [20].
Используемый в комплексном лечении пародонтита и предоперационной подготовке гель «Гликодент», участвуя в построении эпителия, образует границу между поврежденными и подлежащими слоями, препятствует обезвоживанию тканей раны, потере электролитов и белков, предупреждает инвазию микроорганизмов. К возможному механизму действия как эндогенных, так и экзогенных сульфатированных гликозамингликанов, следует отнести то, что, связывая воду, они понижают отек ткани, способствуя локализации воспаления, препятствуя распространению процесса на окружающие ткани. Гель «Гликодент» обеспечивает формирование зубодесневого прикрепления за счет гликозамино-содержащих комплексов, участвующих в формировании гемидесмосом [5].
Одним из препаратов, которые нормализуют тканевой газообмен и метаболизм тканей пародонта, признан гепарин. Под влиянием гепарина происходит нормализация кислородного баланса тканей, улучшается микроциркуляция и транспорт веществ между тканью и кровью. Гепарин устраняет спазмы, ликвидирует микротромбы, повышает проницаемость сосудов, тканей и толерантность тканей к гипоксии, обладает антиаллергическим действием. Оказывая антикоагулирующее и противогипоксическое действие, Гепарин способствует реабилитации повреждённой ткани. Кроме того, Гепарин нормализует ток лимфы в очаге поражения. Нижник В.Г. (2000) доказала, что включение препарата Гепарин в комплексное лечение больных с воспалительными заболеваниями пародонта повышает терапевтический эффект: приводит к сокращению сроков лечения, увеличивает длительность ремиссии, способствует более быстрой ликвидации, наибольшая эффективность достигается при введении Гепарина в ткани пародонта с подогревом до 40 0 С, при помощи приспособления для введения медикаментов в ткани пародонта [18].
Зубаирова Г.Ш. (2009) разработала метод диагностики и комплексного лечения хронического генерализованного пародонтита с использованием нового лекарственного средства, содержащего комбинацию иммуномодулятора (лейкоцитарный интерферон) и пробиотика (бактисубтил). Для улучшения результатов лечения больных хроническим генерализованным пародонтитом автор рекомендует применение лечебного геля с антибактериальными и иммуномодулирующими свойствами, содержащего в качестве основы натрий - карбоксиметилцеллюлозы в сочетании с лейкоцитарным интерфероном и бактисубтилом по схеме: при легкой степени - 5, при средней - 7, при тяжелой - 9 раз, в составе пародонтальной повязки. Для профилактики рецидивов хронического генерализованного пародонтита необходимо повторное лечение по представленной схеме через 6-12 месяцев [9].
Т.В. Ракова (2009) в своей работе показала, что включение в схему традиционного лечения хронического катарального гингивита антисептического препарата «Йодо-гликоль паста нео», активным компонентом которой является 5% йод, и иммуномодулятора « Деринат » обеспечивает ликвидацию воспалительного процесса в пародонте в 3,6 раза быстрее, чем при традиционной терапии, а также позволяет продлить период ремиссии заболевания на 6 месяцев и снизить в среднем количество обострений в 2,3 раза [21].
Непомнящей Н.В. (2008) выявлены группоспецифические клинические особенности хронического генерализованного пародонтита. Автор показал, что у больных с В(III) группой крови чаще встречается тяжелая форма заболевания. У пациентов с А(II) группой крови отмечены наихудшие показатели гигиены полости рта, о чем свидетельствует максимальные индекс зубного камня, индекс Мюлеманна, гигиенический индекс и степень подвижности зубов, у них менее результативна традиционная терапия. Также автором отмечено, что терапия хронического генерализованного пародонтита с включением препарата метаболического действия силистронга по 1 чайной ложке 2 раза в день внутрь, благодаря многогранному действию препарата из плодов расторопши, включающему противовоспалительный и мембранопротекторный эффекты, показана пациентам с сопутствующей соматической патологией и при склонности к рецидивирующему течению заболеваний пародонта [17].
В комплексном лечении заболеваний пародонта большое значение придается физиотерапевтическим методам лечения. Общеизвестны устройства для введения лекарственных веществ постоянным электрическим током, широко применяется переменное магнитное поле, лазеротерапия гелийнеоновым лазером, вакуум-электрофорез, комбинированная КВЧ-лазерная терапия и др. [3].
Таким образом, анализ литературы свидетельствует о неудовлетворенности стоматологов существующими методами лечения пародонтита, обширном поиске новых, более эффективных способов лечения данной патологии, позволяющих получить наиболее эффективное, патогенетически обоснованное лечебное воздействие на ткани пародонта.
Рецензенты:
Скуридин П.И., д.м.н., главный врач ГАУЗ ПО «Городская стоматологическая поликлиника», г. Пенза;
Захаркин А.Г., д.м.н., профессор, заместитель директора по лечебной части ООО «ДентиЗ» Республика Мордовия, г. Саранск.

Рубрика: Медицина
Дата публикации: 10.06.2019 2019-06-10
Статья просмотрена: 567 раз
Библиографическое описание:
Рассказова, В. В. Современные методы комплексного лечения воспалительных заболеваний пародонта: обзор литературы / В. В. Рассказова, П. Н. Войтова. — Текст : непосредственный // Молодой ученый. — 2019. — № 24 (262). — С. 37-39. — URL: https://moluch.ru/archive/262/60494/ (дата обращения: 04.04.2021).
Высокая частота и интенсивность поражения воспалительными заболеваниями пародонта являются современной проблемой стоматологии. Поэтому очень важно определить комплекс мер для предупреждения и лечения таких заболеваний. В данной обзорной статье рассматриваются современные методы комплексного лечения заболеваний пародонта. Приведён обзор отечественной и зарубежной литературы о современных подходах к лечению данной группы заболеваний. Описаны некоторые современные методы и средства комплексного лечения. К ним относятся: терапевтические, ортопедические, хирургические. Знание этих методов необходимо и имеет большое значение для использования в практике врача стоматолога.
Ключевые слова: воспаление, пародонтит, комплексные методы лечения.
Современная стоматология предусматривает комплексный подход к лечению воспалительных заболеваний пародонта. Цель такого подхода — ликвидировать воспалительные процессы в пародонте и восстановить структурные и функциональные элементы пародонтального комплекса. [2 с.104], [8 с.2].
Местным воздействием на воспалительные процессы в пародонте достигается полная ликвидация зубных отложений, как минерализованных так и неминерализованных. После снятия зубных отложений следует медикаментозное лечение, которое способствует более быстрому исчезновению клинических признаков воспаления и увеличению сроков ремиссии. [3, с. 15].
В качестве этиотропной терапии пародонтитов используется современная методика инструментального устранения зубной бляшки и зубного камня, выравнивание поверхности корня зуба — методика Scaling&RootPlaning (SRP). Для выполнения этой техники необходимы кюреты, скейлеры, а так же воздушно-абразивные системы. Scaling и RootPlaning проводятся последовательно в одно посещение. После проведения этой методики поверхность коронки и корня должна быть твердой, чистой и без микрошероховатостей. SRP является одной из наиболее часто используемых процедур, приводящих к уменьшению количества бактерий, и многими врачами рассматривается как золотой стандарт лечения [15 с.132].
Другой вариант механической антимикробной терапии был предложен Quirynen. Это однофазная дезинфекция всей полости рта, подразумевающая полное санирование полости рта, с помощью чистки языка в течение одной минуты раствором хлоргексидина 1 %, а также снятие зубных отложений, орошение пародонтальных карманов 1 % раствором хлоргексидина, полоскание полости рта 0,2 % раствором хлоргексидина в течении 2 ух минут. Но так как хлоргексидин у сенсибилизированных пациентов может вызвать индивидуальную реакцию, необходимо тщательное соблюдение правил безопасности. [16 с.132].
Для нормализации нормальной микрофлоры полости рта используются лекарственные препараты различного спектра, одними из них являются антибактериальные препараты, которые делятся на две основные группы: антисептики и антибиотики. [12, с. 75].
Антибиотики и другие противовоспалительные средства оказывают губительное действие на микроорганизмы в пародонтальных карманах полости рта. При этом происходит массовое недифференцированное и бесконтрольное уничтожение микрофлоры всего биотопа полости рта и, в первую очередь, сапрофитной микрофлоры. Кроме того, антибиотикотерапия приводит к селекции множественно устойчивых вариантов возбудителей, способствующих генерализации воспалительного процесса. Длительное назначение этих препаратов может привести к развитию дисбактериоза из-за подавления нормальной микрофлоры пациента. В связи с этим наиболее часто при пародонтите для подавления патогенных микроорганизмов субгингивальной бляшки применяют антибактериальные препараты местного действия — антисептики [11 с.25].
При местном применении известна высокая эффективность антисептика хлоргексидина [17 с.351]. Он вступает во взаимодействие с бактериями, притягивая отрицательно заряженные частицы. К отрицательным свойствам хлоргексидина относят раздражающее и аллергезирующее действие, окрашивание зубов, пломб и языка, неприятный вкус, расстройство вкусовой чувствительности, десквамацию эпителия полости рта [9 с.144].
Для аппликации на десну можно использовать гель «Метрогил-Дента». Проведены исследования применения геля и отработаны оптимальные и концентрационные характеристики его применения. [4 с.24].
Гель «Холисал» имеет многочисленные результаты эффективного клинического применения в лечении воспалительных заболеваний пародонта. Это комбинированный препарат, активными действующими веществами которого являются холина салицилат и цеталкония хлорид. Оба компонента находятся в гелевойэтанолсодержащей адгезивной основе, которая помогает удерживать активные компоненты на поверхности слизистой оболочки [10 с.44].
Зубаирова Г. Ш. (2009) разработала метод диагностики и комплексного лечения пародонтита с использованием нового лекарственного средства, содержащего комбинацию иммуномодулятора (лейкоцитарный интерферон) и пробиотика (бактисубтил). Автор рекомендует применение лечебного геля, содержащего в качестве основы натрий — карбоксиметилцеллюлозы в сочетании с лейкоцитарным интерфероном и бактисубтилом по схеме: при легкой степени — 5, при средней — 7, при тяжелой — 9 раз, в составе пародонтальной повязки. Для профилактики рецидивов хронического генерализованного пародонтита необходимо повторное лечение по представленной схеме через 6–12 месяцев [6 с.34].
Для шинирования подвижных зубов 1–2 степени фронтальной группы некоторые авторы изготовили шину из диоксида циркония с последующей фиксацией на композитный цемент. По мнению авторов, это долговечный способ фиксации [5 с.34].
Так же можно использовать адгезивно — волоконные шины (GlassSpan) для временного шинирования при генерализованном пародонтите, как делал Е.Н Жулев и соавторы. Для постоянного шинирования они применяли шины из металлокерамических искусственных коронок, цельнолитых коронок, шины-протезы с замковыми креплениями, с внекоронковыми неактивируемыми рельсовыми аттачменами Bredent, с полулабильными сферическими аттачменами Rhein-83 и с балочными аттачменами. [1 с.16–18], [14 с].
С недавнего времени в лечении воспалительных заболеваний пародонта с успехом применяется аппаратный комплекс «Vector» фирмы DurrDental (Германия). Он эффективно удаляет биоплёнку, зубную бляшку, зубной камень. При работе аппаратом суспензия гидроксиаппатита разделяется на частицы, которые имеют положительное воздействие на создание оптимального биологического состояния и регенерации структур пародонта. Так же у пациента формируется положительная мотивация на проведение дальнейшего лечения из-за безболезненности данной процедуры. [13 с.46], [14 с.139].
Таким образом, наличие и знание современных технологий, методов и средств лечения воспалительных заболеваний пародонта имеет важное значение для практического использования в практике врача стоматолога, что еще раз подтверждает комплексный подход к данной патологии.
- Адамчик А. А. Оценка эффективности шинирования шиной из диоксида циркония и материала «Glasspan» при заболеваниях парадонта//Кубанский научный медицинский вестник. 2011. № 1(136). С.16–18.
- Грудянов А. И. Диагностика в пародонтологии / А. И. Грудянов, A. C. Григорьян, О. А. Фролова. — М.: Медицинское информационное агентство, 2004. — 104с.
- Грудянов А. И., Масленикова Г. В., Загнат В. Ф. Сравнительное изу¬чение эффективности воздействия ряда местных антимикробных препаратов на видовой и количественный состав микробной флоры пародонтальных карманов // Стоматология. — 1992. — Т.71. — № 1. — С. 25–26.
- Грудянов А. И., Дмитриева Н. А., Овчинникова В. В. Оценка эффективности локального применения препарата «МетрогилДента» при воспалительных поражениях пародонта // Пародонтология. 2002.№ 3. С. 24–25.
- Жулев Е. Н., Щепетнова Е. Е. Ортопедическое лечение хронического генерализованного пародонтита как этап комплексного этиопатогенетического лечения// Обозрение. Стоматология.2012. № 1(75). С. 34–36.
- Зубаирова Г. Ш. Изменение содержания секреторных иммуноглобулинов в полости рта больных хроническим генерализованным пародонтитом при лечении с локальным использованием пробиотика и иммуномодулятора /Г. Ш. Зубаирова, А. И. Булгакова, Ю. А. Медведев, И. В. Валеев, А. К. Юнусова // Вестник Российской военно-медицинской академии. — Санкт-Петербург, 2009. — № 1 (21). — С. 73–75.
- Караков К. Г., Власова Т. Н., Авшарян Д. С., Оганян А. В. Эффективность применения склерозирующей терапии при гипертрофическом гингивите на фоне пародон-тита//Стоматолог — практик. 2013. № 1. С.44–45.
- .Митин Н. Е., Дармограй В. Н., Курякина Н. В., Дармограй С. В. Новые подходы к лечению заболеваний пародонта растительными средствами // Информационный листок рязанского центра научно-технической информации. — Рязань, 1999. — С.1–3.
- Маланьин И. В. Современные методы лечения и профилактики заболеваний пародонта. Учебно-методическое пособие // Кубанская научная школа стоматологии. — 2012. — 144 с.
- Меркулов С. Я., Цацурина А. С. Опыт использования геля «Холисал» при лечении заболеваний пародонта//Маэстро стоматологии. 2012. № 4(48).
- Олейник О. И. Разработка методов и оценка эффективности результатов индивидуальной профилактики и воспалительных заболеваний пародонта: автореф. дис. докт. мед.наук. — Воронеж, 2014. — 46 с.
- Олейник О. И., Вусатая Е. В., Попова В. С. Комплексный подход к лечению ранних форм воспалительных заболеваний пародонта // Молодой ученый. — 2015. — № 5(85). — С. 75–78.
- Хотит Р. А. Применение аппарата VECTOR в комплексной терапии заболеваний пародонта / Р. А. Хотит // Дентал Юг. — 2006. — № 3. — С. 46–47.
- Оценка эффективности применения вектор-системы в комплексном лечении пациентов с хроническим генерализованным пародонтитом средней степени / О. И. Олейник, М. А. Сорокина, С. В. Ерина, К. П. Кубышкина // Вестник новых медицинскихтехнологий. — 2013. — Т. XХ, № 2. — С. 138–143.
- Apatzidou D. A., Kinane D. F. Quadrant root planing versus same-day full-mouth root planing. I. Clinical findings // Journal of Clinical Periodontology. 2004. Vol. 31(2). P. 132–140.
- Apatzidou D. A., Kinane D. F. Quadrant root planing versus same-day full-mouth root planing. I. Clinicalfindings // JournalofClinicalPeriodontology. 2004. Vol. 31(2). P. 132–140.
- Unsal E., Akkava M., Walsh T. F. Influence of a single applications of subgingival chlorhexidine gel or tetracycline paste on the clinical parameters of adult periodontitis patients //J. Clin. Periodontol. — May 1998. — P.351–5.
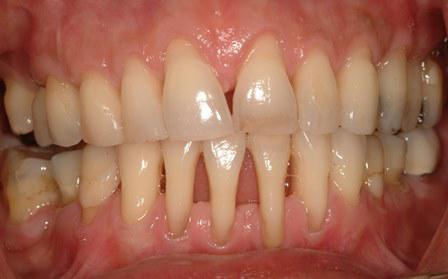
Болезни пародонта – это обобщающий термин, используемый для описания инфекционного воспалительного процесса, который может поражать один структурный элемент или комплекс составных элементов пародонта. Структуры, поддерживающие зуб, представлены альвеолярной костью, периодонтальной связкой и цементом корня. Заболевания пародонта в основном спровоцированы действием зубного налета или микробной биопленкой, представляющей собой гетерогенную структуру из патогенных микроорганизмов. Более 500 видов микроорганизмов считаются потенциальными этиологическими агентами, провоцирующими поражение тканей пародонта. Кроме них, вирусы и грибки тоже играют не последнюю роль в патогенетическом процессе. При возникновении и прогрессировании заболевания патогенные микроорганизмы колонизируют область десен, окружающую зуб, а вследствие их воздействия на ткани начинает формироваться пародонтальный карман. В глубоких пародонтальных карманах можно найти до 109 разновидностей бактерий, но несмотря на потенциал многих патогенов, которые ассоциируются с заболеваниями пародонта, лишь небольшое их количество связано с активной фазой заболевания.
Socransky и коллеги разделили патогенные микроорганизмы, участвующие в прогрессировании заболевания на две основные группы: "красный" и "оранжевый" комплексы. Красный комплекс включает в себя следующие грамотрицательные анаэробные бактерии: Porphyromonas gingivalis, Treponema denticola и Tanneralla forsythia, в то время как оранжевый комплекс состоит из Prevotella nigrescens, Peptostreptococcus micros, Campylobacter rectus, Centruroides gracilis, Campylobacter showae, Eubacterium nodatum и Streptococcus constellatus. Кроме них, с болезнями пародонта тесно ассоциируются Aggregatibacter actinomycetemcomitans и Eikenella corrodens. В результате многочисленных исследований было установлено, что для достижения успешного результата лечения, один из аспектов терапии должен быть направлен именно на нейтрализацию данных бактерий, жизнедеятельность которых напрямую связана с протеканием заболевания.
Антибиотики
Системная антибиотикотерапия должна рассматриваться как один из приемлемых вариантов лечения пациентов с пародонтитом. Данный подход актуален для пациентов, резистентных к обычной терапии заболевания, или у которых наблюдаются следующие проблемы со здоровьем: наличие абсцесса, компромиссное или ослабленное состояние иммунитета, неконтролируемый сахарный диабет, присутствие признаков и симптомов системных поражений, лихорадки и лимфаденопатии. Выбор наиболее подходящего системного антибиотика должен основываться на результатах культивирования микроорганизмов и тестирования их чувствительности к определенному препарату. Таким образом, удается узнать, во-первых, какие микроорганизмы присутствуют в области поражения, и, во-вторых, подобрать наиболее эффективный и действующий агент. Но следует помнить, что системная антибиотикотерапия не должна быть единственным методом лечения, а лишь представлять собой сегмент комплексного подхода обследования, диагностики и разработки адекватной системной терапии. Антибиотикотерапия, как и какой-либо другой метод лечения, имеет свои преимущества и недостатки. Поскольку прием данных препаратов является довольно таки известным методом лечения, пациенты, как правило, понимают основные ключевые моменты данного лечения, и без проблем соглашаются на предложенный алгоритм курса медикаментов. Но вместе с тем, пациенты часто могут путать официальные основные наименования лекарств, забывать дозу, время или даже сам факт их приема, нарушая тем самым эффект их действия. Системные антибиотики могут вызывать побочные эффекты и нарушения функционирования желудочно-кишечной системы в форме диареи или абдоминальных спазмов. Другие возможные негативные влияния препаратов связаны с аллергическими реакциями и возникновением резистентности бактерий к антибиотикам при их длительном и неконтролируемом приеме. Бактериальная резистентность является серьезной проблемой в медицине, поскольку она формирует ряд других научно-клинических дилемм относительно терапевтического соотношения риска лечения против потенциальной пользы от приема антибиотиков.
Системные антибиотики достигают тканей пародонта путем транссудации из сыворотки крови, после чего проходят через соединительный эпителий и выстилку десневого кармана, чтобы попасть в область десневой борозды. Эффективная концентрация антибиотика при достижении им десневой борозды во время курсового приема отличается от таковой в любой другой системе тканей или органе с признаками инфицирования, что связано со специфической структурой пародонта. Существует ряд уже хорошо апробированных схем приема антибиотиков для лечения заболеваний пародонта, которые, как правило, используются в сочетании с механическим удалением над- и поддесневых отложений и бактериального налета. Данный подход в комплексе с эффективной домашней гигиеной полости рта направлен на снижение бактериальной нагрузки в области тканей десны выше и ниже маргинальной границы. Некоторые врачи обычно назначают схемы антибиотикотерапии для лечения и управления заболеваниями пародонта на основе амоксициллина (375 мг) и метронидазола (500 мг) при приеме препаратов 3 раза в день в течение 7 дней в сочетании с проведением скейлинга ротовой полости и полной очисткой области корней в первые 48 часов. Такой подход помогает достичь уменьшения глубины карманов и снизить уровень кровотечения, что было обнаружено при сравнении результатов лечения в исследуемой и контрольной группах. Альтернативная схема лечения предусматривает прием азитромицина (500 мг) в течение 3 дней до проведения процедуры полного удаления зубного камня и очистки поверхности корней, чтобы уменьшить количество бактерий красного комплекса и снизить показатели гингивального индекса. При отсутствии возможностей проведения посева культуры бактерий и определения их чувствительности к антибиотикам, можно пользоваться эмпирическим принципом назначения препаратов для лечения пародонтита. Обоснованные варианты лечения включают в себя комбинацию амоксициллина и метронидазола (250 мг - 500 мг каждого) с приемом препаратов 3 раза в день в течение 8 дней, или комбинацию метронидазола и ципрофлоксацина (500 мг) в течение 8 дней по 2 раза в сутки.
Местная антибиотикотерапия является альтернативным адъюватным вариантом лечения, который также может применятся в ходе лечения поражений пародонта. Суть процедуры состоит в доставке антибиотика непосредственно в пародонтальный карман – то есть прямо в место колонизации патогенных бактерий, при этом концентрация антибиотика в области поражения по сравнению с системным приемом заметно увеличивается. Другим преимуществом является отсутствие потенциальных нарушений расстройств желудочно-кишечного тракта и аллергических реакций. Первым антибиотиком, используемым для местного лечения, был Actisite (пародонтальный тетрациклин). Он состоял из нерезорбируемых, пропитанных тетрациклином, волокон, которые помещались непосредственно в пародонтальный карман и оставались там в течение 10 дней – вплоть до следующего визита к стоматологу. Со временем проходило усовершенствование препаратов и методов их доставки в область пародонтального поражения. Таким образом, был разработан Atridox (Denmat), который является первым резорбируемым антибиотиком местного действия, состоящим из гелевой формы доксициклина. Данный препарат вводится в карман с помощью шприца, и при контакте со слюной – затвердевает, приобретая восковую консистенцию. Таким образом, антибиотик может выделятся из затвердевшей фазы на протяжении 21 дня. Arestin (Orapharma) также является представителем местных рассасывающихся препаратов антибактериального действия, который состоит из гранул миноциклина в форме порошка. Поставляется он в виде ампул, заряженных в шприц. Порошок вводится непосредственно в пародонтальный карман, высокий уровень его терапевтического действия продолжается в течении 14 дней, а сам препарат остается в кармане на протяжении 28 суток. Исследования доказали, что использование антибиотиков местного действия вместе с процедурой полного удаления зубного камня и очисткой поверхности корней позволяет добиться клинически эффективных результатов: наблюдается уменьшение глубины карманов и частичное восстановление нарушенного биологического прикрепления.
Противомикробные ополаскиватели полости рта
Противомикробные полоскания являются хорошо известными и приемлемыми процедурами, эффективно дополняющими комплексное лечение воспаления тканей десен. Примерами аргументированного их использования являются ситуации, когда пациент не в состоянии обеспечить оптимальный уход за полостью рта с помощью обычных гигиенических средств в домашних условиях, например, в послеоперационный период. Чтобы правильно выбрать ротовой ополаскиватель, который бы эффективно справлялся с воспалением десен и в то же время с профилактикой зубного налета, нужно узнать имеет ли он Сертификат одобрения Американской стоматологической ассоциацией. Если да, то данный продукт прошел через ряд клинических, биологических и лабораторных испытаний, которые доказали его противовоспалительную и антибактериальную эффективность. Однако, следует понимать, что данная оценка является рекомендательной, но никак не директивной в отношении препарата. Единственными ополаскивателями, доступными на рынке с соответствующей оценкой Ассоциации, являются представители с фенольными составляющими, по типу Listerine и других аналогичных версий. Золотым стандартом среди антимикробных ополаскивателей также считается хлоргексидин глюконат (0,12%), который в США отпускается лишь по рецепту и известен под коммерческими названиями Peridex и PerioGuard (Colgate-Palmolive). Хлоргексидин является наиболее эффективным антимикробным ополаскивателем, снижающим число бактерий и обеспечивающим эффективное лечение гингивита. Препарат более эффективен в отношении грамположительных бактерий и дрожжей, и менее эффективен в борьбе с грам-отрицательными патогенами. Его обычно назначают в послеоперационный период для снижения бактериальной нагрузки в период заживления. Хлоргексидин имеет высокую субстантивность, что обеспечивает его пролонгированное действие. Некоторые побочные эффекты, связанные с использованием хлоргексидина, включают потенциальное окрашивание зубов и спинки языка; изменение вкусовых восприятий; риск возможного образования наддесневого камня, формирование признаков мукозита и десквамации эпителия. Другими противомикробными ополаскивателями, доступными для широких масс, но менее часто рекомендованными специалистами, являются производные четвертичного аммония, такие как Cepacol (Reckitt Benckiser). Продукты на основе сангвинарина, по типу Viadent, больше широко не доступны на рынке. Продукты на основе оксигенатов, как пероксид водорода, рекомендуется чаще использовать в форме пасты. Они владеют противовоспалительными свойствами, благодаря которым уменьшаются признаки кровотечения. Последнее является важным критическим показателем для оценки воспаления пародонта. Однако данные представители имеют лишь небольшое влияние на уровень бактериальной контаминации, а в последнее время все чаще высказывается мнение об их возможном канцерогенном потенциале. Триклозан является еще одним антимикробным агентом, поставляющимся в форме зубных паст и ополаскивателей. Тем не менее, согласно данных исследований, он тоже демонстрирует минимальное влияние на микробную флору полости рта, а безопасность его использования до сих пор находится под вопросом.
Противовоспалительные агенты
Мы должны помнить, что заболевания пародонта имеют инфекционную природу, а воспалительные явления являются иммунным ответом организма на микробную контаминацию. В воспаленных тканях процесс размножения патогенных бактерий происходит быстрее, что приводит к прогрессированию патологических и разрушительных эффектов воспалительного процесса, посредством активации клеток иммунной системы организма (макрофагов и их предшественников, моноцитов, лимфоцитов, и полиморфноядерных лейкоцитов, таких как нейтрофилы). Компоненты микробной структуры, по типу липополисахарида, который находится в стенках клеток грамотрицательных анаэробных микроорганизмов, активируют макрофаги для продуцирования и секретирования провоспалительных цитокинов, таких как интерлейкин-1 (IL-1) и фактор некроза опухолей-альфа (TNF-alpha). Интерлейкин-1 стимулирует резорбцию кости, а также способствует высвобождению PGE2 клетками фибробластов, которые являются основными и наиболее распространенными типами клеток соединительной ткани. Фибробласты синтезируют коллаген – основной структурный белок соединительной ткани, который является также основным компонентом волокон десны и кости. Данные клетки и клетки воспалительной реакции (нейтрофилы и макрофаги) синтезируют матриксные металлопротеиназы (ММР), которые представляют собой ферменты или белки, участвующие в ряде биологических реакций. Например, ММР-1 и ММР-8 являются ферментами, которые принимают участие в деградации коллагена, что значительно ослабляет структуру пародонта. Активация иммунной системы по своей сути является защитной реакцией организма – ответом на бактериальную инвазию, однако в ходе механизма реализации иммунного ответа происходит разрушение тканей самого организма-хозяина. Данный феномен связан с высвобождением цитокинов, провоспалительных медиаторов и ММР, поскольку данные агенты действуют не только локально на ткани пародонта, но попадая в кровоток могут вызвать и нежелательные системные эффекты.
ММР являются группой протеолитических ферментов, обнаруженных в тканях пародонта, которые в своем составе имеют коллагеназу и желатиназу. Функция данных ферментов состоит в ремоделировании внеклеточного матрикса. Поскольку исследователями было обнаружено, что доксициклин имеет антиколлагенлитические свойства, они предложили использовать его в качестве модуляторного агента для лечения пародонтита. Субантимикробные дозы доксициклина (20 мг дважды в день) являются эффективными для ингибирования активности коллагеназы, и в то же время никак не влияют на фактор антимикробной резистентности при его использовании в сочетании с полным удалением зубного камня и очисткой поверхности корней. Такой подход обеспечивает максимальный эффект для восстановления биологического прикрепления тканей и снижения глубины пародонтальных карманов.
Пероральные лекарственные средства
Нестероидные противовоспалительные препараты (НПВП) также были изучены в качестве ингибиторов реакции организма хозяина при лечении заболеваний пародонта. Механизм их действия состоит в предотвращении продукции простагландинов. Простагландин Е2 (PGE2) напрямую ассоциирован с процессами воспаления и резорбции костной ткани, что подтверждено его верификацией в пораженных пародонтальных участках. В ходе изучения различных НПВП (флурбипрофен, ибупрофен, кеторолак, напроксен, аспирин), которые вводились системно или локально, было обнаружено, что при их сочетании с процедурой полного удаления зубного камня и очисткой поверхности корней, удавалось сохранить имеющуюся высоту альвеолярного гребня, предупреждая его резорбцию. Бисфосфонаты представляют собой класс препаратов, ингибирующих резорбцию альвеолярной кости, которые также были использованы в качестве хост-модулирующих агентов при лечении заболеваний пародонта. Исследования показали, что бисфосфонаты при использовании в сочетании с полной очисткой полости рта, обеспечивают снижение глубины пародонтальных карманов и уровня кровотечения во время зондирования, а также улучшают восстановление биологического прикрепления и обеспечивают сохранение высоты альвеолярного гребня. Однако, несмотря на потенциальные преимущества бисфосфонатов, исследования показали, что длительное применение и высокие дозы препаратов инициируют остеонекроз челюстей. Очевидно, что для аргументированных выводов необходимо проведение дальнейших более детализированных исследований, которые помогут определить соотношение потенциальной пользы препаратов и относительного риска осложнений в процессе лечения пародонтита.
Хост-модулирующая терапия
Локальное применение хост-модулирующих агентов, таких как эмалевые матриксные протеины, костные морфогенетические белки и тромбоцитарные факторы роста, может быть довольно эффективным в ходе комплексного лечения пародонтита. Эмалевые матриксные протеины доступны в форме препарата Emdogain (Straumann) и успешно используются в ходе восстановления пародонтальных дефектов. Данные белки играют роль модуляторов заживления, стимулируя регенерацию всех пародонтальных компонентов поддерживающего аппарата зуба. Костные морфогенетические белки способствуют модуляции и дифференциации мезенхимальных клеток в клетки-предшественники костной ткани. Они действуют в качестве каркаса, на который может наращиваться новая костная ткань, и часто используются при направленной костной регенерации во время аугментации альвеолярного гребня. Наконец, тромбоцитарные факторы роста усиливают хемотаксис нейтрофилов и моноцитов, стимулируют пролиферацию фибробластов, а соответственно и синтез внеклеточного матрикса, а также повышают уровень дифференциации мезенхимальных клеток-предшественников, фибробластов и эндотелиальных клеток. Именно тромбоцитарные факторы роста наиболее часто используется при хирургических вмешательствах на тканях пародонта с целью ускорения их регенерации.
Выводы
Новые знания относительно хост-бактериальных взаимодействий и иммунных реакций организма, которые провоцируют поражение тканей пародонта, станут полезными для разработки более новых и эффективных концепций лечения пародонтита с использованием системных и местных антибиотиков, антимикробных ополаскивателей и принципов хост-модулирующей терапии. Результаты дальнейших исследований могут пролить свет на вспомогательную адьювантную терапию, которая может быть использована для коррекции алгоритмов лечения с целью достижения наиболее успешного эффекта комплексной терапии поражений поддерживающего аппарата зуба.
Читайте также:

