Воспаление десен после лучевой терапии
Опубликовано: 17.04.2024






Лучевой стоматит - как уменьшить боль? 25.08.2020 12:25
Мукозит полости рта - это острое воспаление и изъязвление поверхности рта и горла. Оральный мукозит - серьезная проблема у пациентов, получающих химиотерапию или лучевую терапию. Это болезненное состояние, которое может ограничивать потребление пищи а также быть причиной сокращения, отсрочки или прекращения химиотерапии или лучевой терапии и / или продления госпитализации. Между тем, сокращение или приостановка курса лучевой или химиотерапии, значительно снижает выживаемость при онкологических заболеваниях. Однако продолжать курс лучевой терапии при оральном мукозите не всегда возможно, так как:

Боль в полости рта при лучевом стоматите связана с тем, что при лучевой или химиотерапии разрушается защитный слой эпителия полости рта, который состоит из гиалуроновой кислоты и хондроитинсульфата. В результате слизистая оболочка полости рта покрывается язвами. Пища попадает в эти язвы - вызывая боль. Кроме того, в них развивается инфекция.

Еще одним неприятным симптомом является сухость во рту, так как слюнные железы также страдают от лучевой или химиотерапии.
Д ля лечения лучевого стоматита в Швейцарии был разработан гель "Gelclair", который представляет собой вязкий пероральный гель на основе гиалуроновой кислоты. Гиалуроновая кислота образует защитную пленку, которая прилипает к слизистой оболочке полости рта и очень хорошо переносится. Пленка из гиалуроновой кислоты защищает обнаженные из-за поражений полости рта нервы в течение 5-7 часов после первого применения, обеспечивая 92% уменьшение боли. Gelclair может помочь пациентам поддерживать нормальное питание и потребление жидкости, а также пройти полный курс химиотерапии и лучевой терапии.
Поскольку Gelclair не зарегистрирован в России, его привозят разными способами))) Цена в итоге достигает абсолютно нереальных масштабов. Поэтому мы разработали, официально зарегистрировали и выпускаем российский аналог Gelclair - гель "ВИТА-ГИАЛ". Цена "ВИТА-ГИАЛа" значительно ниже зарубежных аналогов ("Капосол", "Gelclair") при сопоставимом качестве. Гель "ВИТА-ГИАЛ" стоит в районе 290 рублей, раствор для обработки полости рта "ВИТА-ГИАЛ" около 480 рублей.
Наибольший эффект гель "ВИТА-ГИАЛ" дает при комбинации с анестетиком, например лидокаином (разумеется, при отсутствии аллергии).
Для приготовления смеси геля "ВИТА-ГИАЛ" с лидокаином берется 15 мл геля (1 ст. ложка), 20 мл 10% раствора лидокаина и 20 мл 0,9% хлорида натрия или 20 мл линкомицина. Затем компоненты перемешиваются в стакане или чашке до получения однородного раствора.
Полученный раствор нужно удерживать в полости рта не менее 1 минуты и затем выплюнуть. Глотать раствор нежелательно, хотя вреда от этого не будет.
Применять 3 раза в день или чаще (при необходимости) за 30 - 60 минут до приема пищи.
Остеорадинекроз (ОРН) нижней челюсти является серьезным осложнением, которое может возникнуть у пациентов после курса радиотерапии в ходе комплексного лечения новообразований области головы и шеи. Предрасполагающими факторами при этом остаются доза облучения, локализация опухоли, травма зубов в анамнезе и компрометированное состояние стоматологического статуса.
Чаще всего именно у пациентов возрастной категории 50+ регистрируются новообразования головы и шеи и, как правило, у большинства пациентов в этом возрасте имеются дентальные имплантаты, которые играют роль опорных элементов под ортопедические конструкции. Результаты дентальной имплантации, как и состояние периимплантантных тканей, являются некими составляющими элементами в структуре этио-патофизиологического процесса возникновения радионекроза челюстей после проведённой радиотерапии.
Имеющиеся на сегодня исследования по большей мере сконцентрированы на изучении перспектив дентальных имплантатов, установленных до процедуры терапевтического облучения, или же на определении прогноза таких конструкций после такого ятрогенного вмешательства. Но вопрос эффекта радиотерапии на полностью остеоинтегрированный имплантат по-прежнему остается дискуссионным и открытым, поэтому данная статья посвящена описанию изменений периимплантатных структур после терапевтического облучения на примере конкретного клинического случая.
Клинический случай
66-летний пациент был направлен в нашу больницу для дальнейшего лечения ОРН нижней челюсти. 7 лет назад ему проводилась установка титановых инстраосcальных конструкций на месте отсутствующих 35, 36, 45 и 47 зубов. При этом в ходе определенного времени все установленные имплантаты удачно остеоинтегрировались, что было подтверждено в ходе численных повторных контрольных визитов.
Через некоторое время у него диагностировали левостороннюю ротоглоточную карциному, лечение которой проводили посредством лучевой терапии с общей дозой 70 Гр через 2 года после имплантационного вмешательства. В ходе анализа медицинской документации было обнаружено, что левая челюсть была включена в зону терапевтического облучения.
Через 4 года после радиотерапии пациент начал испытывать болевые ощущения в области имплантатов, установленных с левой стороны, в том же участке у него наблюдалось значительное воспаление и отечность десен. После постановки диагноза периимплантита ему было проведено консервативное лечение, состоящее из местной ирригации области поражения и периодического приема антибиотиков на протяжении 6 месяцев. Однако симптомы поражения только усиливались, и он был направлен в нашу больницу для проведения дальнейшего лечения патологии.
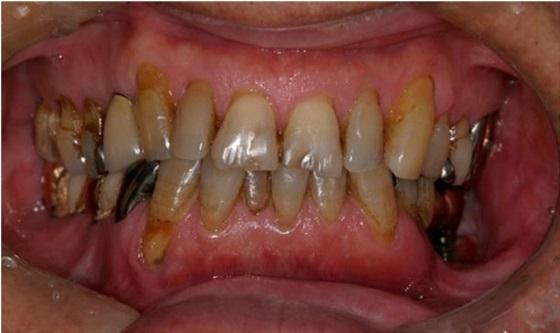
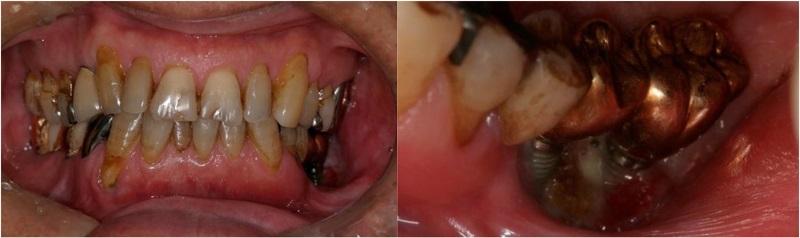
В ходе клинического исследования у пациента был обнаружен болезненный отек левой щеки и гипестезия нижней губы с левой стороны, при этом возможность открытия рта была ограничена до ширины полтора пальца, а вокруг дентальных имплантатов с левой стороны наблюдался некроз альвеолярной кости, воспаление слизистой и периодическое гноеотделение (фото 1).
Фото 1. Клиническая ситуация до лечения.
На ортопантомограмме контурировалась слабо демаркационная зона деструкции костной ткани в области имплантатов на месте 35 и 36 зубов, при этом поражение достигало нижнего края челюсти, что в результате спровоцировало возникновение патологического перелома. Вокруг имплантатов с правой стороны челюсти никаких патологических поражений отмечено не было (фото 2). С помощью КТ-сканирования удалось подтвердить деструкцию нижней челюсти слева и наличие линии перелома через всю толщу костной ткани (фото 3).
Фото 2. Ортопантомограмма пациента до лечения.
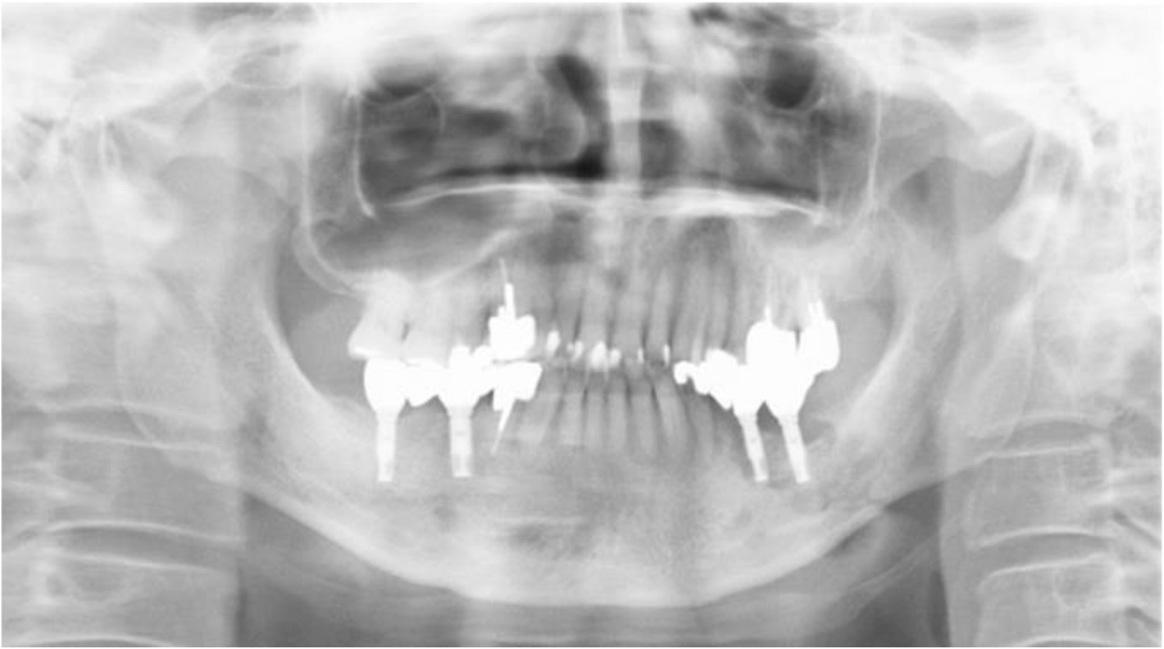
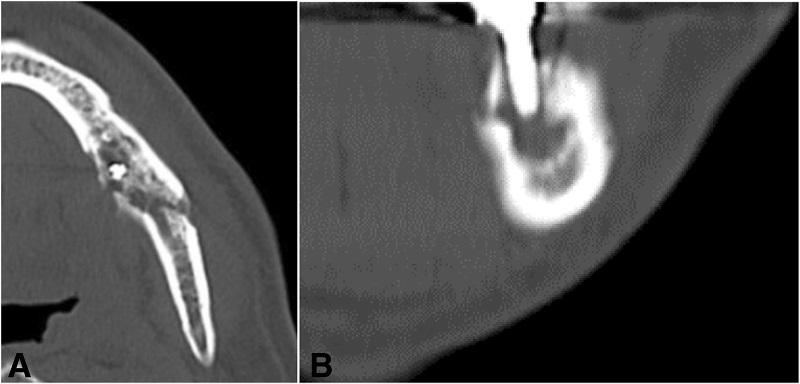
Фото 3. КТ-изображения нижней челюсти с левой стороны: а) аксиальный срез в области левого первого моляра; b) корональный срез в области левого первого моляра.
На первом этапе лечения пациент прошел курс 30 сеансов гипербарической кислородной терапии, что позволило лишь незначительно улучшить имеющиеся симптомы поражения. Учитывая, что на рентгенологических снимках не было замечено никакого прогрессирования области деструкции, была проведения частичная резекция области нижней челюсти с последующим восстановлением дефектного участка посредством свободного микроваскулярного лоскута из малоберцовой кости. Фиксация трансплантата проводилась с использованием титановой пластины (фото 4).
Фото 4: а) Сегментированная резекция пораженного участка нижней челюсти; b) локализированный костный трансплантат из области малоберцовой кости; c) резецированная нижняя челюсть; d) ортопантомограмма после операции.
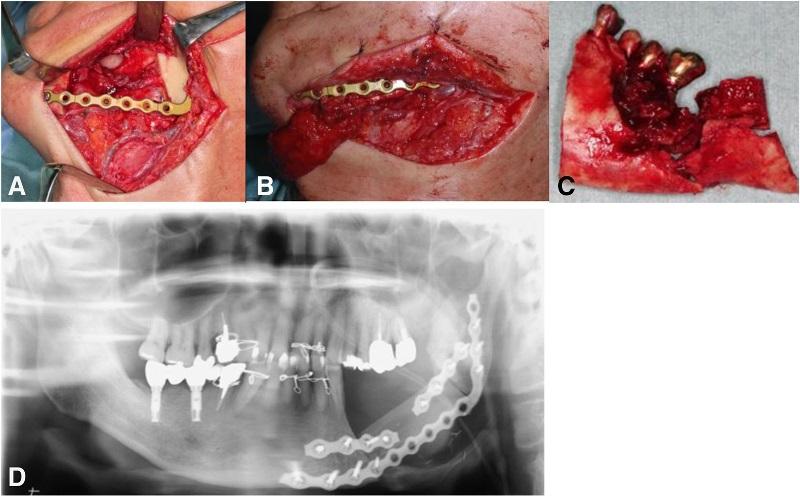
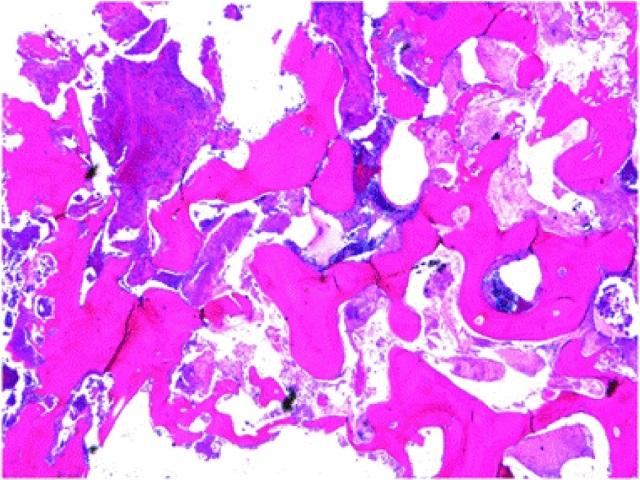
В ходе гистопатологического исследования резецированного участка нижней челюсти было обнаружено потерю остеоцитов и остеобластов в структуре ткани и заполнение костных полостей грибковой массой, а также инфильтрацию области поражения воспалительными клетками с присутствующими признаками фиброза в кости (фото 5).
Фото 5. Гистологический вид резецированного участка нижней челюсти (окраска гематоксилин-эозином).
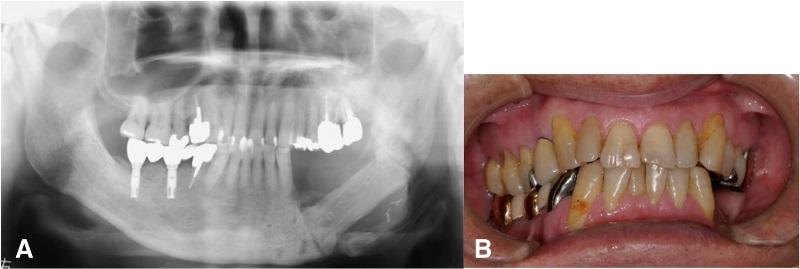
В качестве окончательного был поставлен диагноз остеорадионекроз. В ходе послеоперационного наблюдения никаких дополнительных поражений в области других имплантатов замечено не было, признаки остеорадионекроза челюсти не рецидивировали, резидуальная часть тканей оставалась интактной (фото 6).
Фото 6. a) Ортопантомограмма через год после хирургического вмешательства; b) вид полости рта через 1 год после хирургического вмешательства.
Обсуждение
В данной статье проанализирован клинический случай возникновения ОРН нижней челюсти вокруг дентальных имплантатов, установленных до начала проведения лучевой терапии у пациента.
По нашим наблюдениям, это уже третий подобный случай, описанный в литературе. Granström и коллеги сообщали о трех случаях развития ОРН вокруг дентальных имплантатов, помещенных до радиотерапии для поддержки транскожного протеза. В свою очередь Slama также сообщил о случае ОРН нижней челюсти в области имплантатов после терапевтического облучения. Исходя их этого, можно предположить, что наличие имплантата играет некую роль в развитии ОРН у пациента после радиотерапии.
В нашем клиническом случае у пациента имплантаты были установлены с обеих сторон нижней челюсти, но ОРН был зарегистрирован лишь с левой стороны, что связано с целевой областью облучения левосторонней карциномы ротоглотки. Наличие дентального имплантата может повлиять на развитие ОРН посредством сразу двух механизмов. Во-первых, наличие имплантата может спровоцировать изменения в распределении дозы облучения вокруг титановой инфраконструкции, поскольку и раннее было известно, что имплантаты сами по себе инициируют разброс лучевой и электромагнитной энергии, чем провоцируют изменения твёрдых и мягких периимплантатных тканей, при чем Friedrich уже раньше сообщал о подобном биологическом эффекте.
Ozen и коллеги, исследуя повышение дозы от рассеянного излучения на границе раздела фаз костной ткани и дентального имплантата, пришли к выводу, что увеличение радиационной дозы, действующей на альвеолярную кость происходит непосредственно вблизи титанового винта, и может достигать повышения на целых 21%. На расстоянии уже 2 мм от титановой поверхности увеличение ионизирующей дозы было минимальным, при этом, очевидно, что увеличение радиационной локальной нагрузки на 15-21% может спровоцировать процесс остеонекроза нижней челюсти в периимплантатной области. При этом Beyzadeoglu сообщили, что изменение длины пучков облучения, как и угла их прохождения, значительно не влияет на суммарную дозу поражения, которая может спровоцировать остеонекроз.
Из вышеописанного можно сделать вывод, что область интерфейса имплантат-кость подвергается повышенному облучению в результате эффекта рассеивания радиационного потока посредством самой титановой конструкции, которая может находится в поле терапевтического действия радиации.
Кроме того, причина ОРН может крыться в действии бактериальной инфекции, ассоциированной с имплантатом. Часто вокруг фиксированных металлокерамических конструкций, как и вокруг конструкций с опорой на имплантаты, наблюдаются области гингивита, что, в свою очередь, провоцирует удушение состояния гигиены полости рта, а это вызывает дальнейшую повышенную бактериальную контаминацию периимплантатного участка.
Лучевая терапия посредством воздействия на сосуды, фибробласты и различные регуляторные факторы роста провоцирует нарушение процесса физиологического заживления ран, а также вызывает развития специфического состояния – иммунодефицита. Все это, в свою очередь, снижает уровень резистентности периимплантатных тканей относительно бактериальных агентов полости рта, тем самым увеличивая риск развития периимплантита. Slama и коллеги сообщали о случаях наличия периимплантита до начала развития ОРН, и в нашей ситуации периимплантит прогрессировал вплоть до ОРН. Хорошо известно, что защитная функция окружающих тканей намного слабее вокруг имплантатов, чем вокруг естественных зубов, поэтому вполне вероятно, что периимплантатный мукозит, вызванный лучевой терапией, может легко прогрессировать, переходя в агрессивный периимплантит, и последующее более тяжелое инфекционное поражение костей челюсти.
Выводы
В последнее время дентальные имплантаты стали популярной опцией лечения пациентов с симптомами частичной или полной адентии. Как следствие, число пациентов, проходящих через курс радиотерапии и имеющих дентальные имплантаты, также прогрессивно увеличивается. Для детального анализа эффекта облучения на прогноз дентального имплантата необходимо проведение более прецизионных и выборочных исследований, которые помогут сделать однозначные выводы по этому поводу.
Авторы: Yuji TeramotoEmail author, Hiroshi Kurita, Takahiro Kamata, Hitoshi Aizawa, Nobuhiko Yoshimura, Humihiro Nishimaki, Kazunobu Takamizawa
Что может произойти?
Облучение головы и шеи может вызвать следующие проблемы:
• Язвочки и ранки во рту
• Сухость во рту (ксеростомия) и горле
• Потеря вкусовой чувствительности
• Поражение зубов
• Изменения вкуса (металлический привкус при приеме пищи)
• Инфекции десен, зубов или языка
• Изменения в височном суставе и костях
• Изменения слюны
Посетите стоматолога минимум за 2 недели до начала облучения головы или шеи.
Почему это происходит?
Облучение убивает раковые клетки и повреждает нормальные в слюнных железах, слизистой оболочке полости рта.
Как долго это длится?
Некоторые симптомы, например, язвочки во рту, могут уйти по окончании ЛТ. Некоторые (например, изменения вкуса) могут сохраниться месяцами и даже годами. Некоторые могут остаться навсегда (сухость во рту).
Посетите стоматолога минимум за 2 недели до начала облучения головы или шеи.
Как справиться?
• Если назначено облучение головы или шеи, посетите стоматолога минимум за 2 недели до начала облучения головы или шеи. Стоматолог обследует полость рта и зубы, возможно, проведет необходимое лечение. Если возможости посетить стоматолога до начала ЛТ нет, спросите врача, следует ли Вам обратиться к стоматологу после начал ЛТ.
• Исследуйте свой рот каждый день. Т.о. Вы обнаружите проблемы (язвочки, белый налет, инфекция) как можно раньше.
• Увлажняйте полость рта.
Как этого достичь:
o Часто пейте воду
o Сосите леденцы без сахара
o Жуйте жвачку без сахара
o Используйте заменитель слюны
o Попросите врача выписать препараты для увеличения слюны
• Чистите зубы, десна и язык после каждого приема пищи и перед сном
o Пользуйтесь самой мягкой зубной щеткой. Чтобы сделать щетинки еще более мягкими, сполосните их теплой водой перед началом чистки зубов.
o Пользуйтесь фторсодержащими пастами.
o Пользуйтесь специальным фторсодержащим гелем.
o Не используйте средства для ополаскивания полости рта, содержащие алкоголь.
o Аккуратно пользуйтесь зубной нитью (флоссом) каждый день. Не обрабатывайте лишь кровоточащие области и болезненные.
o Полоскайте рот раз в 1-2 часа раствором: четверть чайной ложки соды и 1/8 чайной ложки соли на стакан теплой воды.
o Если у Вас есть зубные протезы, убедитесь, что они хорошо подогнаны. При потере веса может потребоваться изготовить новые протезы.
o Чистите и промывайте зубные протезы каждый день.
• Уделяйте внимание тому, что Вы едите, когда во рту появились язвочки.
o Выбирайте продукты, которые легко жевать и глотать.
o Откусывайте немного, жуйте медленно и запивайте жидкостью.
o Ешьте влажные мягкие продукты.
o Не ешьте слишком горячую или холодную пищу.
• Избегайте всего, что может повредить полость рта, например:
o Твердая хрустящая пища (чипсы, орехи, сухарики)
o Горячая пища
o Острая пища
o Фрукты и соки с высоким содержанием кислот (томаты, цитрусовые)
o Зубочистки и другие острые предметы
o Все табачные изделия (сигареты, сигары, трубки, жевание табака)
o алкоголь
• Избегайте продуктов и напитков с высоким содержанием сахара. Такие продукты могут повредить зубы.
• Разминайте височный сустав 3 раза в день.
• Упражняйте жевательные мышцы. Открывайте и закрывайте рот 20 раз. Делайте это 3 раза в день.
• Лекарственные препараты. Узнайте у врача о препаратах, защищающих слюнные железы и слизистую полости рта.
• Сообщите врачу, если будет болеть в полости рта. Есть препараты и гели, справляющиеся с болью.
• Вам потребуется особенно тщательно ухаживать за полостью рта в течение всей жизни. Спросите у стоматолога, как часто потребуется посещать его и как лчуше ухаживать за полостью рта по окончании ЛТ.
Избегайте табачных изделий и алкоголя во время облучения головы и шеи.
Е. Ф. Дмитриева
аспирант кафедры ортопедической стоматологии и ортодонтии Федерального государственного бюджетного образовательного учреждения высшего образования «ЮУГМУ» Министерства здравоохранения Российской Федерации
Н. С. Нуриева
д. м. н., профессор кафедры ортопедической стоматологии и ортодонтии ГБОУ ВПО «ЮУГМУ» Минздрава России (Челябинск)
Онкологическая заболеваемость у людей постепенно увеличивается в течение последнего столетия. Число заболеваний злокачественными опухолями головы и шеи также неуклонно увеличивается, достигая в большинстве регионов России 20—25 % от всех злокачественных опухолей. В частности, опухоли органов орофарингеальной области составляют 5,1 % от всех опухолей [3].
Современная стратегия лечения больных плоскоклеточным раком органов головы и шеи включает применение хирургического метода, лучевой терапии, химиотерапии и таргентной терапии, а также различные варианты комбинированного лечения. Среди различных методов лечения в клинической онкологии лучевая терапия занимает одно из ведущих мест. По данным ВОЗ, 70—75 % онкологических больных нуждаются в проведении лучевой терапии.
Несмотря на последние достижения онкологии, в настоящее время после комбинированного и лучевого лечения злокачественных новообразований челюстно-лицевой области невозможно избежать осложнений, связанных с ионизирующим излучением. В частности, побочным результатом лучевой терапии является интенсивное разрушение зубов. Поражение твердых тканей зубов связывают как с непосредственным действием на них лучистой энергии, так и с последующим иммунодепрессивным состоянием, нарушением минерального и белкового обменов, количества и состава слюны, функционального состояния важнейших физиологических систем организма [4].
Цель исследования
Изучить особенности клинической картины лучевого кариеса зубов в зависимости от времени, прошедшего после завершения лучевого лечения опухолей орофарингеальной зоны, что позволяет провести диагностику заболевания на ранних стадиях.
Материал и методы исследования
Данная работа основана на опыте клинического наблюдения 60 пациентов со злокачественными новообразованиями орофарингеальной зоны II—IV стадии в возрасте от 22 до 75 лет. В подавляющем большинстве случаев гистологическое заключение — плоскоклеточный рак (в 97 % случаев), в 3 % случаев идентифицирована карцинома. Осмотренные пациенты получали СПЛИТ-курс ДЛТ: за 2 этапа на опухоль подводится СОД = 66—70 изоГр, на л/узлы шеи СОД = 44—50 изоГр, на метастазы в л/узлы шеи СОД = 60—70 изоГр, на очаги лимфаденопатии более 2,0 см СОД = 60 изоГр. Все пациенты завершили курс лучевой терапии. Наблюдение проводили через 1, 6, 12 и 24 месяца после завершения лучевой терапии. Ни один из пациентов не получал поддерживающей стоматологической терапии на этапах лечения и после выписки. Лучевой кариес при осмотре диагностирован в 100 % случаев через два года после завершения специализированного лечения (рис. 1, 2).
Изменения в облученных зубах мы подразделили следующим образом.
Лучевой кариес 1-й степени: потеря блеска, прозрачности эмали, появление меловидных пятен как проявление деминерализации поверхностного слоя эмали. При этом никаких признаков разрушения и образования дефекта эмали нет. При зондировании полости не определяются. В области шейки зубов по эмалево-цементному соединению обнаруживается застревание зонда. Пациенты, как правило, не жалуются на спонтанную боль или боль от температурных раздражителей. Температурная проба (на холодное) положительная.
Лучевой кариес 2-й степени: в основном прогрессирование кариозного процесса наблюдается в пришеечной области. Характерны разрушение участков эмали, полости с подрытыми краями. Распад не затрагивает дентин. Изменения в цвете могут быть от коричневого до черного. Могут отмечаться повышенная стираемость эмали на режущем крае и хрупкость, отколы эмали. Пациенты, как правило, не жалуются на спонтанную боль или боль от температурных раздражителей. Температурная проба (на холодное) либо слабоположительная, либо отрицательная.

Рис. 1. Пациент В., 63 лет. Лучевой кариес.

Рис. 2. Пациент У., 68 лет. Лучевой кариес.
Лучевой кариес 3-й степени: полное разрушение эмали, распад эмалево-дентинной границы. Дентин размягчен при зондировании. Положительная перкуссия. Без самопроизвольного вскрытия пульпы. Пациенты, как правило, не жалуются на спонтанную боль или боль от температурных раздражителей. Тепловая проба отрицательная. Отсутствие боли основано на потере жизнеспособности и чувствительности пульпы.
Лучевой кариес 4-й степени: полное разрушение коронки зуба, пульповая камера вскрыта, дентин размягченный, темного цвета. Боль либо отсутствовала, либо имели место периодонтитные боли.
В таблице представлены сроки возникновения лучевого кариеса.
Результаты и обсуждение
Лучевой кариес зуба (c. dentis radialis) — генерализованный кариес зуба, развивающийся как осложнение рентгено- или радиотерапии челюстно-лицевой области; протекает с пигментацией и размягчением поверхностных слоев и образованием глубоких пришеечных полостей.
Патогенез лучевого поражения зубов до сих пор окончательно не выяснен. Так, обсуждаются данные о сосудистых, морфологических и дегенеративных нарушениях в пульпе, предшествующих поражению твердых тканей зубов [1]. В полости рта на фоне проведения лучевой терапии челюстно-лицевой области создается кариесогенная ситуация за счет развития радиоиндуцированной ксеростомии, нарушения микрофлоры полости рта, затруднения гигиены полости рта, снижения самоочищения ротовой полости и общего снижения иммунитета. Несмотря на большое количество исследований по этиологии радиоиндуцированного кариеса, до сих пор имеются противоречия в мнениях о первопричинности его возникновения: прямое воздействие радиации или длительное опосредованное воздействие неблагоприятных факторов, возникающих в полости рта после облучения, основным из которых является радиоиндуцированная ксеростомия.
До настоящего времени не сложилось единого мнения о характере лучевого повреждения зубов. Одни авторы рассматривают такие поражения как некариозные, другие — как остро протекающий кариозный процесс.
Клинические проявления последствий радиационного воздействия могут быть весьма различны и зависят от полученной дозы облучения и вида ионизирующей радиации [2]. Обычно спустя 3—6 мес. после лучевого воздействия эмаль зубов утрачивает характерный блеск, становится тусклой, серовато-блеклого цвета. Отмечаются ломкость, стертость жевательной и вестибулярной поверхности зубов. На этом фоне появляются участки некроза, вначале локальные, а затем по типу циркулярного поражения зубов. Указанные поражения обычно темного цвета, заполненные рыхлой некротической массой, безболезненные.
Отсутствие болевого симптома — характерная особенность радиационного поражения, свидетельствующая о подавлении функции одонтобластов. Постепенно участки некроза расширяются и захватывают значительную часть зуба. Удаление некротических масс из очага поражения, как правило, безболезненно, поэтому требует особой осторожности. Если не применять радикальных вмешательств, через 1—2 года окажутся пораженными более 96 % зубов [7].
Таблица № 1. Сроки возникновения лучевого кариеса у пациентов, получавших лучевое лечение опухолей орофарингеальной зоны, %

- опухоли
- рак
- меланома
1. Лучевая терапия и побочные эффекты
Лучевая терапия – это метод лечения рака с помощью высокой энергии, которая убивает опухолевые клетки. Целью лучевой терапии является уничтожить раковые клетки, не повредив здоровые.
У разных людей есть разные побочные эффекты от лучевой терапии и воздействия излучения. У кого-то их совсем мало и они умеренные. А у других людей побочные эффекты лучевой терапии могут быть очень серьезными и в большом количестве. К сожалению, предсказать заранее это невозможно. Помимо индивидуальной реакции побочные эффекты зависят от вида излучения, его дозы, площади тела, которая облучается, и состояния здоровья пациента.
Как быстро проявляются побочные эффекты от лучевой терапии?
На самом деле, есть два вида побочных эффектов после лучевой терапии – ранние и поздние. Первые побочные эффекты лучевой терапии, такие как тошнота и усталость, как правило, носят временный характер. Они появляются во время или сразу после лечения и длятся еще несколько недель после окончания лечения. Но со временем эти симптомы пропадают. Поздние побочные эффекты от лучевой терапии, такие как проблемы с сердцем или легкими, могут развиваться в течение нескольких лет. И часто они приобретают хроническую форму.
Самыми распространенными побочными эффектами от лучевой терапии является усталость и проблемы с кожей. Другие ранние эффекты – выпадение волос и тошнота, обычно связаны с воздействием излучения на определенную часть тела.
Что делать с усталостью при лучевой терапии?
Усталость из-за рака или после лучевой терапии может быть очень сильной. Такой, что она не позволит вести привычный образ жизни. В какие-то дни усталость может усиливаться, а в другие – становится лучше.
Иногда врачи находят и другие причины усталости. И в этом случае удается уменьшить эту проблему. Уровень усталости часто связан с состоянием здоровья пациента. Поэтому больным раком важно лечить не только онкологию, но и другие сопутствующие заболевания. Вовремя принимайте лекарства, назначенные врачом. Побольше отдыхайте, поддерживайте допустимый уровень физической активности и хорошо питайтесь. Соблюдайте баланс между нагрузками и отдыхом. Перебор с постельным режимом может делать вас уставшим еще больше. Но и не перенапрягайтесь, отдыхайте, если это нужно.
Усталость после лучевой терапии обычно бывает временной и проходит через несколько недель после окончания курса лечения.
2. Проблемы с кожей, выпадение волос, проблемы с пищеварительной системой
Лучевая терапия и проблемы с кожей
Еще один побочный эффект лучевой терапии проявляется в том, что кожа выглядит как после долгого пребывания на солнце. Она может быть красной и загорелой. Иногда появляются отеки и волдыри, сухость, шелушение и зуд. Кожа может «слезать», как будто вы обгорели на солнце.
Поэтому для облегчения состояния кожи после лучевой терапии нужно придерживаться нескольких рекомендаций:
- Не носите тесную одежду в области, на которую воздействует излучение;
- Не трите кожу, используйте мягкое мыло и теплую воду для умывания;
- Не прикладывайте ничего холодного или горячего на пострадавшие участки без рекомендации врача;
- Проконсультируйтесь с врачом, прежде чем использовать любые мази, масла, крема или лосьоны;
- Избегайте солнца. Носите закрытую одежду и спросите у врача о том, какие солнцезащитные средства лучше использовать;
- Если лучевая терапия используется для лечения рака молочных желез, не носите бюстгальтер. Или выбирайте хлопчатобумажные модели без косточек;
- Не бинтуйте пораженные участки, если этого не рекомендовал врач.
Раздражение кожи уменьшается через несколько недель после окончания лучевой терапии. Но даже после выздоровления кожа может приобрести более темный оттенок. И в любом случае после лучевой терапии нужно защищать кожу от солнца в течение года после курса лечения.
Выпадение волос при лучевой терапии
Выпадение волос после лучевой терапии бывает у тех пациентов, которые получают излучение в области головы. Если волосы выпадают, это обычно происходит внезапно и в большом количестве Волосы могут выпадать целыми прядями. В большинстве случаев после завершения курса лучевой терапии волосы начинают расти снова. Но они могут быть тоньше или иметь другую структуру.
Один из способов минимизировать потерю волос после лучевой терапии – это укоротить их до начала лечения, чтобы вес волос стал меньше. Если волосы выпадают, обязательно нужно носить головной убор, чтобы защитить голову от солнечных лучей.
Проблемы с пищеварительной системой
Лучевая терапия в зоне головы, шеи или органов пищеварительной системы может стать причиной потери аппетита. Но даже в этом случае важно правильно питаться, чтобы сохранить силы и здоровье.
Вот несколько рекомендаций:
- Ешьте маленькими порциями по пять-шесть раз в день. Это лучше, чем большая тарелка еды три раза в день.
- Попробуйте какие-то новые продукты или наоборот, привычные и любимые блюда. Возможно, они вызовут аппетит.
- Перекусы помогут поддержать силы, когда вы голодны и не имеете возможности полноценно поесть.
3. Проблемы с полостью рта, проблемы со слухом, тошнота, диарея, проблемы в половой сфере
Проблемы с полостью рта
Перед началом лучевой терапии в области головы и шеи обратитесь к стоматологу для тщательного обследования и лечения проблем зубов и полости рта. Радиация может стать причиной неприятных симптомов:
- Язвы в полости рта;
- Отсутствие слюны;
- Сгущение слюны;
- Затрудненное глотание.
Важно рассказать врачам об этих побочных эффектах лучевой терапии. Скорее всего, они помогут справиться с проблемами. В числе прочего для избавления от этих симптомов нужно отказаться от острой и кислой пищи, а также от алкоголя и табака. Полезно часто чистить зубы мягкой щеткой и фторосодержащими зубными пастами.
Проблемы со слухом
Лучевая терапия может привести к ухудшению слуха. Одна из возможных причин – это уплотнение воска в ушах из-за излучения. Об этой проблеме нужно обязательно сообщить врачу.
Тошнота и лучевая терапия
Излучение в области головы и любой части пищеварительного тракта может вызвать тошноту и рвоту. Сообщите врачу об этом симптоме, потому что есть препараты, способные решить проблему.
Диарея
Лучевая терапия в области живота и желудка может вызвать побочный эффект в виде диареи. Диарея обычно начинается через несколько недель после начала лечения. Скорее всего, в этом случае врач назначит специальные препараты и особую диету.
Проблемы в половой сфере
Лучевая терапия в области таза может повлиять на фертильность и половое влечение. Пациенткам, проходящим курс лучевой терапии, противопоказана беременность, так как излучение может серьезно навредить плоду. Лучевая терапия в области таза у женщин способна остановить менструальные периоды и вызвать другие симптомы менопаузы.
У мужчин излучение в районе яичек может повлиять на количество вырабатываемых сперматозоидов и функциональные возможности спермы. Это не обязательно означает невозможность иметь детей. Но в любом случае, проблему стоит обсудить с врачом.
Излучение, воздействующее на область таза, может стать причиной болезненности полового акта у некоторых женщин. Кроме того, из-за лучевой терапии могут появляться рубцы, влияющие на способность влагалища растягиваться. У мужчин излучение может повлиять на нервы и кровеносные сосуды, ответственные за эрекцию.
4. Поздние побочные эффекты от лучевой терапии
Поздние побочные эффекты лучевой терапии могут появиться через несколько месяцев или даже лет после лечения онкологии. Но это еще не означает, что эти побочные эффекты появляются у всех пациентов.
Что может произойти? Например, рубцовая ткань, образовавшаяся под воздействием излучения, может повлиять на работу сердца и легких. Излучение в области живота или таза способно вызвать проблемы с мочевым пузырем, кишечником и сексуальные проблемы.
Еще один возможный побочный эффект – повторная онкология. Есть исследования, которые подтверждают – лучевая терапия обладает канцерогенным эффектом. Хоть и не часто, но у некоторых людей после лучевой терапии и лечения первого рака развивается вторая опухоль. Поэтому при выборе лучевой терапии в качестве метода лечения онкологии важно поговорить с врачом и выявить все возможные плюсы и минусы этого шага.
Читайте также:

