Основные неклеточные компоненты матрикса зубной бляшки
Опубликовано: 17.04.2024
Зубная бляшка. Структура зубной бляшки. Состав зубной бляшки.
Зубная бляшка — наиболее сложный и многокомпонентный биотоп полости рта, в состав которого входят практически все представители микрофлоры полости рта. Количество бляшек и их соотношение значительно варьирует у разных людей и в разные периоды их жизни.
Зубные бляшки — скопления бактерий в конгломерате протеинов и полисахаридов. Матрицу бляшки составляют вещества, попадающие на поверхность зубов со слюной, а также частично образующиеся как метаболиты микроорганизмов. Выделяют над- и поддесневые бляшки, а также бляшки, образующиеся на поверхности зубов и в межзубных щелях. Количественные и качественные изменения микробиоценоза играют решающую роль в возникновении кариеса зубов и пародонтита.
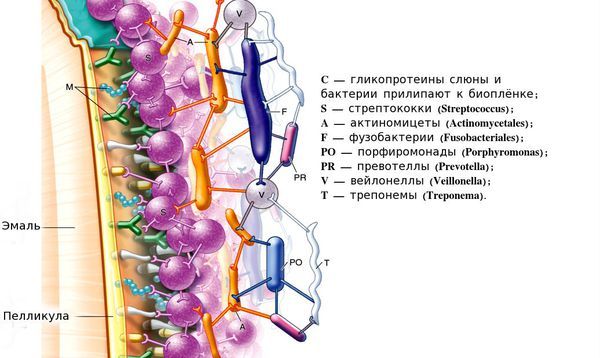
Зубная бляшка начинает формироваться уже через 1-2 ч после чистки зубов. Бляшкообра-зование начинается с взаимодействия кислых групп гликопротеинов слюны с ионами Са2+ зубной эмали, одновременно основные группы гликопротеинов реагируют с фосфатами гидрокси-апатитов. В результате на поверхности зуба образуется тонкая плёнка — пелликула, а присутствие микробов, особенно кислотообразующих, стимулирует её образование. Плёнка облегчает микробную колонизацию поверхности зуба и десневых карманов. Первыми там появляются стрептококки — S. sanguis и S. sativarius, а затем прочие представители аэробной и факультативно-анаэробной флоры. Жизнедеятельность микроорганизмов снижает окислительно-восстановительный потенциал, что создаёт условия для колонизации региона анаэробами— вейло-неллами, актиномицетами и фузобактериями.
При различных значениях рН микробный пейзаж зубных бляшек может значительно варьировать, в частности на верхних зубах преобладают аэробы и факультативные анаэробы (стрептококки и лактобаниллы), на нижних — анаэробы (вейлонеллы и фузобактерии). При образовании бляшек в межзубных щелях микробная колонизация протекает гораздо интенсивнее, но замены аэробных микроорганизмов анаэробами не происходит.
Значительное влияние на развитие зубных бляшек оказывает диета. При высоком содержании в ней углеводов происходит образование большого количества молочной кислоты в результате их ферментации стрептококками и лактобациллами. Молочную кислоту разлагают вейло-неллы, нейссерии и фузобактерии до уксусной, муравьиной, пропионовой и других органических кислот, что обусловливает резкий сдвиг рН среды в кислую сторону. Из углеводов микроорганизмы также могут образовывать различные полисахариды. Внутриклеточные полисахариды аккумулируются в виде запасных гранул. Их разложение также приводит к образованию различных органических кислот. Внеклеточные полисахариды частично утилизируются бактериями, например стрептококками, облегчают их адгезию к субстратам.
В процессе бляшкообразования происходит существенное изменение состава микрофлоры. В первой фазе длительностью 2-4 ч образуется так называемая «ранняя* зубная бляшка, в которой преобладают аэробные и факультативно-анаэробные бактерии — стрептококки, стафилококки, нейссерии и лактобактерии. Общее содержание бактерий не превышает 100-1000 в 1 г. Во второй фазе (4-5-е сутки) их сменяют анаэробные лептотрихии и фузобактерии. Общее содержание бактерий увеличивается до 1-10 млн в 1 г. В третьей фазе (6-7-е сутки и далее) микробиоценоз приобретает качественный окончательный состав, но в нём постоянно происходят количественные сдвиги. Резко снижается содержание аэробов и факультативных анаэробов (нейссерии, стрептококки) с преобладанием облигатных анаэробов (бактероиды, фузобактерии, вейлонеллы, актиномицеты, пептостреп-тококки). Последние выделяют комплекс токсических субстанций и ферментов (коллагеназа, проте-аза, гиалуронидаза и др.), повреждающие прилежащие ткани. Протеазы способны разрушать AT (IgA и IgG), что облегчает дальнейшую микробную колонизацию. Общее содержание бактерий достигает десятков и сотен миллиардов в 1 г. Зубные бляшки могут образовываться и на поверхности пломб; микробный состав бляшек зависит от характера и качества пломбировочного материала.
Согласно современным представлениям, важнейшую роль в возникновении и развитии кариеса играет инфекционный фактор. Кариесогенное действие микроорганизмов связывают с образованием ими зубной бляшки. По данным Bowden (1985), зубная бляшка содержит следующие виды микроорганизмов: факультативные стрептококки — 27 %, факультативные дифтероиды — 23 %, анаэробные дифтероиды — 18 %, пентостреп-тококки — 13 %, вейлонеллы — 6 %, бактероиды — 4 %, фузобактерии — 4 %, нейссерии — 3 %, вибрионы — 2 %. Из стрептококков преобладают Str. mutans, Str. sanguis, Str. mitis.
Установлено, что кариесогенные микробы избирательно накапливаются на поверхностях зубов, наиболее часто поражающихся кариесом (области фиссур и межзубные поверхности). Особено много Str. mutans у лиц, подверженных кариесу, и при множественном кариесе.
Зубная бляшка представляет собой структурированное образование, состоящее из микроорганизмов, расположенных на полисахаридной основе, плотно прикрепленное к поверхности зуба. В состав зубной бляшки, кроме микроорганизмов, входят лейкоциты, эпителиальные клетки, макрофаги. Она растет за счет постепенного наслоения новых бактерий. Кариесогенность зубной бляшки во многом зависит от степени ее накопления и давности.
В течение 1-2-х суток образования бляшки в ней преобладает Str. mutans, кариесогенность которого определяется выработкой им больших количеств молочной кислоты в присутствии углеводов. Это приводит к повышению проницаемости эмали, происходит кислотное растворение в наименее устойчивых участках эмали с последующим проникновением кислот в подповерхностный слой эмали и ее деминерализацией. Дальнейшее образование органических кислот на поверхности эмали усиливает процессы деминерализации, что приводит к образованию микрополостей в эмали, заполненных микроорганизмами и продуктами их метаболизма.
Определено, что чем выше скорость образования зубной бляшки, тем более выражено ее кариесогенное действие. У детей, имеющих повышенный индекс зубной бляшки, прирост интенсивности кариеса происходит в три раза быстрее, чем у детей с низким индексом. Помимо этого, кариес у детей развивается в тех случаях, если в микрофлоре зубной бляшки преобладает Str. mutans.
Однако на кариесогенность зубной бляшки влияют многочисленные факторы, в частности, микрофлора полости рта, количество употребляемых углеводов, количественный и качественный состав слюны, ее физико-химические свойства, содержание в ней минеральных компонентов: чем выше уровень кальция и фосфора, тем меньше кариесогенный потенциал бляшки.
В механизме влияния зубной бляшки на эмаль большая роль принадлежит ферментам микроорганизмов. Ферментативная деятельность этих бактерий приводит к повышенной проницаемости эмали. Известно также, что кариесогенные штаммы микроорганизмов зубной бляшки могут влиять на органическую фракцию эмали зуба. Их действие может особенно проявляться после растворения неорганической фазы эмали.
В то же время зубная бляшка на поверхности зуба механически изолирует подлежащую эмаль от воздействия слюны, являющейся немаловажным минерализующим и защитным фактором.
Определенное влияние на активность зубной бляшки оказывает фтор. Под действием фтора частично теряется способность микроорганизмов вырабатывать кислоту.
Зубная бляшка играет важную роль в развитии болезней пародонта. В возникновении воспалительного процесса в тканях пародонта участвуют микроорганизмы бляшки.
Характер влияния микроорганизмов зубной бляшки на пародонт разносторонний. Микробные ферменты способны повышать проницаемость капилляров, вызывать нарушение проницаемости эпителиальной мембраны и проникать в подэпителиальную соединительнотканную основу слизистой оболочки десны.
Конечно, на состояние зубной бляшки значительное влияние оказывают факторы окружающей среды. К ним относятся иммунобиологическая система жидкости десневой борозды, гидролитические ферменты секретов слюнных желез и ротовой жидкости, секреторные иммуноглобулины, бактериофаги, кислоты, углеводы. Эти биологические факторы находятся в сложном взаимодействии с микрофлорой полости рта и способны ослаблять или усиливать ее патогенный потенциал. Важную роль в поддержании биологического равновесия между бактериальным симбиозом и тканями полости рта играют общие факторы, регулирующие метаболизм тканей полости рта и от которых зависит соответствующая реакция на различные патологические воздействия.
Зубной камень образуется в результате отложения в зубном налете неорганических веществ: в коллоидной основе налета откладываются минеральные соли. При этом изменяется соотношение между микроорганизмами, спущенным эпителием, мукопротеидами и происходит импрегнация зубного налета кристаллами фосфата кальция. Обычно начало минерализации зубного налета происходит через 1-2 дня после его образования.
Механизм влияния зубного камня на пародонт разносторонний. Ввиду плотной консистенции зубной камень оказывает механическое давление, создает условия микротравмы эпителия десны и маргинальных волокон периодонта. Следует также учитывать химическое воздействие зубного камня на пародонт вследствие наличия в нем некоторых токсических элементов. Последние образуют в камне оксиды металлов (пентаксид ванадия, оксид свинца, меди, железа и др.).
Что такое зубной налет? Причины возникновения, диагностику и методы лечения разберем в статье доктора Сидихина Н. О., стоматолога со стажем в 11 лет.

Определение болезни. Причины заболевания
Зубной налёт — это мягкая, липкая биоплёнка, которая состоит из бактерий, продуктов их жизнедеятельности, слюны, остатков еды и тканевого детрита (разрушенных клеток). Налёт появляется на участках, на которых проще закрепиться:
- на шероховатых поверхностях зубов;
- в пришеечной области коронок;
- около пломб;
- в местах крепления зубных протезов;
- в промежутках между зубами;
- в естественных углублениях зуба;
- в труднодоступных для чистки местах;
- на негерметичных краях реставрации зубов;
- над и под десной;
- на мостах, брекетах, коронках.
Зубной налёт состоит из скоплений микроорганизмов, обитающих в полости рта: стрептококков, лактобактерий, стафилококков, нейссерий, вейлонелл, фузобактерий, актиномицетов и дрожжеподобных грибков. Микробы прикрепляются к пелликуле — тонкой плёнке на поверхности зубов. Уже через сутки их число увеличивается до сотен миллионов. А течение нескольких дней микроорганизмы объединяются и образуют бляшку, покрывающую зубную эмаль.
Чтобы сформировалась зубная бляшка, необходимо одновременное действие нескольких факторов:
- нехватка слюны, в том числе во время сна, её застой и повышение кислотности;
- количественный и видовой состав микрофлоры полости рта;
- присутствие углеводов;
- плохая гигиена полости рта.
Зубной налёт появляется при употреблении большого количества углеводов и неправильной или нерегулярной гигиене полости рта. Сахара, которые ест человек, употребляют и микробы, составляющие бляшку. Бактерии способны превращать углеводы в кислоту, которая разрушает зубную эмаль и способствует развитию кариеса [1] [4] [24] .
Симптомы зубного налета
Зубной налёт может проявляться следующими изменениями в полости рта:
- эмаль теряет блеск и приобретает тёмный оттенок;
- жизнедеятельность микроорганизмов вызывает неприятный запах изо рта;
- зубы на ощупь становятся шероховатыми;
- дёсны начинают кровоточить, особенно во время чистки зубов;
- пациенты, избегая кровоточивости, недостаточно хорошо чистят зубы, в результате количество налёта увеличивается;
- возникают покраснение и припухлость дёсен, боль при чистке и пережёвывании пищи;
- повышается чувствительность зубов к температурным или химическим раздражителям;
- усиливается подвижность зубов;
- образуется зубной камень;
- выделяется гной [1][5][18][26] .
Патогенез зубного налета
Через несколько минут после приёма пищи на зубах начинается формироваться плёнка — пелликула , которая состоит из гликопротеинов слюны. Пелликула плотно фиксирована на поверхности зуба, е ё невозможно смыть водой или слюной. Сама по себе плёнка ещё не содержит колоний бактерий и не приводит к кариесу. Патологический процесс начинается спустя несколько суток:
1. Через 48 часов количество микроорганизмов значительно увеличивается и образуется единая бактериальная сеть из более чем 750 различных видов бактерий.
2. На четвёртый — девятый день на зубной эмали формируется зрелая бляшка. Бактерии в её составе преобразуют сахара в кислоты, которые растворяют кальций и разрушают поверхность эмали.
3. Промежутки между призмами эмали увеличиваются. Микроорганизмы проникают в эти пространства и начинается образование кариеса.
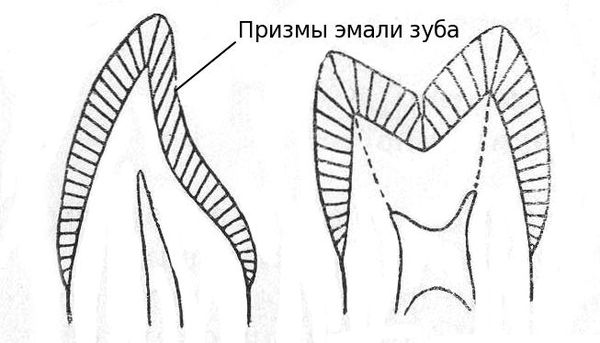
4. Зубная бляшка ограничивает доступ кислорода к поверхности эмали, что способствует размножению анаэробных бактерий (способных жить без кислорода). Сквозь бляшку из слюны не могут проникать и кальций с фосфором, поэтому если из-за плохой гигиены на поверхности зуба образовалась бляшка, то фторсодержащие пасты и эликсиры, даже самых лучшие и дорогостоящие, совершенно бесполезны.
Выраженные нарушения в биохимическом составе полости рта приводят к заболеваниям дёсен, зубов (и как следствие неприятному запаху изо рта) и даже осложнениям на внутренних органах, например на сердце. [1] [17] [21] [24] .
Классификация и стадии развития зубного налета
Зубные отложения подразделяют на минерализованные и неминерализованные:
1. Неминерализованные — это кутикула, пелликула, мягкий зубной налёт и зубная бляшка:
- Кутикула — это остатки оболочки, которая присутствовала на зубе в момент его прорезывания и исчезла после;
- Пелликула (приобретённая кутикула), с одной стороны, защищает эмаль от кислот, с другой — способствует прикреплению микроорганизмов к поверхности зуба;
- Мягкий зубной налёт — клейкие наслоения микроорганизмов, продуктов их жизнедеятельности, слюны, остатков еды и разрушенных клеток.
- Зубная бляшка — плотное образование из микробов и продуктов их жизнедеятельности, способное создать кислую среду и разрушить эмаль.
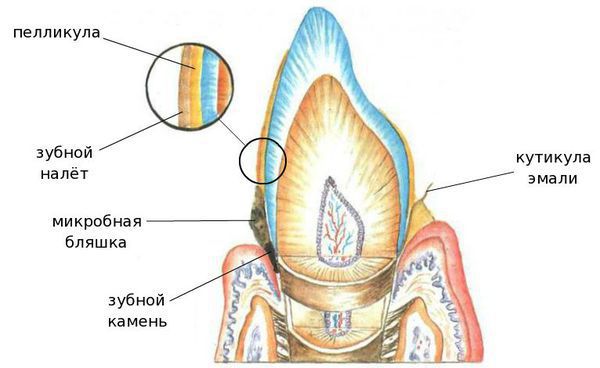
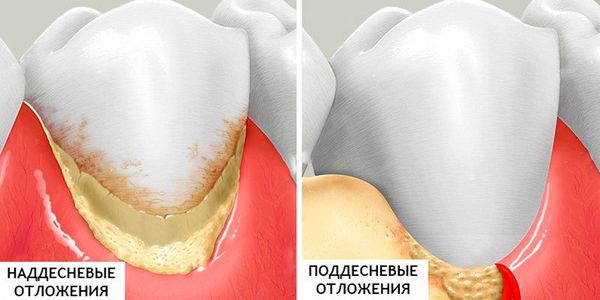
2. Минерализованные отложения — это наддесневой и поддесневой зубной камень (затвердевший налёт):
- Наддесневой зубной камень располагается на поверхности зубов наддесневого края. Чем светлее зубной камень, тем он плотнее и быстрее образуется. Зубной камень является отвердевшей зубной бляшкой. Расположен в основном в области открытия протоков больших слюнных желёз: на язычной поверхности нижних фронтальных зубов, в подъязычной области расположения протоков подъязычных и поднижнечелюстной слюнных желёз, на щёчной поверхности верхних моляров.
- Поддесневой камень расположен на поверхности корня зуба ниже уровня десны. Этот вид камня встречается у пациентов с различными заболеваниями пародонта ( тканей, окружающих и удерживающих зуб ).
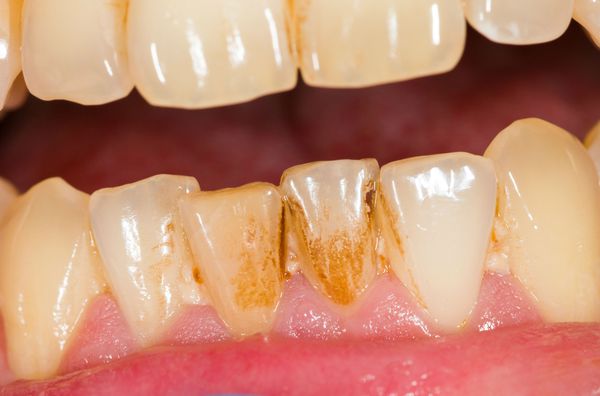
Зубной налёт различают по цвету:
- Липкая плёнка желтовато-белого оттенка — естественные отложения на поверхности зуба, которые появляются во время сна, после приёма пищи. При отсутствии гигиены полости рта возникает затхлый или гнилостный запах изо рта и кислый привкус. Приводит к появлению зубных камней, которые сможет убрать только стоматолог при помощи специальных инструментов.
- Пигментированный зубной налёт образуется при употреблении красящих продуктов: кофе, крепкого чая. Налёт у курильщиков окрашен в коричневый цвет, это вызвано отложением табачных смол и никотина.
- Тёмный зелёный налёт (налёт Пристли), как правило, образуется на молочных зубах и проходит с появлением постоянного прикуса. Выглядит как неровная тёмная кайма, может распределиться вдоль всего зуба или быть в виде пятнышек, и является источником неприятного запаха. Его образуют некоторые видов бактерий, обитающие в полости рта ребёнка. Возможны и другие причины возникновения пигментированного налёта — эндокринологические и желудочно-кишечные заболевания (нарушение обмена веществ, патологии щитовидной железы, гастрит, дуоденит, холецистит, воспаление поджелудочной железы, печени и желчевыводящих протоков), приём препаратов железа и иных витаминов; смена климата. В этих случаях оттенок налёта может быть чёрным, зелёным, коричневым или оранжевым. Налёт и бактерии, которые его образуют, не разрушают ткани зуба, но могут маскировать кариес [1][3][27] .
Осложнения зубного налета
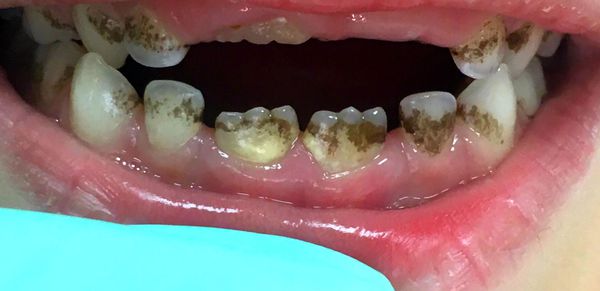
Если налёт не убирать, то он превращается в зубной камень и приводит к воспалению слизистой оболочки рта и дёсен. Отёчность десневого края способствует формированию ложных карманов и одновременно с этим усиливает выделение десневой жидкости. Это создаёт благоприятные условия для развития бактериальной микрофлоры, которая является ключевым фактором тяжёлых осложнений: кариеса, гингивита, пародонтита, стоматита, инфекционного эндокардита.
Кариес — это размягчение твёрдых тканей зуба кислотами, выделяемыми бактериями зубного налёта. Разрушению способствует частое употребление сахаров, высокая кислотность в полости рта, снижение слюноотделения [1] [4] [5] .
Гингивит — это воспаление дёсен, которое сопровождается покраснением, отёком, кровоточивостью и неприятным запахом изо рта. Плохая гигиена позволяет микробным бляшкам накапливаться между десной и зубами, что приводит к воспалению. При этом бороздки между зубами и десной увеличиваются и появляются десневые карманы. Они содержат бактерии, которые, помимо гингивита, могут вызывать кариес корня зуба и пародонтит. Чаще всего к гингивиту приводит зубной налёт. К второстепенным факторам относят: неправильный прикус, зубной камень, плохое восстановление зубов, сухость во рту, изменения гормонального фона, системные нарушения (сахарный диабет, СПИД, авитаминоз, лейкоз, лейкопения), приём лекарственных препаратов [14] [16] [24] .
Пародонтит — это воспалительное заболевание дёсен, при котором атрофируются ткани, в том числе костные, удерживающей зуб в лунке. Ведущую роль в развитии заболевания играют патогенные микроорганизмы зубного налёта. Продукты жизнедеятельности бактерий увеличивает проницаемость кровеносных сосудов, это приводит к иммунному ответу организма и хроническому воспалению.При пародонтите появляется кровоточивость, покраснение и отёк десны, её отхождение от корней зубов, в тяжёлых случаях — гнойное отделяемое из пародонтальных карманов. Также увеличивается подвижность зубов при жевании, а между зубами и десной начинают застревать остатки пищи. Пародонтит — необратимый процесс, так как сопровождается уже деструкцией тканей [18] [19] [26] [28] .
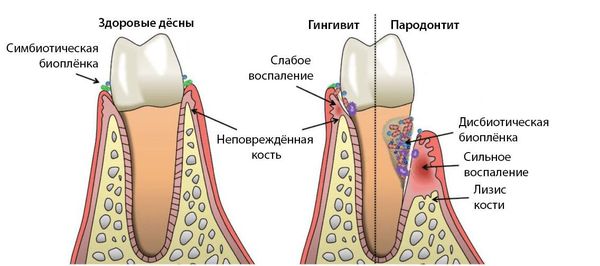
Стоматит — воспалительное заболевание полости рта с образованием язв и эрозией. К патологии приводят бактерии, которые поражают участки с микротравмами. В тяжёлых случаях на слизистой оболочке появляются пузыри, участки отмирания клеток (некроз). У лиц с ослабленным иммунитетом стоматит может стать причиной общей интоксикации [1] [27] .
Галитоз — дыхание с неприятным запахом, вызванное патологическим ростом микроорганизмов в пародонтальных карманах вокруг зубов. Галитоз может быть проявлением общих расстройств при метаболических нарушениях и поражении органов желудочно-кишечного и дыхательного тракта [29] [30] .
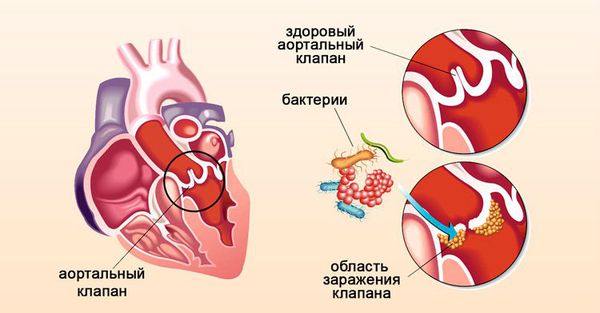
Инфекционный эндокардит — это воспаление внутренней оболочки сердца, которое сопровождается поражением клапанного аппарата и клеток сосудов условно-патогенными возбудителями (в большинстве случаев стрептококками и стафилококками). Бактерии из десневых карманов попадают в кровь, затем прилипают к клеткам сердца или сосуда (чаще уже повреждённого) и вызывают воспаление [6] [12] [25] [32] [32] .
Диагностика зубного налета
Зубной налёт определяется визуально во время осмотра. При этом стоматолог отмечает:
- уровень самостоятельной гигиены полости рта;
- прикус (расположение зубов, скученность);
- изменение формы, цвета, текстуры, поверхности, размеров слизистой полости рта;
- наличие и вид зубных отложений.
Здоровая десна имеет бледно-розовый оттенок, по рельефу похожа на апельсиновую корку. В норме контур десны плотно прилегает к зубу, сосочки полностью заполняют межзубные пространства, слизистая десневой границы легко определяется.
После осмотра стоматолог при помощи окрашивания специальными красителями выявляет количество зубных отложений и оценивает уровень гигиены: от хорошего до очень плохого. Для большинства пациентов достигнуть удовлетворительной гигиены полости рта — достаточно сложная задача.
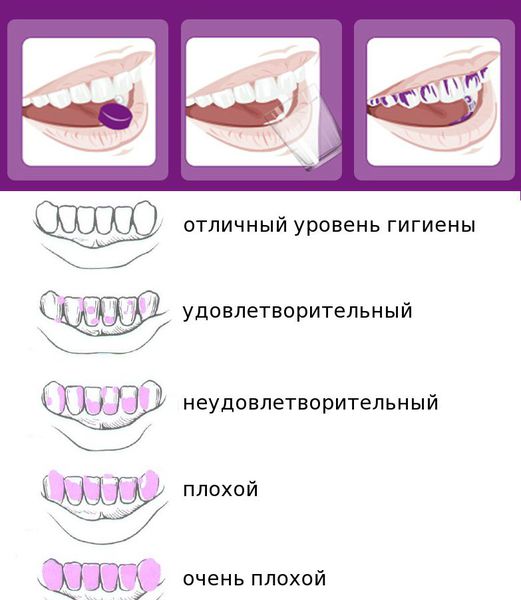
Реакция на воспаление со стороны мягких тканей оценивается по показателям:
- объём мягких тканей и глубина поддесневых карманов;
- интенсивность кровоточивости;
- подвижность зубов.
Воспалительную реакцию со стороны костей челюстей и убыль костной ткани определяют при помощи рентгенологического обследования [1] [7] [9] [27] .
Лечение зубного налета
После диагностики стоматолог удаляет бактериальный налёт. Для этого:
- полость рта обеззараживают антисептиками;
- поверхности зубов с помощью аппарата Air Flow под давлением обрабатывают специальным раствором;
- зубы полируют щёткой, резиновыми чашечками, пастой со фторидами, полировочной штрипсой (тонкой полоской из металла или пластика).
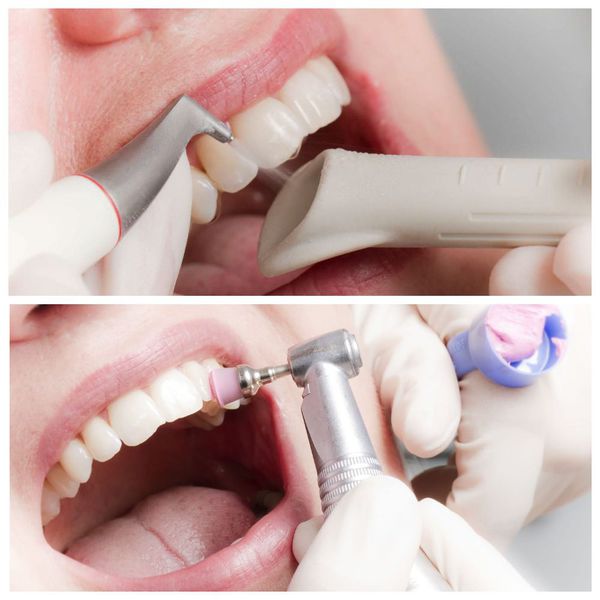
В завершении гигиены врач проводит антисептическую обработку, останавливает кровотечение и накладывает лечебные и антисептические повязки на десну. При выраженном воспалении слизистой назначается курс антимикробных аппликаций и заживляющих мазей. При обильных зубных отложениях рекомендован повторный осмотр [5] [12] [22] [25] .
Прогноз. Профилактика
При регулярном посещении стоматолога зубной налёт выявляют на начальной стадии и легко удаляют. Гигиеническую чистку зубов рекомендовано проводить раз в шесть месяцев. Если налёт не удалён, он переходит в плотное образование и развивается кариес. При своевременном обращении к врачу и правильном лечении прогноз будет благоприятным. При остром кариесе следует 2-4 раза в год посещать стоматолога, обрабатывать полость рта хлоргексидином, есть меньше углеводов и каждые 2-3 года контролировать микробиологические показатели слюны.
Профилактические осмотры, своевременное лечение, удаление зубного налёта существенно оздоравливают полость рта и предупреждают развитие заболеваний дёсен и зубов, однако без удовлетворительной самостоятельной гигиены добиться благоприятных долгосрочных результатов невозможно [7] [9] [15] .
Самое первое в гигиене и борьбе с налётом — это зубная щётка. Её подбирают индивидуально, согласно анатомическим особенностям пациентов. При выборе и использовании учитывают основные моменты:
- Предпочтительны щётки с искусственными щетинками с закруглёнными концами. Натуральную щетину, как правило, быстро колонизируют бактерии, к тому же она недолговечна, а острые концы щетинок могут травмировать десну и твёрдые ткани зуба.
- Охват щетины — не более двух-трёх зубов, это позволит чистить их лучше.
- Ручка удобно располагается в руке.
- Зубные щетки меняют каждые 6-10 недель.
Электрические щетки с вращающимися или колеблющимися головками рекомендованы пациентам с нарушенными мануальными навыками. Они хорошо удаляют налёт при постоянном использовании.
Помимо щётки, важную роль играет зубная паста. Она должна хорошо очищать, не повреждать эмаль, быть приятной на вкус, надолго защищать от микробов. Важное значение в её составе имеют следующие соединения:
- фториды (соединения фтора, например с натрием) — стабилизируют уровень минералов в зубной эмали;
- пирофосфат, хлорид цинка, цитрат цинка — уменьшают наддесневой зубной камень;
- хлорид стронция, гидроксиапатиты и нитрат калия — избавляют от повышенной чувствительности зубов;
- карбонат кальция — нейтрализует кислоты, тем самым защищая зубы [2][3][8] .
Для гигиены межзубных пространств будут полезны зубные нити(флоссы) и нити на держателе (флоссеты). Они легко проникают в межзубные промежутки и удаляют остатки пищи и налёт.
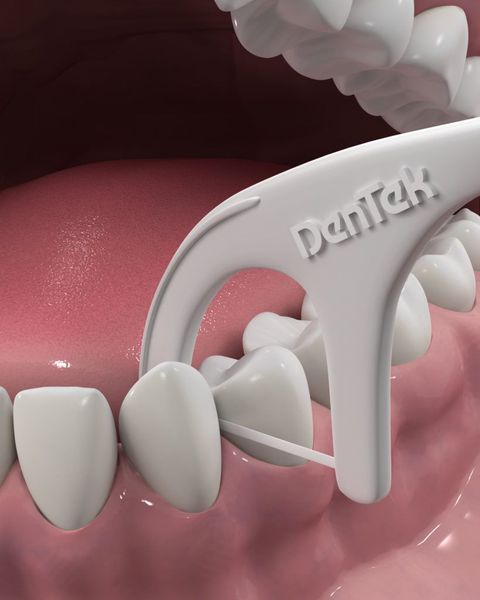
Пациентам с имплантами следует применять интерпроксимальные ёршики. Они состоят из спирально-изогнутого основания с конически или цилиндрически расположенными щетинками. Зубные нити и интерпроксимальные ёршики предназначены только для одноразового применения.
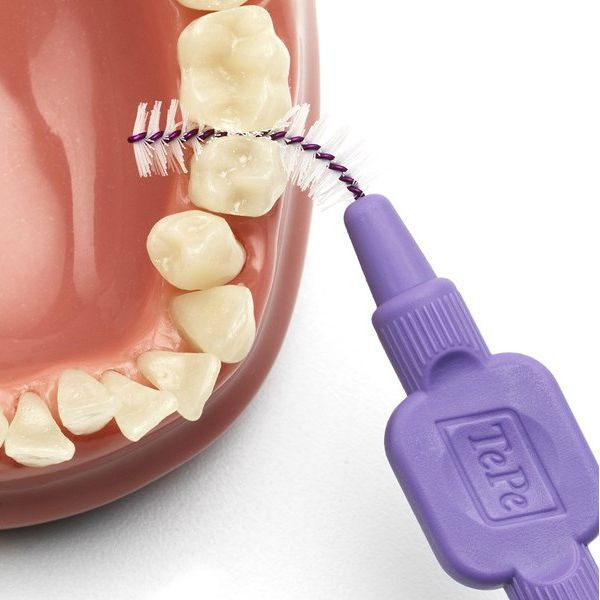
Для удаления остатков пищи можно применять деревянные или пластиковые зубочистки, но следует помнить, что они не избавят от налёта.
При наличии несъёмных конструкций (брекеты, коронки, импланты) полезен и незаменим ирригатор — прибор, который струёй воды под давлением очищает зубную поверхность и маcсирует мягкие ткани.
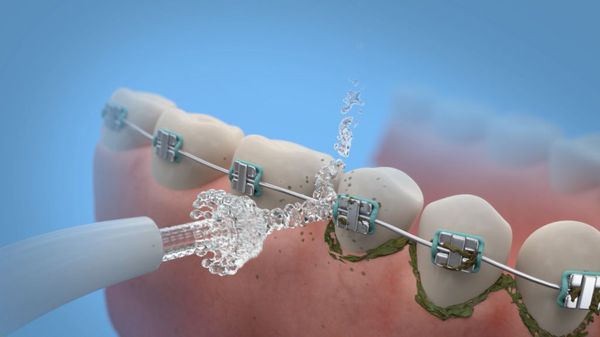
Ополаскиваетели для рта не являются самостоятельным средством для устранения зубных отложений, и удаляют налёт только в комплексе с другими средствами. При хронических заболеваниях пародонта полоскать рот не рекомендуется — это повышает риск попадания частичек инфицированных отложений в десневой карман и может усилить воспаление.
Хлоргексидин — это антисептик, который обладает антибактериальным действием и уменьшает зубные отложения. Но из-за побочного раздражающего действия (вплоть до химического ожога сосочков языка с нарушением вкусовой чувствительности) курс хлоргексидина в составе ополаскивателя ограничивают до двух недель, с повторением через три месяца.
Жевательная резинка в течение 15-20 минут после приема пищи механически очищает зубы за счёт повышения слюноотделения. Жевательные резинки следует выбирать без сахара, с ксилитом — сахарозаменителем, который препятствует размножению бактерий в полости рта.
Одним из важных факторов профилактики зубных отложений является питание. Для предотвращения кариеса важно получать из пищи достаточно минералов (кальция и фтора) и снижать количество сахара. Также следует исключить курение и уменьшить употребление красящих продуктов — чёрного кофе или чая [2] [3] [8] [10] .
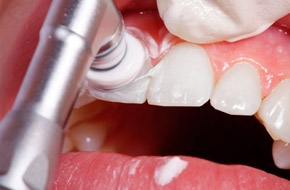
Профессиональная профилактика кариеса и гингивита, проводимая в условиях стоматологического кабинета врачом или гигиенистом, включает в себя выявление местных факторов, способных вызвать заболевание зубов и пародонта, профессиональное удаление зубных отложений, местное применение минерализующих препаратов и герметизацию слепых ямок и фиссур зубов.Выявление местных факторов, способствующих развитию основных стоматологических заболеваний, в условиях стоматологического кабинета ограничивается диагностикой зубных отложений, подсчетом индексов гигиены полости рта, определением содержания кариесогенной микрофлоры полости рта и свойств слюны с помощью стандартных наборов.
Профессиональное удаление зубных отложений включает инструментальное удаление зубной бляшки и зубного камня с последующей шлифовкой и полировкой поверхностей зубов и пломб.
Средства, применяющиеся при профессиональной гигиене полости рта:
- стоматологические или гигиенические наконечники,
- циркулярные щетки для стоматологического наконечника,
- ручные инструменты для удаления зубных отложений,
- ультразвуковые системы для удаления зубных отложений,
- воздушно-абразивные системы для удаления зубных отложений,
- химические средства для удаления зубных отложений,
- полировочные чашечки,
- пасты для удаления зубных отложений и полировки поверхностей зубов.
В целях насыщения зубов минеральными компонентами применяются:
- растворы для аппликаций и электрофореза,
- минералосодержащие лаки,
- гели с высоким содержанием фтора для врачебного использования.
Для герметизации слепых ямок и фиссур зубов применяются герметики различных класссов.
Средства для выявления факторов, способствующих развитию основных стоматологических заболеваний
Эта группа средств включает индикаторы для выявления зубных отложений и стандартные наборы и системы, позволяющие выявить степень риска развития стоматологических заболеваний у конкретного человека. Примером такой системы может быть система фирмы Vivadent (Schaan, Lichtenstein). Фирмой предлагается методика, позволяющая выявить бактерии Str. mutans с помощью теста Dentocult SM strip mutans. При стимуляции выделения слюны путем жевания парафиновых кубиков достигается смывание бактерий с поверхностей зубов. Пластмассовый шпатель вводится несколько раз под язык больного. В связи с выраженными адгезивными свойствами Str. mutans они прилипают к плотным поверхностям, в том числе к поверхностям зуба и протезов и, в частности, к шпателю. Шпатель затем вводится в питательную среду, в которую предварительно помещается таблетка антибиотика типа Bacitracin, задерживающего рост всех бактерий, кроме Str. mutans. Инкубируя флакон со шпателем в течение 2 дней при температуре 37 °С, выращивают колонии Str. mutans. Оценка плотности бактериальных колоний проводится с помощью образца (model chart). Выделяются 4 степени зараженности, выраженные в единицах колоний (КВЕ): класс 0 соответствует плотности колонии от 0 до 103, класс 1 — от 103 до 105, класс 2 — от 105 до 106, класс 3 — больше 106 КВЕ/млн. Набор содержит 10 реактивных штрипсов, 10 трубочек для субстрата, 10 бацитрациновых пластинок и 10 кусочков парафина.Поскольку в качестве индикатора высокого кариозного риска рассматривается существенное повышение количества лактобацилл, с середины 70-х годов фирмой предлагается тест Dentocult LB, позволяющий определить количество лактобацилл в слюне. С этой целью собирается стимулированная при жевании парафиновых кубиков слюна и высеивается на селективный агар. Флаконы с агаром инкубируются в течение 4 дней при температуре 37 °С. Плотность вырастающих колоний лактобацилл оценивается при сравнении с прилагаемым образцом (model chart) в единицах КВЕ (Kolonieenbildende Einheiten — единицы высеваемых колоний): I степень — до 103, II — 104, III — 105, IV — до 106 КВЕ. Выше 100 000 единиц колоний на 1 мл слюны оценивается как высокий риск поражения кариесом. Набор Dentocult LB содержит 10 носителей предметов и 10 кусочков парафина.С помощью теста Dentobuffstrip относительно простым путем определяется буферная емкость слюны и оценивается возможность буферной системы слюны нейтрализовать кислоту в полости рта. На тестовую полоску, импрегнированную кислотой, добавляется капля слюны. Через несколько минут цвет меняется в зависимости от буферной емкости: желто-коричневый свидетельствует о низком рН слюны (рН 4,5) и, соответственно, о недостаточной способности слюны нейтрализовать кислую среду. Зеленый оттенок соответствует рН=4,5 -5,5, синий цвет — рН=6. Набор содержит 10 реактивных штрипсов, 10 кусочков парафина и 10 пипеток.Аналогичная система DentoCheck предложена фирмой Butler.Полученные с помощью указанных тестов данные существенно помогают врачу оценить степень активности кариозного процесса и применить в каждом конкретном случае дифференцированно соответствующие меры, направленные на профилактику кариеса зубов.
Если вы нашли ошибку, пожалуйста, выделите фрагмент текста и удерживая ЛЕВЫЙ Ctrl, нажмите Enter. Вы можете отправить не более 5 сообщений за 30 минут!

Структура статьи
- Этиология
- Диагностика
- Клинические лабораторные исследования
- Маркеры формирования костной ткани
- Маркеры состояния обмена
- Маркеры резорбции костной ткани
- Прогностическая значимость
- Лабораторная программа : Метаболизм костной ткани
Этиология
Для остеопороза характерно снижение минеральной плотности с сопутствующими изменениями количества и микроархитектуры костной ткани, что сопровождается нарушением прочности скелета и повышением опасности переломов, особенно позвоночника, шейки бедра и запястья.
Масса костной ткани зависит от взаимодействия между клетками, формирующими (остеобласты) и разрушающими (остеокласты) кость. Индивидуальный пик костной массы, который в норме достигается к 25-30 годам, зависит от генетических и ненаследст-венных факторов: гормонального статуса, физических нагрузок, питания. Нарушение гор-монального статуса, несбалансированное питание, малоподвижный образ жизни, курение, чрезмерное потребление алкоголя являются факторами риска снижения костной массы Таким образом, остеопороз - гетерогенное заболевание, он может быть классифицирован как первичный или вторичный в соответствии с причинами, ответственными за потерю костной массы.
Диагностика
Начальный этап диагностики остеопороза – это выявление факторов риска на основе данных пациента:
- низкое содержание кальция в рационе;
- дефицит витамина D;
- заболевания ЖКТ (снижение всасываемости кальция);
- ранняя менопауза;
- длительные периоды иммобилизации
- длительный прием глюкокортикоидов, гормонов щитовидной железы;
- заболевания щитовидной железы, надпочечников, почек, печени;
- низкий индекс массы тела;
- вредные привычки (курение,алкоголь);
- низкая физическая активность.
Денситометрия - измерение плотности костной ткани, основано на измерение минерального компонента костной ткани – кальция.
В настоящее время для ранней диагностики остеопороза используют различные методы костной денситометрии, позволяющие выявить уже 2-5% потери массы кости, оценить динамику плотности костной ткани в процессе развития заболевания или эффективность лечения. Применяются изотопные методы (моно - и двухфотонная абсорбциометрия), рентгеновские (моно - и двухэнергетическая абсорбциометрия, количественная компьютерная томография ) и ультразвуковые. С помощью монофотонной, моноэнергетической и ультразвуковой денситометрии исследуют периферические отделы скелета. Эти методы наиболее подходят для скрининга остеопороза или предварительного диагноза. Наиболее универсальным является применение двухэнергетической рентгеновской абсорбциометрии (DEXA) – золотой стандарт, позволяющей измерять содержание костного минерала в любом участке скелета, а также определять содержание солей кальция, жира и мышечной массы во всем организме. Стандартными (автоматическими) программами для таких денситометров являются программы для поясничных позвонков, проксимальных отделов бедра, костей предплечья и программа "все тело".
Независимо от того, как рассматривать остеопороз – как заболевание или синдром, - риск переломов, определяемый при денситометрии, не может быть одинаковым для всех костей скелета. Поэтому выбор его участков для исследования является чрезвычайно важ-ным, Чтобы сделать этот выбор, необходимо помнить о том, что в костной ткани имеются два разных слоя. Компактное (кортикальное) вещество вносит основной вклад в прочность кости, но характеризуется невысокой скоростью метаболических процессов. Губчатое (трабекулярное) вещество, напротив, весьма активно в плане обмена веществ. Отмечено, что разные виды остеопороза по-разному сказываются на этих двух слоях.
При преимущественном поражение трабекулярного вещества – развивается постменопаузальный, гипогонадальный, стероидный остеопороз; кортикального вещества – сенильный, гипертиреодный, гиперпаратиреодный, диабетический остеопороз. При многих видах остеопороза наблюдается тенденция постепенного "распространения" остеопороза от осевого скелета (прежде всего позвонков), где появляются первые признаки остеопороза, к периферическому. Поэтому, учитывая чрезвычайную ценность ранней диагностики остеопороза, в целом следует отдать предпочтение исследованию осевого скелета. Исследование периферических отделов (большеберцовая, пяточные кости, фаланги пальцев) часто называют скриниговыми.
Клинические лабораторные исследования
В основе патогенеза развития остеопороза лежит дисбаланс процессов костного ремоделирования (костеообразования) и костной резорбции: либо преобладает ускоренная резорбция, либо сниженое костеообразование, либо замедление обеих составляющих костного обмена. В норме количество новообразованной ткани эквивалентно разрушенной.
Основная цель ранней биохимической диагностики остеопороза состоит в оценке интенсивности костного метаболизма. Для этого используются специальные биохимические маркеры, которые можно разделить на три группы.
Наибольшее значение в дифференциальной диагностике заболеваний скелета метаболического характера имеет оценка гормонального статуса больных, в частности парати-реоидного гормона (ПТГ), половых стероидных и гонадотропных гормонов, а также витамина Д, участвующего с ПТГ в регуляции обмена кальция. Определение концентрации кальция, фосфора и общей активности щелочной фосфатазы сыворотки крови использу-ются в оценке общего статуса больного и имеет вспомогательное, но не диагностическое значение.
Маркеры формирования костной ткани
Остеокальцин – основной неколлагеновый белок костного матрикса, который син-тезируется остеобластами. Синтез остеокальцина зависит от витамина К и Д, что до некоторой степени снижает чувствительность и специфичность определения остеокальцина, как маркера метаболизма костной ткани. Но, именно ,его концентрация в крови отражает метаболическую активность остеобластов костной ткани, поскольку остеокальцин крови – результат нового синтеза, а не освобождения его при резорбции кости. Он синтезируется остеобластами во внеклеточное пространство кости, часть попадает в кровоток, где он и может быть проанализирован. Высокий уровень ПТГ подавляет выработку белка остеобластами, в результате чего снижается его концентрация в костной ткани и в крови. По мнению многих авторов, этот показатель "возможный" прогностический индикатор усиления заболевания костей.
Кальцитонин – полипептидный гормон, выделяемый С-клетками щитовидной железы. Основной эффект кальцитонина – снижение уровня кальция в крови и отложение в кости. По своему действию является антагонистом паратгормона. Кальцитонин действует через специфические рецепторы (в костях, почках), в результате чего тормозится резорбция костей и выход кальция из кости.
Костный фермент щелочной фосфатазы (b ALP) Его исследование, наряду с общей активностью щелочной фосфотазы (ЩФ), существенно повышает информативность при дифференциальной диагностике заболеваний скелета и печени. Щелочная фосфотаза ассоциируется с активностью остеобластов и поэтому ее определение дополняет картину формирования костной ткани.
Маркеры состояния обмена
Паратгормон (ПТГ) – является одним из основных регуляторов кальциево-фосфорного обмена, синтезируется паращитовидными железами в ответ на уменьшение внеклеточной концентрации кальция. Он активирует резорбцию костной ткани и приводит к поступлению кальция и фосфора в кровь. Тиреотроопный гормон (ТТГ), наоборот, способствует усвоению кальция и препятствует его выводу из костной ткани. Между тем, уровень кальция в крови должен быть постоянным, если его мало, то риск развития сердечной патологии высок и регуляторная система нашего организма идет на все, чтобы содержание кальция в крови было нормальным, "забирая" его у скелета, мыщц.
Кальций, фосфор – основные минеральные компоненты костной ткани. Разные формы и стадии остеопороза могут проявляться различными сдвигами в концентрациях этих минералов. Другой аспект проблемы нарушения кальциевого гомеостаза – дефицит витамина Д. Хорошо известно, что с возрастом наблюдается прогрессирующее снижение кишечной абсорбции не только кальция, но и витамина Д, а также образование витамина Д в коже. В 2006 году группа экспертов Американского национального фонда по изучению остеопороза показала, что лечение препаратами кальция и витамина Д экономически эффективно и выгодно в целях профилактики остеопороза.
Маркеры резорбции костной ткани
Для оценки эффективности лечения остеопороза используют, как правило, маркеры резорбции, поскольку их снижение под влиянием терапии начинается уже через 2-3 недели и достигает плато через 3-6 месяцев (НИИ трансплантологии и искусственных органов МЗ РФ). Выявление нормального или значительно повышенного уровня маркера резорбции при однократном определении уже имеет диагностическое значение.
Деоксипиридинолин (ДПИД). На сегодняшний день ДПИД считают самым адекватным маркером резорбции кости. Костный коллаген характеризуется наличием поперечных связей между отдельными молекулами коллагена, которые играют большую роль в его стабилизации и представлены в виде деоксипиридинолина. Выход ДПИД в сосудистое русло из кости происходит в результате его разрушения остеокластами. ДПИД не подвергается дальнейшим метаболическим превращениям и выводится с мочой в неизменном виде. Его экскреция повышается при многих видах остеопороза.
beta-CrossLaps – (С-концевые телопептиды) образующиеся при деградации колагена 1 типа, который составляет более 90 % органического матрикса кости. Измерение beta-CrossLaps позволяет оценить темпы деградации относительно "старой" костной ткани. В норме малые фрагменты коллагена, образующиеся при его деградации, поступают в кровь и выводятся почками с мочой. У пациентов со сниженной функцией почек содержание beta-CrossLaps в сыворотке крови возрастает вследствие снижения экскреции. При патологическом увеличении резорбции костной ткани (пожилой возраст, остеопороз) коллаген 1 типа деградирует в большом объеме, что приводит к увеличению уровня фрагментов коллагена в крови.
В настоящее время все больше появляется данных о влиянии полиморфизмов генов на минеральную плотность костной ткани (МПКТ). Группой ученых из ГУ института ревматологии РАМН были получены данные о влиянии полиморфизма гена ВМР4 на ми-неральную плотность костной ткани и маркеры костного ремоделирования в группах женщин в постменопаузе, имеющих остеопороз.Обнаружена значимая ассоциация полиморфизма этого гена (6007С – Т полиморфизма 4 экзона) с МПКТ поясничного отдела и маркерами костного ремоделирования. При этом средний уровень щелочной фосфатазы был снижен, а значение уровня CrossLaps были высокими. Эти данные свидетельствуют о более низкой интенсивности процессов костеообразования и более высокой интенсивности процессов костной резорбции.
Изучение аллельного полиморфизма сети генов костного ремоделирования является перспективным направлением для выявления генотипов предрасположенности к остеопорозу.
Таким образом, определение уровня биохимических маркеров резорбции и ремоделирования кости позволяет:
- при профилактическом обследовании выявить пациентов с метаболическими нарушениями процессов ремоделирования и резорбции костной ткани;
- оценить и прогнозировать уровень потери костной массы;
- оценить эффективность проводимой терапии уже через 2-3 месяца
Прогностическая значимость
Высокие уровни маркеров резорбции костей, превышающие норму в 2 раза, связывают с двукратным увеличением риска переломов; пациенты с остеопорозом, имеющие уровни маркеров резорбции костей, превышающие нормы в 3 раза, имеют другую метаболическую костную патологию (включая злокачественную). Таким образом, показаниями для исследования маркеров метаболизма костной ткани являются:
- определение риска развития остеопороза;
- мониторинг в период мено - и постменопаузы;
- мониторинг при проведении гормональной заместительной терапии;
- оценка эффективности терапии антирезорбционными препаратами
Лабораторная программа: Метаболизм костной ткани
Маркеры формирования костной ткани
- Остеокальцин
- Щелочная фосфатаза
- Паратгормон (ПТГ)
- Неорганический фосфор
- Ионизированный кальций Маркеры резорбции костной ткани
- Деоксипиридинолин (ДПИД)
- CrossLaps – коллаген 1 типа
Читайте также:

