При хронических пародонтитах возрастает транссудация в слюну сывороточных
Опубликовано: 26.04.2024
Наиболее мощным фактором, способствующим развитию и поддержанию болезней пародонта, является развитие дисбиоза в полости рта, который развивается на фоне сниженного иммунитета, или сам приводит к его изменению. Дисбиотические изменения протекают часто на фоне вторичного иммунодефицита
Воспалительные поражения пародонта возникают в результате сложного взаимодействия бактериальной инфекции и ответной реакции организма. Системные факторы и факторы внешней среды, способствующие их развитию, могут влиять и на течение процессов. Для пародонтита характерен комплекс патологических изменений, в основе которых лежат неуклонно прогрессирующее и волнообразно текущее хроническое воспаление, распространяющееся из десны на нижние отделы пародонта, и связанные с ним деструктивные процессы. Таким образом, при пародонтите, как правило, обнаруживается картина сопутствующего ему гингивита, органично входящего в комплекс патологических изменений, характерных для развившихся форм воспалительных заболеваний пародонта.
Развитие хронического пародонтита сопровождается существенными изменениями состояния иммунных механизмов защиты ротовой полости, проявляющимися в местных изменениях состава клеток крови десны (в том числе количественного соотношения популяций и субпопуляций лимфоцитов), а также содержания в слюне иммуноглобулинов и цитокинов. Данные изменения варьируют в зависимости от степени повреждения пародонта и отражают процессы местного воспаления и активации иммунных механизмов защиты. Ингибирование иммунных реакций сопровождается хронизацией патологического процесса и потерей зубов, ведущую роль в патогенезе играет дисбаланс местных иммунных реакций.
Иммунологические исследования пациентов с тяжелыми формами генерализованного пародонтита показали, что в общем изолированный патологический процесс сопровождался существенными изменениями Т- и В-звеньев иммунитета. При хроническом генерализованном пародонтите в тканях пародонта развивается поликлональная активация В-лимфоцитов, что привлекает в зону поражения нейтрофильные лейкоциты. Последнее, в условиях активации В-лимфоцитов приводит к неадекватному ответу на присутствие патогенных микроорганизмов.
Снижение функциональной активности авангардной линии антимикробной защиты, представленной нейтрофильными гранулоцитами и макрофагами, способствует пролонгированию течения и хроиизации процесса.
Хронические воспалительные заболевания пародонта развиваются на фоне подавленных механизмов фагоцитарной защиты, при этом характер местной иммунной реакции в зависимости от степени тяжести процесса существенно не различается. У одного и того же пациента выраженность воспалительного процесса в пародонте может колебаться от катарального гингивита до легкой или тяжелой форм пародонтита.
Современные открытия в области расшифровки механизмов естественного и адаптивного иммунитета на наноуровне позволили изучить роль образ-распознающих рецепторов эпителиальных клеток (pattern recognition receptors), идентифицирующих молекулярный образ микроорганизмов, запускающих активацию про- и противовоспалительных цитокиновых каскадов. Так, у больных с хроническим генерализованным пародонтитом в десневой жидкости наблю-. дается- увеличение содержания как про-, так и противовоспалительных медиаторов с наличием признаков ПтД-девиации (снижение уровня INF-y и повышение уровня IL-4). В пародонтальном комплексе у этих пациентов отмечалось выраженное увеличение концентраций Ig классов G, М и А, что, по-видимому, является следствием локальной поликлональной активации В-лимфоцитов. В десневой жидкости больных с хроническим генерализованным пародонтитом установлено повышение уровня цитокинов RANKL, TNF-a, TL-1 и снижение концентрации OPG, ч то может быть причиной активации остеокластов и последующей деструкции костной ткани. В зоне пародонта при этом развивается «нетипичное» для хронического процесса воспаление, характеризующееся повышенным уровнем IL-8 и преобладанием количества нейтрофилов над численностью других форм лейкоцитов.
Опосредованное образ-распознающими рецепторами преодоление эпителиального барьера микробами с формированием хронического очага инфекции возможно при внедрении как патогенной, так и условно-патогенной нормальной микрофлоры, если развивается утрата местной толерантности к ней. Известно, что интактный пародонт представляет собой достаточно эффективный барьер для бактерий. Инвазии пародонтопатоге-нов препятствует соединительнотканный эпителий и комплекс иммунных факторов защиты. В тех случаях, когда общая масса бактерий или вирулентность некоторых их видов достигает определенного критического уровня, происходит их внедрение в ткани пародонта. Возможно, этому способствует травма пародонта, а также сбои в иммунной системе.
В процессе инвазии бактерии могут вырабатывать соединения, ингибирующие или полностью блокирующие активность защитных сил. Инвазия бактерий приводит к гибели тканей и образованию микроабсцессов. Гистологически, в коронковой части пародонтального кармана внедрившиеся бактерии окружены мощными инфильтратами плазматических клеток, защищающими нижележащие ткани от инфекции. Уничтожение бактерий, внедрившихся в клетки и ткани пародонта, осуществляется посредством клеток фагоцитарной и лимфоцито-макрофаговой систем. Эти системы сами по себе обладают большим деструктивным потенциалом и могут стать причиной нарушения тканей пародонта вследствие дегрануляции и выработки цитокинов.
Иммунный ответ организма на присутствие пародонтопатогенов основан на взаимодействии нескольких систем: слизисто-секреторной, нейтрофильной, гуморальной, комплементарной и иммунорегуляторной. Предполагают, что основным механизмом слизисто-секреторной системы защиты является препятствие прикреплению на поверхности клеток адгезивных элементов пародонтопатогенов. Микроорганизмы с более активной адгезивной системой, например, трепонемы, прикрепляются к поверхностной мембране эпителиальных клеток. Другие микробы, отторгнутые защитной системой, прикрепляются к трепонеме и продолжают колонизацию.
Бактерицидные свойства слюны предотвращает развитие патогенной микрофлоры зубного налета, ведущего этиологического фактора заболеваний пародонта. Доказательством участия слизистосекреторной системы в защите от инвазии пародонтопатогенов являются фактические данные об увеличении содержания секреторного иммуноглобулина А (slgA) в слюне у больных пародонтитом. Однако эти данные противоречивы. Так, Орехова Л.Ю. с соавт. (2001) обнаружили снижение уровня секреторного иммуноглобулина в ротовой жидкости при пародонтитах.
Барер Г.М., Лемецкая Т.И. (1996) выявили повышенный уровень иммуноглобулинов основных классов вследствие их местного синтеза в воспаленной десне, а также транссудации из пораженных тканей с последующим поступлением десневой жидкости в смешанную слюну. В крови больных с данной‘Патологией снижается концентрация Ig А, М, G. По данным А.А. Кунина с соавт. (2001) при хроническом генерализованном пародонтите в стадии обострения содержание в ротовой жидкости Ig А, Е, G и лизоцима повышено, в то же время содержание slgA понижено, появляются следы Ig М. В десневой жидкости значительно увеличено количество макрофагов, нейтрофилов, лимфоцитов и эпителиоцитов. При этом в три раза снижена функциональная активность Т-лимфоцитов капиллярной крови десны.
Таким образом, хронический гингивит и пародонтит представляют собой многокомпонентные процессы, ключевыми из которых, с одной стороны, являются воспалительно-инфильтративные и деструктивные, а с другой стороны — компенсаторные. Ремиссия, которая наступает самостоятельно либо достигается проведением эффективного лечения, есть результат мобилизации и компенсаторной перестройки тканевых систем пародонта с их выведением на новый уровень гомеостаза. Наиболее мощным фактором, способствующим развитию и поддержанию болезней пародонта, является развитие дисбиоза в полости рта, который развивается или на фоне сниженного иммунитета, или сам приводит к его изменению.
Существует также механическая теория, которая позволяет по-новому взглянуть на патогенез воспалительного процесса в тканях пародонта. Весьма существенными явились результаты изучения изменений в системе иммунитета при длительной гиподинамии. Было обнаружено снижение способности лимфоцитов к активации и пролиферации, что повышает степень риска развития инфекционного процесса. Хорошо известно, что в полости рта лимфоциты относят к факторам местной защиты. Они мигрируют из лимфоидной ткани глоточного кольца и крови, через стенки микрососудов, обильно кровоснабжающих ткани десны. При длительной гипокинезии количество функционирующих микрососудов значительно уменьшается. Для тканей пародонта очень важно, что уменьшение кровоснабжения снижает уровень миграции клеток крови в десневую и ротовую жидкости. Это-касается также и сывороточных иммуноглобулинов, и компонентов комплементов, являющихся гуморальными факторами местной защиты тканей полости рта.
Можно представить, что снижение активности лимфоцитов влечет за собой уменьшение продуцирования секреторного иммуноглобулина IgA плазматическими клетками, образующимися из местных В-лимфоцитов в слизистой оболочке десны. Снижение же способности лимфоцитов к пролиферации, ведет к уменьшению связанных с ними иммуноглобулинов, что в свою очередь ослабляет защитные реакции в тканях пародонта. Становится понятным, что именно снижением активности лимфоцитов по причине регионарной гиподинамии и гипокинезии можно объяснить тот факт, что защитная реакция в пародонте начинается не с активации лимфоцитов антигенами микробов зубной бляшки, а с нейтрофильного хемотаксиса — увеличения числа нейтрофилов в зубодесневой борозде.
Для понимания механизмов развития деструктивных процессов в пародонте чрезвычайно важным явилось обнаружение при изучении иммунной системы в условиях гипокинезии достоверного увеличения продукции лимфоцитами остеокластактивирующего фактора, который вызывает потерю Са костной тканью. Совершенно очевидно также, что снижение интенсивности жевательной функции сопровождается снижением уровня саливации, что в свою очередь, ослабляет естественную резистентность тканей полости рта (в частности за счет таких факторов, как лизоцим, муцин и пр.). С уменьшением, саливации страдает и такой путь, снижения количества микроорганизмов в полости рта, как смыв их ротовой жидкостью.
Все вместе взятое благоприятствует микробной агрессии в полости рта и развитию воспаления в тканях пародонта, которые имеют наибольший контакт со скоплением микробов в зубной бляшке. Для развития воспаления в пародонте не менее важным является то, что гиподинамия способствует нарастанию устойчивости патогенных микробов к антибиотикам и возникновению аутоинфекции, а также сенсибилизации аллергенами аутомикрофлоры. Последнее, как установлено, вызывает потерю костной ткани в пародонте.
Благодаря изучению проблем гипокинезии и гиподинамии, стало очевидным, что малоподвижный образ жизни, который ведет человек в нашем столетии, отрицательно сказывается на состоянии его иммунной системы и сопротивляемости микробным инфекциям. Следует полагать, что это усугубляет последствия снижения факторов местной защиты полости рта, связанные с регионарной гиподинамией и гипокинезией (гипофункцией) в жевательной системе. Дополнением к этому являются многочисленные соматические заболевания, которые еще больше ослабляют иммунные силы организма и приводят в своем патогенезе к убыли костной ткани.
Таким образом, хронические очаги инфекции в полости рта вносят существенный вклад в развитие иммунологических дисбалансов, постоянно отвлекая на себя иммунологические ресурсы организма и истощая общий потенциал противоинфекционной защиты, что множит число вновь возникающих инфекционных очагов и хронизирует их. С другой стороны, полость рта у этих больных становится постоянно существующим источником распространения инфекции в нижележащие органы, а также лимфогенно и гематогенно по всему организму. Персистирующий антигенный инфекционный стимул неизбежно обусловливает аллергическую сенсибилизацию организма, что еще более грубо нарушает равновесие иммунной системы»больных, оказывая на нее угнетающее и дезорганизующее влияние.

Приглашаем подписаться на наш канал в Яндекс Дзен
Актуальность. При генерализованном воспалительно-деструктивном процессе в пародонте отмечаются глубокие нарушения гомеостаза полости рта. Несомненную роль в патогенезе заболеваний пародонта играют процессы образования минерализованных над- и поддесневых назубных отложений [14, 20]. Считается [6], что влияние «зубной» бляшки и «зубного» камня не следует рассматривать только как местный фактор, поскольку их образование и активность зависят от состояния реактивности организма (изменение минерального и белкового состава слюны, десневой жидкости, их ферментативной активности).
Более высокая концентрация неорганического фосфата в смешанной слюне больных с воспалительными заболеваниями пародонта также создает условия для камнеобразования [12, 16, 17]. Весьма интересным является установленное сходство химического состава слюнных и мочевых фосфатных камней, что позволяет рассматривать сиало- и нефролитиаз как единый процесс патогенного минералообразования в организме человека [13, 15].
Интерес к изучению минеральных составляющих организма, его биологических жидкостей и тканей [8], возрос в последние годы со стороны представителей различных специальностей. Из 14 жидкостей организма только в трех (слюна, желчь, моча) могут образовываться камни [4, 5], т. е. камни в организме человека формируются в органах, активно участвующих в поддержании гомеостаза, водно-электролитном и кислотно-щелочном равновесии.
В процессах камнеобразования в почках и слюнных железах много общего. Установлено, во-первых, что усиление секреторной деятельности слюнных желез вызывает угнетение водо- и солевыделительной функции почек. Во-вторых, извитые канальцы почки, как и слюнные трубки, участвуя в солевом обмене организма, очень сходны по строению и функции. В-третьих, клиницистам известны примеры тесных взаимоотношений слюнных желез с мочеполовой системой человека [1].
Из 14 жидкостей организма только в трех (слюна, желчь, моча) могут образовываться камни
Мочекаменная болезнь — наиболее распространенная болезнь мочевой системы. Длительно протекающий нефролитиаз сопровождается стойким нарушением минерального обмена в организме [11]. Показано [3], что причинами образования камней являются нарушение минерального обмена веществ (в основном фосфорно-кальциевого).
Наличие анатомо-физиологической и функциональной взаимосвязи моче- и желчевыводящих путей считается доказанным. Желчнокаменная болезнь является распространенным (не менее чем у 10—15 % взрослого населения) заболеванием, развивающимся в любом возрасте. Если принять во внимание сведения об этиологии и патогенезе желчно- и мочекаменной болезней, то нельзя не заметить некоторого сходства в трактовке механизмов камнеобразования у больных и со слюнно-каменной болезнью [2, 7, 18]. Таким образом, актуальность проблемы множественных заболеваний в организме человека не вызывает сомнений.
Цель исследования
Определить параметры ротовой жидкости больных хроническим генерализованным пародонтитом (ХГП) при наличии патогенного минералообразования и без него.
Материал и методы
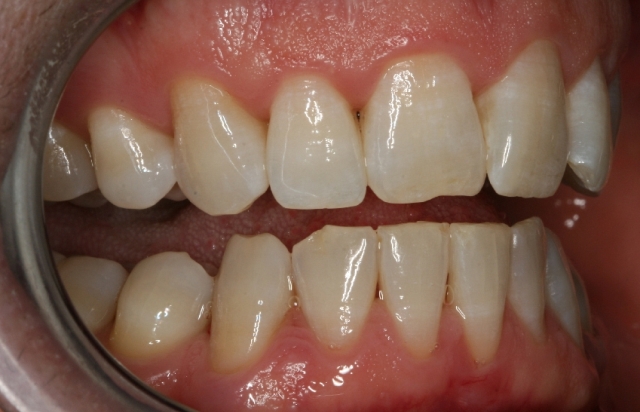
Исследовали ротовую жидкость 34 больных ХГП средней степени тяжести. Основную группу составили 24 пациента ХГП (рис. 1), ассоциированного с желчно-, моче- или слюнно-каменной болезнью, контрольную — 10 пациентов ХГП без указанной соматической патологии (без патогенного минералообразования).
Рис. 1. Минерализованные отложения у больного ХГП средней степени тяжести, ассоциированным с мочекаменной болезнью.
Ротовую жидкость собирали утром натощак или через 1—3 часа после приема пищи по 2 мл путем сплевывания в пробирку. Полученный образец центрифугировали при скорости 13 000 об./мин. в течение 6—10 мин. Надосадочную жидкость аспирировали и определяли в ней pH и электролиты (К+, Na+, Ca2+, HCO3-).
Исследования проводили на аппарате RADIOMETER ABL 80 FLEX (Дания) в биохимической лаборатории Смоленской областной клинической больницы (зав. Л. Н. Чемодурова). Количественные показатели результатов исследования рассчитывались автоматически. Полученная информация выдавалась в печатном варианте.
Результаты исследования и их обсуждение
Анализируя полученные данные (табл. № 1), следует отметить, что уровень ионизированного кальция в ротовой жидкости у больных ХГП средней степени тяжести с патогенным минералообразованием оказался достоверно ниже, чем у лиц с ХГП без патогенного минералообразования.
Таблица № 1. Биохимические показатели ротовой жидкости у больных ХГП с патогенным минералообразованием (пм) и без него (бпм).
Хронический пародонтит – это длительно текущий, инфекционно-индуцированный патологический процесс, затрагивающий все структуры пародонта и приводящий к деструкции его тканей и резорбции альвеолы. Хронический пародонтит сопровождается зудом и кровоточивостью десен, наличием над- и поддесневых зубных отложений и пародонтальных карманов, галитозом, подвижностью и смещением зубов, эндогенной интоксикацией. Диагностические мероприятия при хроническом пародонтите включают анализ данных пародонтограммы, ортопантомограммы, биопсии тканей десны. Лечение хронического пародонтита зависит от степени выраженности и включает снятие зубных отложений, местную противовоспалительную терапию, физиотерапию, шинирование зубов; при необходимости – удаление подвижных зубов, лоскутные операции.
МКБ-10
- Причины
- Местные факторы
- Общие факторы
- Классификация
- Симптомы хронического пародонтита
- Диагностика
- Лечение хронического пародонтита
- Легкая степень
- Средняя степень
- Тяжелая степень
- Прогноз и профилактика
- Цены на лечение
Общие сведения
Хронический пародонтит – воспалительное заболевание пародонтального комплекса, имеющее циклическое, неуклонно прогрессирующее течение. Согласно статистике, та или иная форма пародонтита выявляется у 90-95% населения. В зоне риска развития хронического пародонтита находятся преимущественно лица старше 30-40 лет. По данным ВОЗ, потеря зубов вследствие хронического пародонтита наблюдается в 5 раз чаще, чем по причине кариеса. Клиническая значимость хронического пародонтита не ограничивается рамками стоматологии, поскольку состояние пародонта тесно связано с эндокринными, сердечно-сосудистыми заболеваниями, болезнями крови.

Причины
Местные факторы
Хронический пародонтит обусловлен целым рядом местных и общих предпосылок. Главным местным этиологическим фактором выступает пародонтопатогенная микрофлора (превотеллы, актиномицеты, порфиромонады, бактероиды, пептострептококки и др.), в большом количестве присутствующая в зубном налете. Микроорганизмы и их токсины повреждают эпителий десны, вызывая его воспалительную реакцию в форме хронического катарального или гипертрофического гингивита.
В дальнейшем, проникая в зубодесневую бороздку, патогены способствуют ее углублению и образованию зубодесневых карманов. Агрессивное действие над- и поддесневого налета, содержащего колонии бактерий, заключается в постепенном разрушении подлежащей соединительной ткани, включая периодонтальную связку, образующую зубодесневое соединение. Кроме микробного фактора, в развитии хронического пародонтита большую роль играют стоматологические заболевания:
- кариес;
- зубной камень;
- травмы зуба;
- неправильный прикус;
- бруксизм;
- тяжи слизистой оболочки и пр.
Пусковым моментом может выступать хроническая травматизация тканей пародонта неправильно поставленными пломбами или плохо подогнанными зубными протезами.
Общие факторы
Среди общих факторов, способствующих развитию хронического пародонтита, велика роль эндокринопатий (сахарного диабета, остеопороза, ожирения), патологии ЖКТ (гастрита, холецистита, энтероколита, гепатита), аллергических и аутоиммунных заболеваний, болезней системы крови, гиповитаминозов, лучевых поражений и пр.
Классификация
Учитывая распространенность воспалительно-дистрофического процесса, в пародонтологии выделяют локализованный (очаговый) и генерализованный (диффузный) хронический пародонтит. В клиническом течении хронического пародонтита чередуются фазы обострения и ремиссии. В зависимости от выраженности патологических изменений в пародонте выделяют начальную стадию и стадию развившихся нарушений, которая включает 3 степени тяжести хронического пародонтита.
- Начальная стадия хронического пародонтита характеризуется разволокнением компактной пластинки, наличием признаков остеопороза, снижением высоты межзубных перегородок не более чем на 1/4 длины корня зуба. Пародонтальные карманы имеют глубину не более 2,5 мм.
- Легкая степень хронического пародонтита диагностируется при глубине пародонтальных карманов от 2,5 до 3,5 мм; убыли альвеолярной кости не более чем на 1/3 длины корня зуба; незначительной подвижности зубов.
- Средне-тяжелая степень хронического пародонтита характеризуется глубиной пародонтальных карманов от 3,5 до 5 мм; резорбцией альвеолярной кости на половину длины корня зуба; патологической подвижностью зубов I-II степени.
- Тяжелая степень хронического пародонтита определяется при глубине пародонтальных карманов свыше 5 мм; убыли альвеолярной кости более половины длины корня зуба и патологической подвижности зубов II-III степени. В особо запущенных случаях происходит полная резорбция костной ткани, гибель связочного аппарата и выпадение зуба из своего ложа.
Симптомы хронического пародонтита
В начальном периоде хронического пародонтита пациенты ощущают зуд и пульсацию в деснах, дискомфорт при пережевывании пищи. Десны рыхлые, отечные, кровоточат при чистке зубов. Отмечается застревание пищи в межзубных промежутках, появление неприятного запаха изо рта. При стоматологическом обследовании выявляются признаки катарального гингивита, наличие зубных отложений и неглубоких зубодесневых карманов в межзубной области. Зубы сохраняют свою неподвижность.
Легкая степень хронического пародонтита характеризуется прогрессированием патологических изменений. Усиливается болезненность и кровоточивость десен, галитоз. В полости рта быстро и в больших количествах скапливается мягкий зубной налет, образуется зубной камень. При осмотре выявляются признаки хронического катарального или гипертрофического гингивита, зубодесневые карманы с отделяемым серозно-гнойного характера, расшатывание зубов.
При хроническом пародонтите средне-тяжелой степени ко всем вышеназванным симптомам присоединяются оголение и повышенная чувствительность шеек зубов к температурным и химическим воздействиям. Вследствие выраженного гипертрофического гингивита десны теряют свою обычную конфигурацию и цвет; зубодесневые карманы глубокие, с серозно-гнойным отделяемым. В период обострения развивается альвеолярная пиорея – выделение гнойного экссудата из пародонтальных карманов. Зубы подвижны, между ними образуются диастемы и тремы.
Хронический пародонтит тяжелой степени протекает с выраженной симптоматикой (кровоточивостью десен, подвижностью и смещением зубов, галитозом, обильными зубными отложениями, диффузным гингивитом и пр. Выраженная боль в деснах затрудняет жевание и чистку зубов. Отмечается выпадение отдельных зубов (частичная адентия).
Обострения хронического пародонтита сопровождаются эндогенной интоксикацией - недомоганием, повышением температуры тела, увеличением регионарных лимфоузлов. Десна становится отечной и резко болезненной; из зубодесневых карманов выделяется гной, образуются свищи и абсцессы, усиливается подвижность зубов.
Диагностика
Диагностика и лечение хронического пародонтита проводится стоматологом-пародонтологом. При необходимости к диагностике сопутствующих заболеваний могут быть подключены эндокринолог, гастроэнтеролог, кардиолог, гематолог, аллерголог, ревматолог. Проводится:
- Стоматологический осмотр. Во время осмотра оценивается выраженность изменений: определяются гигиенические и пародонтальные индексы, производится измерение глубины пародонтальных карманов, проводятся функциональные пробы (проба Шиллера-Писарева), составляется пародонтограмма и др.
- Рентген. Степень выраженности хронического пародонтита определяется на основании данных прицельной рентгенографии и ортопантомографии.
- Лабораторная диагностика. С целью определения микробной обсемененности зубодесневых карманов проводится ПЦР-соскоб, бактериологический посев на питательные среды. Для подтверждения эндогенного происхождения хронического пародонтита рекомендуется исследование крови на сахар, определение иммуноглобулинов, содержания СРБ.
На основании данных биопсии десны хронический пародонтит дифференцируют с гингивитом и пародонтозом.
Лечение хронического пародонтита
Объем и характер лечебных мероприятий значительно варьируется в зависимости от степени выраженности хронического пародонтита. Перед началом лечения хронического пародонтита проводится снятие зубных отложений, в дальнейшем пациенту даются практические рекомендации по соблюдению эффективной гигиены полости рта.
Легкая степень
При начальной и легкой форме лечение хронического пародонтита осуществляется консервативными методами, включающими:
- антисептическую обработку слизистой оболочки полости рта (перекисью водорода, хлоргексидином, фурацилином);
- пародонтологические аппликации противовоспалительных средств;
- физиотерапевтические процедуры (электрофорез, ультрафонофорез, дарсонвализацию, лазеротерапию, озонотерапию, массаж десен).
Средняя степень
Лечение хронического пародонтита средне-тяжелой степени предполагает дополнительное проведение закрытого и открытого кюретажа зубодесневых карманов, склерозирующей терапии. Целесообразно назначение внутрь антибактериальных препаратов. Также может потребоваться избирательное пришлифовывание и лечебное шинирование подвижных зубов.
Тяжелая степень
Лечебная тактика в отношении хронического пародонтита тяжелой степени требует сочетания методов терапевтической и хирургической пародонтологии. В этом случае, кроме местной и системной противовоспалительной терапии, по показаниям производится:
- удаление зубов с патологической подвижностью;
- гингивэктомия;
- лоскутные операции (в т. ч. с остеопластикой);
- вскрытие пародонтальных абсцессов и т. п.
Больные с тяжелым хроническим пародонтитом нуждаются в консультации стоматолога-ортопеда для планирования ортопедическое лечения – протезирования конструкциями с шинируюшими элементами.
Прогноз и профилактика
Правильно проведенное комплексное лечение хронического пародонтита и дальнейшее соблюдение рекомендаций стоматолога позволяет восстановить функцию зубочелюстной системы на длительный срок. Легкие и средние степени хронического пародонтита, как правило, не приводят к потере зубов; при тяжелом течении имеется высокий риск развития вторичной адентии.
Профилактика хронического пародонтита заключается в устранении местных и общих провоцирующих факторов (снятии зубных отложений, лечении кариеса, замене некачественных протезов, исправлении прикуса, лечении сопутствующих заболеваний, отказе от вредных привычек и пр.). Пациенты с хроническим пародонтитом нуждаются в диспансерном наблюдении, периодической профессиональной гигиене полости рта и проведении поддерживающей терапии.
- Издательство «Медиа Сфера»
- Об издательстве
- Рекламодателям
- Доставка / Оплата
- Контакты
Кафедра госпитальной терапевтической стоматологии, пародонтологии и гериатрической стоматологии Московского государственного медико-стоматологического университета
ГБОУ ВПО «Московский государственный медико-стоматологический университет им. А.И. Евдокимова» Минздрава России, Российская Федерация
ГБОУ ВПО «Московский государственный медико-стоматологический университет им. А.И. Евдокимова» Минздрава России, Российская Федерация
Изменение биохимических показателей ротовой жидкости при комплексном лечении хронического генерализованного пародонтита средней степени тяжести
Журнал: Российская стоматология. 2015;8(1): 42-43
Пашковская А. Э., Аракелян И. Р., Сувкова Е. И. Изменение биохимических показателей ротовой жидкости при комплексном лечении хронического генерализованного пародонтита средней степени тяжести. Российская стоматология. 2015;8(1):42-43.
Кафедра госпитальной терапевтической стоматологии, пародонтологии и гериатрической стоматологии Московского государственного медико-стоматологического университета





Кафедра госпитальной терапевтической стоматологии, пародонтологии и гериатрической стоматологии Московского государственного медико-стоматологического университета
ГБОУ ВПО «Московский государственный медико-стоматологический университет им. А.И. Евдокимова» Минздрава России, Российская Федерация
ГБОУ ВПО «Московский государственный медико-стоматологический университет им. А.И. Евдокимова» Минздрава России, Российская Федерация
Ведущую роль в развитии воспалительных заболеваний пародонта играет микробная флора зубных отложений, особенно штаммы пародонтопатогенных анаэроб, что требует применения противомикробных средств широкого спектра и нередко приводит к развитию резистентности, дисбактериоза или аллергической реакции. Несмотря на внедрение в медицинскую практику современных методов диагностики и лечения, остается актуальным поиск эффективных и безопасных лекарственных препаратов для лечения воспалительных заболеваний тканей пародонта.
Антигомотоксический препарат траумель С широко применяется в медицине, а в частности — в стоматологической практике.
Препарат оказывает влияние на все звенья воспалительного процесса, стимулирует процессы регенерации и защитных реакций организма.
При анализе литературы отсутствуют данные, определяющие терапевтическую эффективность использования препарата в комплексном лечении хронического генерализованного пародонтита средней степени тяжести на основании биохимических показателей ротовой жидкости, что явилось целою исследования.
Материал и методы. Обследованы 78 пациентов, в том числе 63 пациента, страдающих хроническим генерализованным пародонтитом средней степени тяжести, и 15 пациентов с клинически здоровым пародонтом. Включенные в исследование пациенты не имели других соматических патологий. Возраст обследуемых составлял от 30 до 65 лет.
Пациенты были разделены на 4 группы в зависимости от методики применения препарата:
— 1-я (контрольная) группа — пациенты с клинически здоровым состоянием пародонта;
— 2-я — группа сравнения. Комплексное лечение без применения препарата;
— 3-я группа — комплексное лечение с применением препарата в инъекционной форме;
— 4-я группа — комплексное лечение с применением препарата в инъекционной и таблетированной формах.
Для контроля эффективности лечения совместно с клиническими методами обследования использовали дополнительные: определение биохимических показателей ротовой жидкости (аспартатаминотрансферазы и аланинаминотрансферазы, щелочной фосфатазы и общего белка).
Всем пациентам, участвующим в исследовании, проводилось пародонтологическое лечение: все этапы профессиональной гигиены, лечение кариеса и его осложнений. При хорошем уровне гигиены проводили хирургическое лечение, которое заключалось в операции «открытый» кюретаж. На этапе хирургического лечения применялся антигомотоксический препарат траумель С.
Результаты. Фермент щелочная фосфатаза является показателем фосфорно-кальциевого обмена и играет ведущую роль в создании минеральной структуры костей организма.
При воспалительных процессах в полости рта активность щелочной фосфатазы ротовой жидкости коррелирует с тяжестью заболевания, а увеличение ее активности свидетельствует о воспалительном процессе в пародонте. Это происходит в результате активизации пародонтопатогенной бактериальной микрофлоры, содержащей большое количество щелочной фосфатазы. Увеличение активности щелочной фосфатазы может быть обусловлено разрушением тканей пародонта и выходом в ротовую жидкость данных ферментов из клеток соединительной ткани и клеток, участвующих в поддержании структуры остеокластов и остеобластов.
Значения щелочной фосфатазы до начала лечения у пациентов с хроническим генерализованным пародонтитом средней степени тяжести в обследуемых группах колебались от 24,54±0,42 до 26,18±0,15 МЕ/мл и были в среднем в 1,5 раза выше значений щелочной фосфатазы в контрольной группе у лиц с интактным пародонтом. Полученные значения активности щелочной фосфатазы указывают на наличие хронического воспаления в тканях пародонта и нарушения метаболических процессов в костной ткани, что согласуется с данными литературы.
Значения щелочной фосфатазы через 1 мес после лечения во всех группах снизились и находились в пределах нормы.
Через 6 мес в обследуемых группах, несмотря на отсутствие клинических признаков воспаления десны, при удовлетворительной гигиене полости рта уровень щелочной фосфатазы в ротовой жидкости изменился. В группе, где использовали препарат, значение щелочной фосфатазы через 6 мес после лечения осталось в пределах нормы. В группе, где препарат не применялся на этапах лечения, уровень щелочной фосфатазы увеличился и приблизился к значениям до лечения.
Антигомотоксический препарат при комплексном лечении пародонтита средней степени тяжести вызвал значительное и более длительное снижение активности щелочной фосфатазы, чем при традиционном лечении. Считается, что снижение активности щелочной фосфатазы является дополнительным показателем эффективности проведенного лечения и свидетельствует об уменьшении степени сенсибилизации и снижении активности патологического процесса.
Активность трансаминаз ротовой жидкости (аланин- и аспартатаминотрансферазы) отражает глубину воспалительных процессов и состояние аминокислотного обмена в тканях пародонта.
В нашем исследовании у пациентов контрольной группы активность аланинаминотрансферазы составила 6,71±0,42 МЕ/л, аспартатаминотрансферазы — 18,38±0,25 МЕ/л, что укладывается в пределы нормальных показателей.
В результате анализа выявлено статистически значимое отличие активности аланин- и аспартатаминотрансферазы в ротовой жидкости пациентов с хроническим генерализованным пародонтитом средней степени тяжести от значений в контрольной группе. При определении активности аминотрансфераз в ротовой жидкости у пациентов с хроническим генерализованным пародонтитом средней степени тяжести до лечения выявлено повышение активности на 50% аланинаминотрансферазы и на 30% аспартатаминотрансферазы по сравнению с контрольной группой.
Через 1 мес после начала лечения активность аланинаминотрансферазы в ротовой жидкости пациентов с хроническим генерализованным пародонтитом средней степени тяжести в исследуемых группах достоверно (р

Наиболее мощным фактором, способствующим развитию и поддержанию болезней пародонта, является развитие дисбиоза в полости рта, который развивается на фоне сниженного иммунитета, или сам приводит к его изменению. Дисбиотические изменения протекают часто на фоне вторичного иммунодефицита
Воспалительные поражения пародонта возникают в результате сложного взаимодействия бактериальной инфекции и ответной реакции организма. Системные факторы и факторы внешней среды, способствующие их развитию, могут влиять и на течение процессов. Для пародонтита характерен комплекс патологических изменений, в основе которых лежат неуклонно прогрессирующее и волнообразно текущее хроническое воспаление, распространяющееся из десны на нижние отделы пародонта, и связанные с ним деструктивные процессы. Таким образом, при пародонтите, как правило, обнаруживается картина сопутствующего ему гингивита, органично входящего в комплекс патологических изменений, характерных для развившихся форм воспалительных заболеваний пародонта.
Развитие хронического пародонтита сопровождается существенными изменениями состояния иммунных механизмов защиты ротовой полости, проявляющимися в местных изменениях состава клеток крови десны (в том числе количественного соотношения популяций и субпопуляций лимфоцитов), а также содержания в слюне иммуноглобулинов и цитокинов. Данные изменения варьируют в зависимости от степени повреждения пародонта и отражают процессы местного воспаления и активации иммунных механизмов защиты. Ингибирование иммунных реакций сопровождается хронизацией патологического процесса и потерей зубов, ведущую роль в патогенезе играет дисбаланс местных иммунных реакций.
Иммунологические исследования пациентов с тяжелыми формами генерализованного пародонтита показали, что в общем изолированный патологический процесс сопровождался существенными изменениями Т- и В-звеньев иммунитета. При хроническом генерализованном пародонтите в тканях пародонта развивается поликлональная активация В-лимфоцитов, что привлекает в зону поражения нейтрофильные лейкоциты. Последнее, в условиях активации В-лимфоцитов приводит к неадекватному ответу на присутствие патогенных микроорганизмов.
Снижение функциональной активности авангардной линии антимикробной защиты, представленной нейтрофильными гранулоцитами и макрофагами, способствует пролонгированию течения и хроиизации процесса.
Хронические воспалительные заболевания пародонта развиваются на фоне подавленных механизмов фагоцитарной защиты, при этом характер местной иммунной реакции в зависимости от степени тяжести процесса существенно не различается. У одного и того же пациента выраженность воспалительного процесса в пародонте может колебаться от катарального гингивита до легкой или тяжелой форм пародонтита.
Современные открытия в области расшифровки механизмов естественного и адаптивного иммунитета на наноуровне позволили изучить роль образ-распознающих рецепторов эпителиальных клеток (pattern recognition receptors), идентифицирующих молекулярный образ микроорганизмов, запускающих активацию про- и противовоспалительных цитокиновых каскадов. Так, у больных с хроническим генерализованным пародонтитом в десневой жидкости наблю-. дается- увеличение содержания как про-, так и противовоспалительных медиаторов с наличием признаков ПтД-девиации (снижение уровня INF-y и повышение уровня IL-4). В пародонтальном комплексе у этих пациентов отмечалось выраженное увеличение концентраций Ig классов G, М и А, что, по-видимому, является следствием локальной поликлональной активации В-лимфоцитов. В десневой жидкости больных с хроническим генерализованным пародонтитом установлено повышение уровня цитокинов RANKL, TNF-a, TL-1 и снижение концентрации OPG, ч то может быть причиной активации остеокластов и последующей деструкции костной ткани. В зоне пародонта при этом развивается «нетипичное» для хронического процесса воспаление, характеризующееся повышенным уровнем IL-8 и преобладанием количества нейтрофилов над численностью других форм лейкоцитов.
Опосредованное образ-распознающими рецепторами преодоление эпителиального барьера микробами с формированием хронического очага инфекции возможно при внедрении как патогенной, так и условно-патогенной нормальной микрофлоры, если развивается утрата местной толерантности к ней. Известно, что интактный пародонт представляет собой достаточно эффективный барьер для бактерий. Инвазии пародонтопатоге-нов препятствует соединительнотканный эпителий и комплекс иммунных факторов защиты. В тех случаях, когда общая масса бактерий или вирулентность некоторых их видов достигает определенного критического уровня, происходит их внедрение в ткани пародонта. Возможно, этому способствует травма пародонта, а также сбои в иммунной системе.
В процессе инвазии бактерии могут вырабатывать соединения, ингибирующие или полностью блокирующие активность защитных сил. Инвазия бактерий приводит к гибели тканей и образованию микроабсцессов. Гистологически, в коронковой части пародонтального кармана внедрившиеся бактерии окружены мощными инфильтратами плазматических клеток, защищающими нижележащие ткани от инфекции. Уничтожение бактерий, внедрившихся в клетки и ткани пародонта, осуществляется посредством клеток фагоцитарной и лимфоцито-макрофаговой систем. Эти системы сами по себе обладают большим деструктивным потенциалом и могут стать причиной нарушения тканей пародонта вследствие дегрануляции и выработки цитокинов.
Иммунный ответ организма на присутствие пародонтопатогенов основан на взаимодействии нескольких систем: слизисто-секреторной, нейтрофильной, гуморальной, комплементарной и иммунорегуляторной. Предполагают, что основным механизмом слизисто-секреторной системы защиты является препятствие прикреплению на поверхности клеток адгезивных элементов пародонтопатогенов. Микроорганизмы с более активной адгезивной системой, например, трепонемы, прикрепляются к поверхностной мембране эпителиальных клеток. Другие микробы, отторгнутые защитной системой, прикрепляются к трепонеме и продолжают колонизацию.
Бактерицидные свойства слюны предотвращает развитие патогенной микрофлоры зубного налета, ведущего этиологического фактора заболеваний пародонта. Доказательством участия слизистосекреторной системы в защите от инвазии пародонтопатогенов являются фактические данные об увеличении содержания секреторного иммуноглобулина А (slgA) в слюне у больных пародонтитом. Однако эти данные противоречивы. Так, Орехова Л.Ю. с соавт. (2001) обнаружили снижение уровня секреторного иммуноглобулина в ротовой жидкости при пародонтитах.
Барер Г.М., Лемецкая Т.И. (1996) выявили повышенный уровень иммуноглобулинов основных классов вследствие их местного синтеза в воспаленной десне, а также транссудации из пораженных тканей с последующим поступлением десневой жидкости в смешанную слюну. В крови больных с данной‘Патологией снижается концентрация Ig А, М, G. По данным А.А. Кунина с соавт. (2001) при хроническом генерализованном пародонтите в стадии обострения содержание в ротовой жидкости Ig А, Е, G и лизоцима повышено, в то же время содержание slgA понижено, появляются следы Ig М. В десневой жидкости значительно увеличено количество макрофагов, нейтрофилов, лимфоцитов и эпителиоцитов. При этом в три раза снижена функциональная активность Т-лимфоцитов капиллярной крови десны.
Таким образом, хронический гингивит и пародонтит представляют собой многокомпонентные процессы, ключевыми из которых, с одной стороны, являются воспалительно-инфильтративные и деструктивные, а с другой стороны — компенсаторные. Ремиссия, которая наступает самостоятельно либо достигается проведением эффективного лечения, есть результат мобилизации и компенсаторной перестройки тканевых систем пародонта с их выведением на новый уровень гомеостаза. Наиболее мощным фактором, способствующим развитию и поддержанию болезней пародонта, является развитие дисбиоза в полости рта, который развивается или на фоне сниженного иммунитета, или сам приводит к его изменению.
Существует также механическая теория, которая позволяет по-новому взглянуть на патогенез воспалительного процесса в тканях пародонта. Весьма существенными явились результаты изучения изменений в системе иммунитета при длительной гиподинамии. Было обнаружено снижение способности лимфоцитов к активации и пролиферации, что повышает степень риска развития инфекционного процесса. Хорошо известно, что в полости рта лимфоциты относят к факторам местной защиты. Они мигрируют из лимфоидной ткани глоточного кольца и крови, через стенки микрососудов, обильно кровоснабжающих ткани десны. При длительной гипокинезии количество функционирующих микрососудов значительно уменьшается. Для тканей пародонта очень важно, что уменьшение кровоснабжения снижает уровень миграции клеток крови в десневую и ротовую жидкости. Это-касается также и сывороточных иммуноглобулинов, и компонентов комплементов, являющихся гуморальными факторами местной защиты тканей полости рта.
Можно представить, что снижение активности лимфоцитов влечет за собой уменьшение продуцирования секреторного иммуноглобулина IgA плазматическими клетками, образующимися из местных В-лимфоцитов в слизистой оболочке десны. Снижение же способности лимфоцитов к пролиферации, ведет к уменьшению связанных с ними иммуноглобулинов, что в свою очередь ослабляет защитные реакции в тканях пародонта. Становится понятным, что именно снижением активности лимфоцитов по причине регионарной гиподинамии и гипокинезии можно объяснить тот факт, что защитная реакция в пародонте начинается не с активации лимфоцитов антигенами микробов зубной бляшки, а с нейтрофильного хемотаксиса — увеличения числа нейтрофилов в зубодесневой борозде.
Для понимания механизмов развития деструктивных процессов в пародонте чрезвычайно важным явилось обнаружение при изучении иммунной системы в условиях гипокинезии достоверного увеличения продукции лимфоцитами остеокластактивирующего фактора, который вызывает потерю Са костной тканью. Совершенно очевидно также, что снижение интенсивности жевательной функции сопровождается снижением уровня саливации, что в свою очередь, ослабляет естественную резистентность тканей полости рта (в частности за счет таких факторов, как лизоцим, муцин и пр.). С уменьшением, саливации страдает и такой путь, снижения количества микроорганизмов в полости рта, как смыв их ротовой жидкостью.
Все вместе взятое благоприятствует микробной агрессии в полости рта и развитию воспаления в тканях пародонта, которые имеют наибольший контакт со скоплением микробов в зубной бляшке. Для развития воспаления в пародонте не менее важным является то, что гиподинамия способствует нарастанию устойчивости патогенных микробов к антибиотикам и возникновению аутоинфекции, а также сенсибилизации аллергенами аутомикрофлоры. Последнее, как установлено, вызывает потерю костной ткани в пародонте.
Благодаря изучению проблем гипокинезии и гиподинамии, стало очевидным, что малоподвижный образ жизни, который ведет человек в нашем столетии, отрицательно сказывается на состоянии его иммунной системы и сопротивляемости микробным инфекциям. Следует полагать, что это усугубляет последствия снижения факторов местной защиты полости рта, связанные с регионарной гиподинамией и гипокинезией (гипофункцией) в жевательной системе. Дополнением к этому являются многочисленные соматические заболевания, которые еще больше ослабляют иммунные силы организма и приводят в своем патогенезе к убыли костной ткани.
Таким образом, хронические очаги инфекции в полости рта вносят существенный вклад в развитие иммунологических дисбалансов, постоянно отвлекая на себя иммунологические ресурсы организма и истощая общий потенциал противоинфекционной защиты, что множит число вновь возникающих инфекционных очагов и хронизирует их. С другой стороны, полость рта у этих больных становится постоянно существующим источником распространения инфекции в нижележащие органы, а также лимфогенно и гематогенно по всему организму. Персистирующий антигенный инфекционный стимул неизбежно обусловливает аллергическую сенсибилизацию организма, что еще более грубо нарушает равновесие иммунной системы»больных, оказывая на нее угнетающее и дезорганизующее влияние.

Приглашаем подписаться на наш канал в Яндекс Дзен
Читайте также:

