Для некротизации пульпы в моляре верхней челюсти достаточно мышьяковистой пасты
Опубликовано: 25.04.2024

Введение. В стоматологической практике до сих пор используется ангидрид мышьяковистой кислоты (As2O3) в виде пасты для девитализации пульпы зуба. Этот метод лечения пульпита - девитализация пульпы зуба, - был предложен в 1836 году Spooner. Сущность девитальных методов лечения - удаление коронковой и корневой пульпы с предварительной деструкцией всех структур этой ткани, нарушением ее функции. Глубина поражения пульпы зависит от сроков действия и дозы мышьяковистого ангидрида. Показания для девитального метода лечения пульпита: острый диффузный пульпит, хронический фиброзныйпульпит, хронический гипертрофический пульпит в зубах с непроходимыми, искривленными корнями у пожилых пациентов, при непереносимости (аллергии) к местным анестетикам, тяжелом общем состоянии (например, постинсультное, постинфарктное состояние, декомпенсированное течение сердечно-сосудистых заболеваний), ограниченном открывании рта (контрактура нижней челюсти).
Мышьяк - химический элемент V группы периодической системы, не металл, относится к семейству азота. Мышьяк относят к иммунотоксичным элементам, «тиоловым ядам». Он взаимодействует с тиоловыми группами белков, цистеином, глутатионом, липоевой кислотой, оказывает влияние на окислительные процессы в митохондриях. Токсическая доза для человека - 5–50 мг. Органы-мишени для мышьяка: костный мозг, ЖКТ, кожа, легкие, почки. Механизм токсического действия мышьяка связан с нарушением обмена серы, селена и фосфора. Механизм некротического действия мышьяковистого ангидрида следующий. Будучи протоплазматическим ядом, он реагирует с сульфгидрильными группами, блокируя ферментные системы (тиоловые ферменты) путем вытеснения из них водорода. Оксидаза теряет свои специфические функции как фермент окисления, что приводит к местному нарушению тканевого дыхания, гипоксии. Под действием самого малого количества мышьяка отмечается расширение кровеносных сосудов, развивается тромбоз, возникают кровоизлияния. Нервные волокна претерпевают зернистый распад миелиновых оболочек, узловатое набухание и распад осевого цилиндра. Нарушение тканевого дыхания, изменение обмена веществ приводит к гибели клеток.Трехвалентный мышьяк снижает ресинтез АТФ, образование щавелевоуксусной кислоты из пирувата, что влечет развитие гипогликемии. Нарушение гликолиза сопровождается нарушением синтеза ацетилхолина, что является причиной развития периферической невропатии. Образование АТФ-арсената (вместо нативного АДФ) также нарушает нормальный синтез АТФ. Невропатия проявляется мышечной слабостью, снижением рефлексов, доминированием боли и нарушением чувствительности. Мышьяковистая трехокись, растворившись в воде с образованием мышьяковистой кислоты, становится чрезвычайно ядовитой к мягким и твердым тканям и канцерогенной. Мышьяк способен кумулироваться в организме (паренхиматозные органы, кости, кожа, ногти, волосы).
Мышьяковистый некроз челюсти. Таким образом, длительное воздействие мышьяка может вызвать токсические изменения в периодонте зуба и некроз окружающих тканей (см. фото). Если мышьяковистую пасту, наложенную на дно кариозной полости, не герметично изолировать временной пломбой, то мышьяковистый ангидрид вызывает ожог десны, а затем некроз кости (остеонекроз) - заболевание, характеризующееся гибелью костных клеток в участках ишемии, которое имеет хроническое прогрессирующее течение, длительность заболевания составляет от 1 года до 8 лет; остеонекроз длительное время может протекать бессимптомно, в последующем пациента может беспокоить боль в кости, возможно развитие невропатии и др. Специфических клинических проявлений мышьяковистый остеонекроз не имеет, что затрудняет дифференциальный диагноз заболевания. В диагностике остеонекроза имеют значение лучевые методы исследования (например, рентгенологическое исследование челюстей [см. фото]). Эпидемиологические исследования остеонекроза в России не проводились. В США каждый год регистрируется 15000 новых случаев остеонекроза, чаще у мужчин молодого и среднего (20-50 лет) возраста.
Лечение остеонекроза - это сложный и длительный процесс. При передозировке мышьяковистой пасты, увеличении времени ее экспозиции, при ожоге слизистой оболочки альвеолярного отростка челюсти лечение заключается во вскрытии полости зуба, удалении пульпы, промывании корневого канала антидотом мышьяка - 5% раствором унитиола (для обезвреживания всосавшегося мышьяка внутримышечно вводят 1 мл 5% раствора унитиола на 10 кг массы больного: первые сутки - 3 - 4 инъекции, во вторые - 2 - 3 инъекции, в последующие 3 - 7 суток - 1 - 2 инъекции в сутки). ! Репаративные процессы в ране после удаления леченого зуба и некрэктомии челюсти характеризуются медленным течением.
Лечение ожога слизистой оболочки заключается в максимально быстром удалении остатков вещества (мышьяка) с поверхности слизистой оболочки и ее активное, длительное промывание раствором антисептика, перекиси водорода, обработка мыльной или известковой водой, присыпание жженой магнезией, смазывание поверхности некроза настойкой йода. Это позволит предотвратить более глубокое распространение препарата в ткани. После отторжения некротических масс и образования демаркационной зоны рану обрабатывают кератопластическими препаратами (витамин А, масло шиповника, каратолина, облепиховое масло, винилин и др.), так как раны отличаются длительным течением и слабой наклонностью к эпителизации.
Медикаментозное лечение включает назначение курантила, ксантинола никотината, трентала в течение 1-3 месяцев. Регуляторы кальциевого обмена способствуют ремоделированию костной ткани в сочетании с -кальцидолом. Применение фосамакса (активное действующее вещество: алендроновая кислота) в комплексном лечении мышьяковистого остеонекроза челюсти уменьшает боль в челюсти, активизирует метаболические процессы в костной ткани (восстановление костной ткани), сокращает длительность воспалительного процесса (фосамакс принимают после утреннего подъема с постели, за 30 мин до первого приема пищи, запивая полным стаканом воды. Нельзя разжевывать или рассасывать таблетку в полости рта; препарат принимают в дозе 70 мг 1 раз в неделю в течение 1 месяца). В комплекс лечения включают ЛФК, лазеро- и магнитотерапию.
Профилактика. Для профилактики осложнений при девитализации пульпы мышьяковистой пастой необходимо: соблюдать показания к данному методу лечения (см. начало статьи), избегать передозировки препарата, создать герметичность закрытия препарата временной пломбой. При использовании мышьяковистой пасты врач-стоматолог должен придерживаться дозирования пасты в зависимости от размера зуба, состояния пульпы, возраста больного. Для девитализации пульпы достаточно 0,0002 - 0,0004 г мышьяковистого ангидрида, рекомендуемая продолжительность действия в однокорневых зубах - 24 часа, в многокорневых зубах - 48 часов. В настоящее время для облегчения дозирования мышьяковистая паста выпускается в виде гранул или ниточек различного цвета. Кариозная полость должна быть герметично закрыта для предотвращения утечки мышьяковистой пасты. При расположении кариозной полости на контактной поверхности коронки зуба необходимо восстановить стенку стекло-иономерным цементом, чтобы исключить любой контакт мышьяка со слизистой оболочкой.
В процессе лечения пульпита иногда возникает необходимость девитализации (некротизации) пульпы. Хотя следует отметить, что более целесообразным считается лечение пульпита под анестезией в одно посещение — метод витальной экстирпации.
В настоящее время применяется два способа девитализации пульпы зуба: применение девитализирующих паст и электрохимический некроз пульпы.
ДЕВИТАЛИЗИРУЮЩИЕ ПАСТЫ
Для девитализации пульпы зуба применяют либо мышьяковистую, либо параформальдегидную пасту.
Мышьяковистая паста включает в свой состав:
I. Мышьяковистый ангидрид, оказывающий на пульпу не- кротизирующес действие.
Описано три основных механизма местного токсическою действия мышьяковистого ангидрида:
— прямое цитотоксическое действие, связанное с блокадой цитохромов, что приводит к нарушению процессов клеточного дыхания и гибели клеток;
-денатурация белков при контакте с мышьяковистым ангидридом;
— блокада соединениями мышьяка синапсов симпатических нервных волокон, в результате чего происходит нарушение тонуса кровеносных сосудов, их расширение, стаз крови и тромбоз. Это приводит к прекращению кровообращения в пульпе.
2. Местный анестетик (чаще дикаин) для быстрого купирования болевого синдрома.
3. Сильный антисептик (тимол, карболовая кислота, камфора) для подавления микрофлоры в полости зуба, предотвращения распространения микроорганизмов в глубжележащие ткани, обеззараживания пульпы в дентинных канальцах и дельтовидных разветвлениях.
4. Вяжущие вещества (танин) добавляют в мышьяковистую пасту для увеличения продолжительности ее действия. Такие пасты пролонгированного действия применяют, если пациент не может явиться на прием в ближайшие двое суток.
Примером «стандартной» мышьяковистой пасты может служить состав препарата «Arsenic Paste» компании «Dentstal»
Мышьяковистый ангидрид — 30,0
Лидокаина гидрохлорид — 28,5
Наполнитель — до 100,0
Основные правила наложения мышьяковистой пасты
— мышьяковистую пасту рекомендуется накладывать на вскрытый рог пульпы. Иногда допускается наложение девитализирующей пасты на невскрытую пульпу. Однако в этом случае увеличивается риск усиления болевого синдрома за счет отека пульпы и повышения давления в полости зуба;


чтобы уменьшить риск «утечки» компонентов мышьяковистой пасты через краевую щель между стенками полости и временным материалом, нужно накладывать девитализирующую пасту таким образом, чтобы расстояние между ней и краем полости было не менее 2 мм (рис. 468). Особенно это требование актуально при придесневой или межзубной локализации кариозной полости, где повышена вероятность попадания мышьяковистого ангидрида на слизистую оболочку, что может привести к «мышьяковистому ожогу» или «мышьяковистому некрозу» десневого края и глубжележащих тканей; количество мышьяковистой пасты, необходимое для девитализации пульпы одного зуба, соответствует размеру головки шаровидного бора №1 (доза мышьяковистого ангидрида — 0,0006-0,0008 г);

— поверх мышьяковистой пасты накладывают небольшой ватный тампон, пропитанный раствором анестетика и отжатый;
— полость без давления герметично закрывают повязкой из водного дентина;
— сроки наложения «стандартной» мышьяковистой пасты: в резцах, клыках, премолярах — 24 часа, в молярах — 48 часов. В зависимости от особенностей состава сроки наложения девитализирующих паст могут изменяться. В данном вопросе следует руководствоваться рекомендациями фирмы-производителя.
Параформальдегидная паста предназначена для девитализации и мумификации пульпы. Параформальдегид (параформ, триоксиметилен) является продуктом полимеризации формальдегида. В высоких концентрациях он вызывает некроз тканей и оказывает бактерицидное действие. Преимуществом параформальдегидной пасты перед мышьяковистой является более мягкое действие: она не вызывает раздражения периодонта. Девитализация пульпы происходит через 6—8 дней.
Накладывается параформальдегцдная паста по тем же правилам, что и мышьяковистая.
Примером параформальдегидной пасты может служить препарат «Caustinerf fort sans arsenic» компании «Septodont» (рис. 469):
Лидокаина гидрохлорид — 37,0
Фирма «Septodont» выпускает три препарата для девигализации пульпы зуба:
— «Каустинерв мышьяковистый» — «Caustinerf arsenical»;
— «Каустинерв быстродействующий» — «Caustinerf rapide»;
— «Каустинерв защищающий без мышьяка» — «Caustinerf fort sans arsenic».
Девитализация пульпы перечисленными препаратами основана не только на некротизации, но и на склерозировании пульпы. Благодаря этому, даже если в микроканальцах или дополнительных ответвлениях корневых каналов и остается ткань пульпы, то после применения «Каустинерва» она бывает склерозирована и антисептически обработана.
Выбор препарата у взрослых пациентов производится с учетом клинической ситуации в зависимости от желаемого срока девитализации пульпы (табл. 62). Это очень удобно при планировании следующего посещения.

Сроки действия девитализирующих паст фирмы «Septodont»
Сроки девитализации пульпы
Caustinerf arsenical Caustinerf rapide Caustinerf fort sans arsenic
7 дней 3 дня 7-10 дней
ЭЛЕКТРОХИМИЧЕСКИЙ НЕКРОЗ ПУЛЬПЫ
Если в процессе эндодонтического лечения пульпита пройти канал не удается, девитализацию пульпы в непройденной части канала можно провести с помощью трансканального электрофореза 10% спиртового раствора йода.
Техника проведения этой процедуры достаточно проста (см. рис. 470).
Предварительно пломбируются хорошо проходимые каналы. Затем на устья не пройденных каналов накладывается небольшой ватный тампон, смоченный 10% спиртовым раствором (настойкой) йода, в него погружается активный электрод (катод), который представляет собой одножильный медный провод в полихлорвиниловой изоляции. Конец электрода должен быть очищен от изоляции на 2-3 мм. Тампон изолируется от среды полости рта липким воском. Пассивный электрод (анод) накладывается на предплечье.
Процедура обязательно проводится под анестезией. Необходимость этого диктуется тем, что при сохранении болевой чувствительности невозможно установить силу тока, достаточную для полноценного некроза пульпы. Сила тока — 3 мА (не меньше!). Продолжительность одной процедуры — 15 минут. После первой процедуры меняется ватный тампон с настойкой йода, в него погружается электрод, заливается липким воском и в это же посещение делается вторая процедура. Затем пациент направляется к врачу-стоматологу для продолжения лечения.

Некроз пульпы в данном случае происходит за счет электрохимических процессов, протекающих под кагодом (образование щелочей, которые вызывают глубокий колликвационный ожог и некроз пульпы). Следует также иметь в виду, что длительного обеззараживания содержимого непроходимой части канала данная процедура не обеспечивает. Поэтому, после проведения электрохимического некроза пульпы обязательна импрегнация не удаленной части пульпы или депофорез гидроксида меди-кальция.
Преимущество электрохимического некроза пульпы перед использованием девитализирующих паст — возможность сократить количество посещений, так как пульпа некротизируется в течение 35—40 минут, и в первое же посещение можно приступать к импрегнации содержимого не пройденной части корневого канала.
М. А. Егорова
студентка ГОУ ВПО «Казанский государственный медицинский университет» Росздрава, кафедра терапевтической стоматологии
Л. Р. Мухамеджанова
д. м. н., доцент, заведующая кафедрой терапевтической стоматологии ГОУ ВПО «Казанский государственный медицинский университет» Росздрава, кафедра терапевтической стоматологии
Более четырех столетий назад немецкий алхимик, философ и оккультист Теофраст Гугенгейм, известный как Парацельс, предложил использовать мышьяк и его соединения для лечения различных заболеваний. С этого времени, пожалуй, и начинается нелегкая, полная драматических моментов «медицинская судьба» мышьяковистых соединений. Одновременно идет активное изучение их биологического действия. Уже к середине XVII века были разработаны рецептурные прописи, включающие мышьяковистую кислоту и предназначенные для лечения заболеваний крови, инфекционных заболеваний и др. Не остались в стороне и дантисты, для которых проблема обезболивания воспаленной пульпы была своеобразной «болевой точкой».
Современные специалисты, занимающиеся вопросами эндодонтии, используют многочисленные препараты мышьяка для девитализации пульпы, при этом мнения о целесообразности их применения зачастую бывают диаметрально противоположными. Поэтому нам представляется весьма актуальным изучение исторических аспектов создания и использования мышьяковистой пасты в зубоврачевании.
Материалом для исследования послужили выдержки из руководств по зубоврачеванию XVII — XX веков, историографическое описание развития зубоврачевания.
Анализ источниковой базы свидетельствует о том, что мышьяк использовали при лечении пораженных зубов примерно в 500 г. до н. э., о чем записано в книге Чжу-Цина. Однако после этого и до XIX века никаких упоминаний больше не найдено. В первой половине XIX века наконец начали реализовываться идеи J . Hunter : были предприняты попытки удаления пульпы тонким зазубренным инструментом после прижигания ее кислотой. Нерв удаляли трепаном, иглами или специальным ручным инструментом-троакаром. Пульпу продолжали прижигать с целью предварительного обезболивания подобных вмешательств. Однако в это же время в эндодонтическую практику было привнесено средство, существенно изменившее ее характер: в 1836 г. американский дантист Shearjashub Spooner в труде «Путь к здоровым зубам, или Популярный трактат о зубах» описал способ «умерщвления нерва» мышьяковистой кислотой (хотя и без последующего его удаления). Мышьяковистую кислоту рекомендовалось смешивать с сульфатом морфия. Сегодня нам покажется удивительным этот факт, поскольку в описываемые времена не было ограничений в применении наркотических анальгетиков. В 1872 году в статье «Что мы будем делать с молочным зубом, в котором пульпа подвергается распаду?» (« What shall we do with deciduous teeth in which the pulps are exposed ?») предлагалось наложение мышьяковистого препарата с последующим удалением коронковой пульпы и пломбированием полости временного зуба. Автор считал необходимым предупредить родителей о возможности «…развития периостита, затем — альвеолярного абсцесса», после чего (!) «никаких серьезных проблем не возникает». Немецкий ученый Ad . Witzel (1874) отмечает, что применение мышьяковистой кислоты «создало новый этап в учении о зубных болезнях».
Практическое применение мышьяковистой пасты описывает Ю. Шефф в «Руководстве зубных болезней» (1882). Для устранения зубной боли он предлагает использовать мышьяковистую пасту и карболовую кислоту. Приводит несколько рецептов, содержащих наркотические анальгетики для местной анестезии при непосредственном соприкосновении с обнаженной пульпой: настойка опия; настойка, состоящая из морфия, спирта и хлороформа; пилюли, содержащие креозот. После приготовления последних рекомендовалось «вкладывать на вате на болящую полость».
J . Parreidt (1890) предлагает использовать мышьяковистую пасту при воспалении пульпы еще и как обезболивающее средство: «Удаляют пломбу, прижигают и выскабливают зубную мякоть». Для прижигания автор рекомендует мышьяк, к которому прибавляют небольшое количество карболовой кислоты; вместо морфия используют йодоформ. Паррейдт пользовался прижигающим средством следующего состава:
- R р. Ас id . arsenicosi .
- Pulv. Jodoform. pur. alcoholisat.
- Acid. carbolic . pur . ana .
Впервые ограничения в применении мышьяковистой кислоты были внесены только в 1898 году W . D . Miller в руководстве по консервативному зубоврачеванию. Он указывал, что «…у детей применять мышьяковистую кислоту не следует, зубы их обыкновенно чересчур порозны и мягки, и foramen apicale большею частью слишком широко, либо уже произошло рассасывание части верхушки корня. При таких условиях легко может случиться, что мышьяковистая паста окажет воздействие на корневую оболочку». Следующий «удар» по применению мышьяковистой пасты был нанесен Советом по лекарствам Американской стоматологической ассоциации ( Ada , 1961). Основным недостатком «необратимой девитализирующей анестезии» является токсическое воздействие на периодонт. Вследствие технической сложности дозирования весьма высока вероятность поражения периодонта. Кроме того, не теряло актуальности канцерогенное действие мышьяковистых препаратов.
В XX веке мышьяковистая кислота (ангидрид) начала применяться в виде пасты. Для составления пасты к кислоте добавляли медикаментозные вещества, обладающие анестезирующими, антисептическими свойствами, а также средства, замедляющие диффузию мышьяка в ткань пульпы и тем самым ослабляющие его токсическое действие. Для этой цели использовали новокаин, карболовую кислоту, танин, йодоформ, гвоздичное, камфорное масла, глицерин. Е. М. Гофунг и И. Г. Лукомский (1936) рекомендуют вводить в мышьяковистую пасту танин и коричное масло, что способствует одновременно и мумификации каутеризированной пульпы. Присутствие в пасте морфина или кокаина рассчитано на меньшую чувствительность пульпы в процессе девитализации, однако многие считают их действие весьма сомнительным. Добавление к пасте креозота или карболовой кислоты вызывает ожог пульпы с последующим струпом, мешает быстрому всасыванию мышьяка.
В литературе упоминается применение черепичного мышьяка для девитализации пульпы. Действие его нежнее мышьяка, а главное — он не дает осложнений на периапикальные ткани. Однако черепичный мышьяк есть не что иное, как кобальт, действие которого принципиально отличается от действия мышьяковистой кислоты.
В 1927 году M ủ ller делает чрезвычайное указание: «…пульпы, экстирпированные после девитализации их мышьяковистой пастой, оказались стерильными». Это новое обстоятельство значительно повышало ценность мышьяка. Однако сегодня известно, что мышьяк сам по себе не обладает бактерицидными свойствами. Здесь имеют значение вещества, входящие в состав мышьяковистой пасты: фенол, креозот и др.
Учитывая то, что мышьяковистая кислота представляет собой сильный протоплазматический яд, необходимо строго придерживаться дозирования пасты в зависимости от размеров зуба, состояния пульпы, возраста больного и выбора метода лечения пульпита. Однако множество споров вызвала дозировка мышъяковистой пасты. Позже пришли к мнению, что достаточно 0,0002-0,0004 г мышьяковистой кислоты в однокорневых зубах оставлять на 24 часа, в многокорневых — на 48 часов. Одним из главных условий наложения пасты является непосредственный контакт с тканью пульпы. А. И. Рыбаков (1980) отмечает, что «правильное вскрытие рога пульпы является искусством. От того, как вскрывается зубная полость, зависит успех дальнейшего лечения».
На сегодняшний день детально изучен механизм воздействия мышьяковистой кислоты на пульпу. Будучи протоплазматическим ядом, мышьяковистый ангидрид, прежде всего, воздействует на окислительные ферменты пульпы, приводит к местному нарушению тканевого дыхания и явлениям гипоксии. Под действием самого малого количества мышьяка оксидаза теряет свои специфические функции как фермент окисления. Кроме того, мышьяк блокирует тиоловые соединения, выполняющие функции коферментов дыхания. В симптомокомплексе действия мышьяка на пульпу очень характерны изменения в сосудистой системе. Уже через 2-2,5 часа после начала девитализации развивается гиперемия, сосуды, особенно капилляры, резко расширены, затем появляются многочисленные кровоизлияния, которые зависят от изменения стенок сосудов и потери их сопротивляемости. Отек приводит к сдавлению ткани пульпы. Нервные волокна пульпы претерпевают зернистый распад миелиновых оболочек, узловатое набухание и распад осевого цилиндра. Варикозность нервного волокна сменяется его гибелью. Изменения во всех группах клеточных элементов пульпы сводятся к явлениям кариорексиса и гибели клеток, в первую очередь одонтобластов. Глубина поражения пульпы находится в непосредственной связи со сроком действия и дозой мышьяковистой кислоты. В месте приложения мышьяковистой кислоты наблюдается картина гибели всех элементов коронковой пульпы.
Что касается тех случаев, когда мышьяковистая паста не оказывает достаточного действия, то они объясняются присутствием в пульпе дентиклов, которые не пропускают через себя мышьяк и являются для него непреодолимым препятствием. В таких случаях Е. М. Гофунг и И. Г. Лукомский (1936) рекомендуют удалить дентиклы и вновь наложить мышьяковистую пасту.
Удачно проведенная девитализация обеспечивает демаркацию между некротизированной пульпой и периодонтом, в результате чего создаются условия для выделения пульпы из каналов с минимальным кровотечением и, следовательно, для заживления операционной раны после экстирпации.
В настоящее время на отечественном и зарубежном фармацевтическом рынке появляется огромное количество лекарственных форм, предназначенных для профессионального применения в стоматологии. И мышьяковистые препараты для девитализации пульпы тоже не остались без внимания научно-исследовательских лабораторий ведущих предприятий по производству стоматологических материалов. Мышьяковистая паста стала выпускаться дозированно, в виде гранул различного цвета в зависимости от необходимых сроков наложения пасты (зеленый, синий и др.). Иногда в состав мышьяковистой пасты вводят наполнитель в виде ниточек разного цвета (или ваты) для правильной дозировки, что значительно облегчило применение их при различных клинических ситуациях.
Таким образом, на основании аналитического обзора литературных источников мы считаем целесообразным выделение трех этапов истории применения мышьяковистого ангидрида при лечении пульпита. 1-й этап (500 г. до н. э. — начало Х I Х века) характеризуется применением мышьяковистого ангидрида без добавления наркотических аналгетиков, антисептиков и консистентных веществ. На 2-м этапе (середина Х I Х века — середина ХХ века) мышьяковистый ангидрид входит в состав многокомпонентных паст, содержащих анальгетики, мумифицирующие препараты, консистентные вещества. 3-й этап (с середины ХХ века по настоящее время) отличается применением дозированных, пролонгированных препаратов, позволяющих осуществить индивидуальный подход к подбору дозы и определить длительность периода девитализации пульпы.
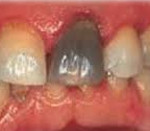
Некроз пульпы - это гибель клеток сосудисто-нервного пучка в коронковой или корневой части зуба, возникающая как следствие осложненного кариеса или травматического повреждения зуба. Заболевание может протекать бессимптомно, но чаще основным проявлением некроза пульпы является продолжительная ноющая боль в зубе от горячей пищи. Диагностику данной стоматологической патологии проводят на основании жалоб пациента, прицельной дентальной рентгенографии, температурных проб и электроодонтометрии. Для лечения некроза пульпы проводят эндодонтическую обработку корневых каналов с их дальнейшей пломбировкой.
- Причины некроза пульпы
- Классификация некроза пульпы
- Симптомы некроза пульпы
- Диагностика некроза пульпы
- Лечение некроза пульпы
- Цены на лечение
Общие сведения
Некроз пульпы - это необратимая форма пульпита. Некоторые авторы относят некроз пульпы к хроническому гангренозному пульпиту, другие выделяют в отдельную патологию. При некрозе пульпы происходит отмирание части сосудисто-нервного пучка в коронковой или в корневой пульпе зуба. За счет образования некротизированных участков нерва и нарушения кровоснабжения угнетаются иммунные факторы зуба, возникают условия для размножения бактерий. Некроз пульпы может развиваться как в молочных, так и в постоянных зубах. Этой патологии подвержены мужчины и женщины любых возрастов. Очень важно диагностировать некроз пульпы вовремя, потому что часто воспалительные явления переходят на периодонтальную связку и приводят к повреждению тканей периодонта.

Причины некроза пульпы
Выделяют несколько групп факторов, приводящих к возникновению некроза пульпы: химические, бактериальные, термические и механические. Химический некроз пульпы чаще всего возникает в результате применения агрессивных веществ на этапе лечения кариеса, например, спирта или фенола и др. Вещество проникает в пульпу зуба через дентинные канальцы, в результате чего происходит химический ожог тканей сосудисто-нервного пучка зуба, который заканчивается его некрозом. Химический некроз пульпы приводит к развитию воспалительных явлений в периодонтальной связке, окружающей зуб. Выявляется такой вид некроза случайно, при обнаружении на рентгенограмме изменений в периапикальных тканях зуба. Также внимание врача привлекает серый цвет твёрдых тканей. Такой зуб чаще всего ранее лечен по поводу среднего или глубокого кариеса.
При бактериальном поражении пульпы зуба в тканях сосудисто-нервного пучка обнаруживают смешанную микрофлору, в то время как здоровая пульпа зуба - стерильна. Основное значение отводят стрептококку и стафилококку. Также при микробиологическом исследовании обнаруживают аэробных микроорганизмов - клостридии перфрингенс, фузобактерии. Термический некроз пульпы развивается вследствие ее ожога при обработке зуба, часто во время подготовки к протезированию. Это возникает, если используются наконечники без водяного охлаждения, отчего происходит перегрев тканей.
Травматический некроз пульпы может быть результатом острой или хронической травмы. Острая травма зуба возникает при однократном приложении силы, например, в результате удара, падения. Происходит разрыв периапикальных тканей, нарушается кровоснабжение тканей пульпарной камеры, возникает их некроз. Хроническая травма появляется вследствие длительного регулярного воздействия на периодонт. Сначала этот процесс компенсирован, но в дальнейшем из-за нарушения кровоснабжения происходит некроз пульпы. Это явление может встречаться при патологической стираемости зубов, профессиональных вредных привычках (например, у швей - перекусывание зубами нитки, у рыболовов - лески).
Классификация некроза пульпы
В стоматологии выделяют колликвационный и коагуляционный некроз пульпы. При колликвационном некрозе пораженная ткань имеет дряблую консистенцию, может содержать большое количество жидкости. Этот вид некроза встречается при поражении зуба микроорганизмами и продуктами их жизнедеятельности. Также развитие колликвационного некроза возможно при лечении пульпита биологическим методом, а именно – при прямом покрытии пульпы зуба гидроокисью кальция.
Коагуляционный некроз обычно не связан с хроническим инфекционным воздействием. При таком виде некроза происходит гипоксия и вследствие этого - некротизация участка пульпы зуба. Коагуляционный некроз пульпы встречается при острой травме периодонта, когда нарушается питание сосудисто-нервного пучка зуба. Чаще всего оба вида некроза безболезненны, боль возникает в том случае, если присоединяется такой вид бактерий, как бактероиды. Данная классификация важна при изучении патофизиологии процесса. В клинической практике основное значение уделяют анамнезу заболевания, симптомам и данным дополнительных методов исследования.
Симптомы некроза пульпы
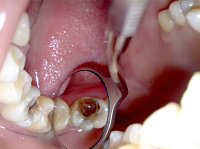
Часто некроз пульпы развивается бессимптомно. Может обнаруживаться случайно при проведении рентгенологического исследования (ортопантомограммы, компьютерной томографии). В таком случае некроз часто сочетается с изменениями в периапикальных тканях зуба. В некоторых случаях пациент обращается к стоматологу с жалобами на изменение цвета зуба. При осмотре полости рта стоматолог обнаруживает зуб серого цвета. При вскрытии пульпарной камеры определяется гнилостный запах. Перкуссия таких зубов бывает положительной. Поверхностные слои пульпы грязно-серого цвета, не кровоточат. Зондирование корневой пульпы также может быть положительно.
Некоторые пациенты предъявляют жалобы на боль от горячей пищи. Это связано с жизнедеятельностью особых бактерий, чаще всего бактероидов. Воздействие горячей температуры приводит к образованию газов в полости зуба. При этом характерно медленное нарастание боли при нагреве зуба и постепенное угасание при устранении раздражителя. Пациенты с некрозом пульпы практически всегда отмечают, что зуб болел ранее.
Диагностика некроза пульпы
Диагностика некроза пульпы проводится на основании жалоб больного, анамнеза заболевания, клинической картины. В качестве дополнительных методов исследования применяют термопробы. Так, зуб с некрозом пульпы либо не будет реагировать на термические раздражители, либо будет давать положительную реакцию на горячее.
На рентгенограмме (ортопантомограмма, прицельные снимки, компьютерная томография) выявляют изменения в тканях периодонта. Отмечается расширение периодонтальной щели, может быть резорбция костной ткани в области верхушки зуба. При электроодонтометрии могут быть получены результаты от 60 до 100 мкА, они связаны с электропроводимостью пульпы: чем больше тканей нерва некротизировано, тем выше будет проводимость электрического тока.
Дифференциальную диагностику некроза пульпы следует проводить с необратимым пульпитом и хроническим верхушечным периодонтитом. При хроническом апикальном периодонтите будет наблюдаться безболезненное зондирование на всем протяжении корневого канала, может быть свищевой ход или рубец от свища, гиперемия переходной складки, такой зуб никогда не реагирует на температурные раздражители, показания ЭОД более 100мкА. При необратимом пульпите сохраняется реакция на температурные раздражители, зондирование болезненно, характерны ночные боли с иррадиацией в прилегающую область.
Лечение некроза пульпы
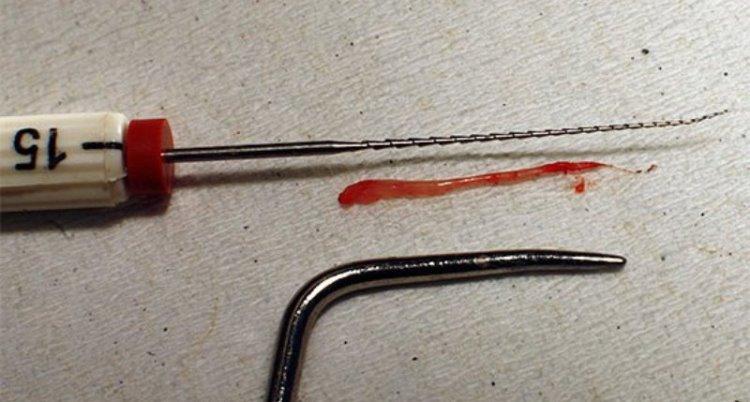
При некрозе пульпы проводится эндодонтическое лечение. Оно подразумевает тщательную обработку корневых каналов. Лечение каналов проводят в несколько этапов. При первом посещении механически очищают стенки корневых каналов ручными или машинными инструментами, промывают антисептическими растворами на основе гипохлорита натрия для удаления некротизированных органических остатков пульпы. Для уничтожения микроорганизмов на две недели в канале оставляют гидроокись кальция, которая создает высокощелочную среду, губительную для бактерий. При втором посещении повторно промывают каналы антисептиками (чаще всего раствором хлоргексидина) и проводят пломбировку корневых каналов.
Для профилактики некроза пульпы необходимо проходить регулярные осмотры у врача-стоматолога, санировать очаги хронической инфекции в полости рта, проводить замену пломб с нарушением краевого прилегания.
Проблемы эндодонтического лечения зубов в случаях некроза пульпы или при неполном формировании корня заключаются в ограниченной эффективности очистки корневого канала и наличие риска выведения пломбировочного материала за пределы апекса. Подобные осложнения возникают по причине дивергенции стенок корневого канала и слишком расширенного апикального сужения.
Использование эндодонтических повязок на основе гидроксида кальция способствует дезинфекции корневого пространства и процессу апексификации, однако подобные процедуры являются довольно длительными и не лишены риска возникновения перелома или повторного инфицирования.
В качестве альтернативного материала был предложен минерал триоксид агрегат – МТА, который решает проблему длительной эндодонтической терапии, но, как и кальций гидроксид, лишь способствует апексификации и депозиции дентина на боковых стенка канала. Следовательно, для физиологического закрытия области верхушки корня необходимо найти такой материал, действие которого обеспечивало бы наиболее естественное протекание данного процесса.
Реваскуляризация пульпы предусматривает дезинфекцию и обильную ирригацию области некротизированной ткани не полностью сформированных зубов с использованием различных антибактериальных растворов и комбинаций антибиотиков по типу ципрофлоксацина, метронидазола, миноциклина и амоксициллина или же с использованием пасты гидроксида кальция.
В ходе повторного посещения с целью реваскуляризации стимулируют внутриканалное кровотечение для образования кровяного сгустка в качестве матрицы восстановления сосудисто-нервного пучка. В конце манипуляции проводится герметизация области шейки зуба.
В данной статье представлен клинический случай реваскуляризация пульпы после травмы в области правого бокового резца верхней челюсти. Результаты 12-месячного наблюдения свидетельствует об успешности проведенного лечения.
История болезни
10-летний пациент был осмотрен в ходе эндодонтического специализированного курса, который проводился Бразильской стоматологической ассоциацией. Со слов пациента стало известно, что два года назад он перенес травму зуба во фронтальной области, а за несколько недель до нынешнего визита начал замечать отек и образование свищевого хода в области травмы. Кроме того, пациента начали беспокоить болевые ощущения в данной области. Системных заболеваний у мальчика не отмечалось.
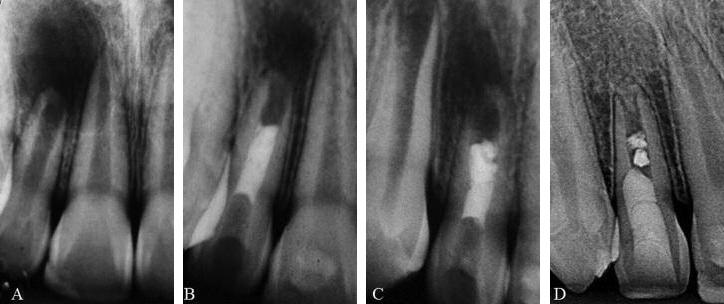
Клинический осмотр включал пальпацию, анализ подвижности зубов, холодовые и температурные тесты (Endo Ice, Hygenic, Akron), а также периодонтальное зондирование в области резца и клыка. Результаты всех исследований были в пределах нормы, за исключением отсутствия реакция на термическое воздействие со стороны правого бокового резца. Данный зуб также демонстрировал подвижность II степени, в рентгенологической проекции были отмечены признаки апикального периодонтита, сопутствующие неполному формированию корней (фото 1а).
Пациенту был поставлен диагноз хронического периапикального абсцесса. Было принято решение сначала провести полужесткое шинирование с целью стабилизация зуба в лунке. В ходе повторного визита после выполнения местной анестезии (2% лидокаин и эпинефрин 1: 80 000) и фиксации коффердама был сформирован эндодонтический доступ с использованием боров 1016HL и 3083 (Dentsply Maillefer). Было обнаружено только одно устье канала, в котором при помощи апекслокатора (Elements Apex Locator, Sybronendo) определяли рабочую длину канала. Обработку эндопространства проводили по методике crown-down, используя для этого K-файлы из третьего поколения (Dentsply Maillefer). Ирригацию проводили посредством 2% раствора хлоргексидина и 2,5 мл физиологического раствора (Fórmula & Ação) при каждом изменении размера файлов. В конце вмешательства в эндодонтическое пространство упаковали антибиотическую пасту, содержащую ципрофлоксацин (200 мг) и метронидазол (500 мг). В качестве временного материала для закрытия доступа применяли микрогибридный композит (Z100, 3M ESPE).
Спустя двадцать девять дней провели удаление временного композитного материала, а также антибиотикосодержащей пасты, после чего обеспечили обильное орошение физиологическим раствором и 2% хлоргексидиновым гелем (Fórmula и Ação). Канал высушивали бумажными штифтами (Tanari) и кровотечение стимулировали файлом 30-го размера (Dentsply Maillefer), стабилизируя сгусток на расстоянии 3 мм ниже эмалево-цементного соединения. В качестве уплотнителя в области шейки зуба применяли минерал триоксид агрегат МТА (Angelus), а в качестве временного восстановительного материала – стеклоиономерный цемент (Ketac-Fil, 3M ESPE) (фото 1b).
После этого пациента направили к врачу для проведения окончательной реставрации проблемного зуба. Через 5 месяцев у больного не отмечалось ни подвижности зуба, ни каких-либо нарушений при проведении пальпации или перкуссии. Стабилизация периапикального очага была подтверждена рентгенологически (фото 1c), клинически же пациент также не проявлял никаких симптомов. Тем не менее, зуб продолжал проявлять чувствительность к действию температурных факторов. Через 12 месяцев рентгенографически было отмечено значительное утолщение боковых стенок корня, завершение их формирования и полное заживление перирадикулярного очага. Наблюдались также признаки значительной адсорбции МТА, что свидетельствовало о заполнении корневого пространства тканями пульпы и депозиции дентина (фото 1d). Зуб нормально реагировал на холодовые тесты, что свидетельствовало об успешности проведенного лечения.
Фото 1
a: Рентгенограмма до начала лечения
b: В качестве барьера в пришеечной области использовали МТА и стеклоиономерный цемент.
c: Рентгенограмма через 5 месяцев.
d: Рентгенограмма через 1 год.
Обсуждение
До недавнего времени апексификация была единственным методом лечения, подходящим для зубов с некрозом пульпы и несформированным корнем. Однако основным недостатком данной терапевтической стратегии является то, что данная процедура является довольно длительной и требует постоянной замены эндодонтических повязок из гидроксида кальция.
Таким образом, повышается риск возникновения перелома корня и его повторного инфицирования. По этой причине в качестве альтернативного материала было предложено использование МТА. Однако, даже данный материал не способствует эффективной диспозиции дентина на боковых стенках корня, а также в области апикального сужения.
Основные цели реваскуляризации пульпы состоят в восстановлении сосудисто-нервного пучка в эндодонтическом пространстве и завершении процесса формирования корня. Следовательно, соответствующие клинические действия при реваскуляризации отличаются от таковых при апексификации.
В данном случае хлоргексидин использовался в качестве вспомогательного химического раствора по причине его меньшей токсичности по сравнению с гипохлоритом натрия, учитывая имеющейся риск выведения химического агента в ткани периодонта при достаточно широком диаметре апикальной части зуба. Данный протокол был также описан еще в ряде недавно опубликованных клинических исследований. Использование гидроксида кальция и/или антибиотических паст является крайне важным этапом лечения для обеспечения реваскуляризации некротизированной пульпы в условиях неполной сформированности корней.
Данные пасты обеспечивают дезинфекцию корневого пространства, поскольку из-за продолжающегося роста корня проведение полноценной механической очистки является нежелательным. Отдельные исследования, однако, указывают на возможный риск изменения цвета зуба после применения пасты миноциклина. Поэтому ципрофлоксацин и метронидазол являлись препаратами выбора в данном клиническом случае.
Отсутствие болевых симптомов, исчезновение свищевого хода, продолжение процесса формирования корней и восстановление чувствительности к действию термических факторов являются ключевыми факторами успеха, указывающими на эффективность проведенной процедуры реваскуляризации. Все позитивные признаки реваскуляризации были отмечены и в данном клиническом случае даже через 12 месяцев в ходе контрольного осмотра пациента. Iwaya (2001) и Banchs и Trope (2004) уже ранее опубликовывали клинические случаи реваскуляризации зубов, в которых им удавалось добиться успешного результата лечения через 30 и 24 месяца соответственно. Исследования, проведенные в различных областях стоматологии, указывают на то, что разные индивиды могут по-разному реагировать на подобные ятрогенные вмешательства, а сама реакция таковых сильно зависит от системных и иммунных условий. Именно позитивное влияние данных факторов может обосновать достижение эффективного результата лечения в такие довольно короткие строки.
Клинический случай, представленный в этой статье, подтверждает тот факт, что реваскуляризация пульпы является перспективным методом лечения зубов с некротизированной пульпой и в условиях неполностью сформированного корня. Однако, учитывая принципы доказательной стоматологии, для аргументации успешности данного метода мы советуем провести дополнительные более детализированные исследования перспективного характера.
Выводы
Цель данной статьи состояла в том, чтобы продемонстрировать позитивный результат реваскуляризации некротизированной пульпы в условиях не полностью сформированного корня зуба. Данная процедура является многообещающей альтернативой апексификации, но для ее аргументации необходимо проведение дополнительного количества исследований.
Авторы: Ricardo Machado, Gustavo Almeida, Thamara Silva Santos, Brunna Presmini Barbosa, Guilherme Augusto Moreira, Alberto Porto Junior
Читайте также:

