Удаление зуба при тромбоцитопатии
Опубликовано: 24.07.2024

Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
Общие принципы лечения приобретенных и наследственных тромбоцитопатии
Диета больных тромбоцитопатиями должна быть витаминизирована с исключением уксуссодержащих консервированных продуктов. Дополнительно назначаются поливитамины, отвар крапивы и орехи арахиса.
Исключаются препараты, вызывающие нарушение свойств тромбоцитов: салицилаты, курантил, папаверин, эуфиллин, индометацин, бруфен, карбенициллин, нитрофураны. Ограничивается прием препаратов, ингибирующих метаболизм арахидоновой кислоты и нарушающих функции тромбоцитов, а также физиотерапевтические процедуры (УФО, УВЧ).
Проводится лечение сопутствующих заболеваний и санация хронических очагов инфекции.
Общая гемостатическая терапия: при кровотечении назначается 5% раствор аминокапроновой кислоты в суточной дозе 200 мг/кг, которую вводят в/в капельно, остальная часть принимается внутрь. В дальнейшем при уменьшении кровоточивости препарат принимают внутрь. Аминокапроновая кислота стимулирует адгезивно-агрегационные свойства тромбоцитов и повышает резистентность сосудистой стенки. Аналогично используется 12,5% раствор дицинона (этамзилат натрия) внутривенно по 2-4 мл, а затем внутрь по 1-2 таблетке 4 раза в день. Дицинон уменьшает тормозящее действие простациклина на агрегацию тромбоцитов. Вместо дицинона может использоваться 0,025% раствор адроксона внутримышечно по 1-2 мл. Для остановки кровотечения применяют внутривенные вливания 10% раствора кальция глюконата по 1-5 мл в зависимости от возраста.
Местная гемостатическая терапия: при носовых кровотечениях закапывают 3% раствор перекиси водорода + смесь растворов тромбина, адроксона и аминокапроновой кислоты (1 амп. тромбина + 50 мл 5% аминокапроновой кислоты + 2 мл 0,025% раствор адроксона). Этот же раствор используется для купирования послеоперационных и маточных кровотечений. При маточных кровотечениях для усиления сократительной способности матки применяют прегнин, а при подтвержденных гормональных нарушениях - эстрогенные препараты внутримышечно: фолликулин (5000-10000 ЕД), синэстрол (2 мл 0,1% раствора).
Неотложная помощь при носовых кровотегениях. Ребенку придается полусидячее положение, с тем чтобы кровь не заглатывалась и свободно изливалась в подставленный лоток, что имеет значение для определения объема кровопотери. На затылок кладут пузырь со льдом, что рефлекторным путем способствует остановке кровотечения. Рекомендуется ввести в носовой ход гемостатическую губку, вату или тампон, смоченный 3% перекисью водорода, прижав его через крыло носа.
При отсутствии эффекта применяют переднюю тампонаду полости носа: марлевым тампоном, смоченным 5% е-аминокапроновой кислотой или перекисью водорода,. последовательно выполняют углубления носовой полости. При неэффективности производят заднюю тампонаду носа. После анестезии кровоточащий участок можно прижечь нитратом серебра.
При непрекращающихся или повторных кровотечениях назначают препараты общего гемостатического действия - внутривенное введение аминокапроновой кислоты в дозе 0,1-0,2 г/кг, внутримышечно 2,5% раствор адроксона по 1 - 2 мл 2-4 раза в сутки, 12,5% раствор дицинона (этамзилата) по 2-4 мл каждые 4-6 ч. При рецидивирующих кровотечениях кроме терапии основного заболевания для профилактики атрофического ринита интраназально применяют масляные растворы. Необходимо гемостазиологическое обследование.
Прогноз. При наследственных тромбоцитопатиях в случаях отсутствия внутричерепных геморрагии для жизни благоприятный, если проводится адекватная терапия и вовремя ликвидируется выраженная кровопотеря. Следует отметить, что массивные внутричерепные геморрагии характерны лишь для очень тяжелых форм тромбастении, болезни Виллебранда и синдрома Бернара-Сулье.
Диспансерное наблюдение больных тромбоцитопатиями
Неполная клинико-лабораторная ремиссия.
- Консультации: педиатр - 1 раз в месяц ЛОР и окулист - 1 раз в год стоматолог - 2 раза в год гематолог - 1-2 раза в месяц, по показаниям - чаще.
- Объем обследования: анализ крови с подсчетом числа тромбоцитов - 1-2 раза в мес анализ мочи - 2-3 раза в год коагулограмма и ретракция кровяного сгустка - 1 раз в месяц коагулограмма и ретракция кровяного сгустка - 1 раз в 3-6 мес и при появлении геморрагического синдрома.
- Объем реабилитации: полноценная витаминизированная (витамины С и РР) диета, режим с ограничением физических нагрузок, без инсоляции. Продолжение начатой в стационаре глюкокортикостероидной терапии, прием симптоматических и сосудоукрепляющих препаратов: аскорутина, препаратов кальция, аминокапроновой кислоты препаратов, улучшающих функциональные свойства тромбоцитов: этамзилат, рибоксин, трентал, АТФ. Фитотерапия: черноплодная рябина, шиповник, пастушья сумка, водяной перец, лист крапивы в течение 10-15 дней каждого месяца. Освобождение от уроков физкультуры и экзаменов. Санация очагов хронической инфекции. Курсы реабилитационной терапии по 3-4 нед 1 раз в 3 мес и в период интеркуррентных заболеваний. Снятие с учета и вакцинация через 5 лет стойкой клинико-лабораторной ремиссии.
Полная клинико-лабораторная ремиссия.
- Консультации: педиатр и гематолог - 1 раз в 3-6 мес ЛОР и стоматолог - 1 раз в год.
- Объем обследования: анализ крови с подсчетом числа тромбоцитов - 1 раз в 3 мес анализ мочи - 1 раз в год коагулограмма и ретракция кровяного сгустка - по показаниям.
- Объем реабилитации: диета витаминизированная, режим свободный по возрасту, занятия физкультурой в подготовительной группе, с 3-го года полной ремиссии - в основной группе. Прием сосудоукрепляющих средств и фитопрепаратов. Оздоровление в местных санаториях.
Курсы реабилитационной терапии длительностью по 3-4 нед весной и осенью и в период интеркуррентных заболеваний.
Первичная профилактика заболевания не разработана, вторичная профилактика рецидивов включает: плановую санацию очагов инфекции предупреждение контактов с больными инфекционными заболеваниями (особенно ОРВИ) дегельминтизацию индивидуальное решение вопроса о проведении профилактических прививок исключение инсоляции, УФО и УВЧ занятия физкультурой в подготовительной группе обязательное исследование крови после любого перенесенного заболевания.
Дискуссии о прекращении приема антикоагулянтных препаратов до и после стоматологических процедур ведутся на протяжении многих лет. Дело в том, что и сторонники, и противники терапии называют весомые доводы в пользу своей позиции. И появление новых препаратов этой группы только еще больше запутало врачей.
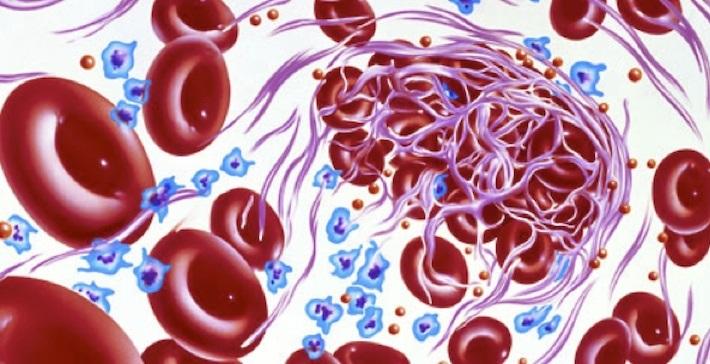
Сторонники соблюдения антикоагулянтной терапии в процессе стоматологического лечения уверены, что отмена препарата ведет к высокой вероятности инсульта, инфаркта миокарда, эмболии легких или глубокого тромбоза вен. Эти осложнения представляют гораздо большую опасность для жизни, чем возможное кровотечение в ходе стоматологического лечения.
Как правило, вероятность травмы крупных кровеносных сосудов во время стоматологической процедуры мала, а значит, невысок риск тяжелых геморрагических осложнений, полагает эта группа врачей. Кроме того, в стоматологическом кабинете есть необходимые средства, чтобы быстро остановить местное кровотечение.
Противники этого подхода убеждены, что даже среднее кровотечение, которое может возникнуть при одновременном удалении нескольких зубов, синус-лифтинге или операции в ротовой полости, может привести к неудовлетворительным результатам процедуры. Кроме того, они считают, что предвидеть опасное кровотечение практически невозможно, и в большинстве стоматологий нет препаратов и инструментов для остановки такого кровотечения.
Сторонники прекращения терапии также заявляют, что вероятность кровотечения у пациентов сильно варьируется, и также может зависеть от одновременного приема других медикаментов. Некоторые медикаменты могут усилить действие антикоагулянтов, что дополнительно повышает вероятность кровотечения в процессе и после процедуры.
Традиционно в качестве антикоагулянта назначают варфарин. Большинство врачей знакомы с этим препаратом и потенциальными кровотечениями, которые он может вызывать. Также известно, что витамин K ослабляет действие варфарина. Для оценки риска кровотечения при ряде процедур у пациентов, принимающих варфарин, используют показатель международного нормализованного отношения (МНО).
В последние годы появилась новая группа оральных антикоагулянтов прямого действия, и многие врачи предпочитают выписывать эти препараты взамен варфарину, в особенности для профилактики коагулопатии у пациентов с фибрилляцией предсердий. Речь идет о следующих медикаментах: дабигатран (Pradaxa), ривароксабан (Xarelto), апиксабан (Eliquis), эдоксабан (Savaysa).
В отличие от варфарина, действие которого заключается в блокировании синтеза витамин K-зависимых факторов, новые препараты действуют напрямую подавляя активированные факторы свертывания крови (фактор 2 – тромбин или фактор Ха – активная форма фактора тромбокиназы). Основное преимущество новых медикаментов в том, что при их приеме не требуется следить за показателем МНО. При этом, оценить риск тяжелого кровотечения у пациента, принимающего такой препарат, сложнее.
Остановить тяжелое кровотечение у пациента, принимающего антикоагулянты прямого действия (ривароксабан, апиксабан, эдоксабан) сложнее, чем у пациента, принимающего варфарин или дабигатран, поскольку у новых медикаментов нет специфического противодействующего вещества, способного блокировать эффект этих антикоагулянтов. По этой причине сторонники и противники терапии не перестают спорить о применении традиционных или новых антикоагулянтов в процессе и после стоматологического лечения.
По результатам двух независимых исследований было установлено, что риск кровотечения в ходе или после стоматологической операции у пациентов, принимающих антикоагулянты прямого действия, минимален. Следовательно, прекращать прием этих медикаментов до и после стоматологическое процедуры не нужно.
Первое исследование было проведено в больнице при Королевском колледже Лондона. В нем приняли участие 82 пациента, принимающих антикоагулянты прямого действия. В ходе эксперимента, пациентам суммарно провели 111 операций по удалению зубов. 35 пациентов (32%) прекратили прием антикоагулянтов, по совету врача, перед и после стоматологической процедурой. У большинства участников не наблюдались кровотечения в ходе стоматологической процедуры. Продолжительные кровотечения наблюдались у 15 пациентов (13,5%), из них 7 пациентам (6,3%) потребовалось принять меры для устранения кровотечения. На основе полученных результатов, авторы работы заключили, что большинство больных, принимающих антикоагулянты прямого действия, могут не прекращать терапию и во время стоматологических процедур.
Второе исследование было проведено в университете Тель-Авива. В нем приняли участие 111 больных, принимающих антикоагулянты прямого действия. 72 участника суммарно прошли 305 стоматологических процедур за 115 посещений. Был отмечен 1 случай «существенного» кровотечения (0,9%) и 6 случаев «небольших» кровотечений (5,2%), которые удалось остановить обычными способами, не прибегая к помощи медикаментов. Таким образом, частота кровотечений составила 6,1%.
На основе полученных результатов, авторы пришли к выводу, что риск кровотечения у пациентов, принимающих антикоагулянты прямого действия, незначителен и не имеет существенных осложнений. Таким образом, нет необходимости прекращать антикоагулянтную терапию при посещении стоматолога, вне зависимости от сложности или продолжительности процедуры.
Несмотря на это многие специалисты продолжают считать, что перед посещением стоматолога необходимо прекратить прием антикоагулянтов, чтобы предотвратить возможные тяжелые кровотечения. Необходимо соотносить эти риски с вероятными опасными последствиями, которые могут возникнуть при временном отказе от антикоагулянтов. Так, больные, прекращающие прием антикоагулянтов, в особенности препаратов прямого действия, подвергают себя неоправданному риску тяжелых осложнений и даже смерти.
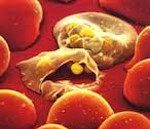
Тромбоцитопатии - группа наследственных и приобретенных нарушений гемостаза, возникающих вследствие качественной неполноценности тромбоцитов при их нормальном количестве. Тромбоцитопатии у детей проявляются склонностью к образованию петехий и гематом при незначительных травмах, кровотечениям (носовым, желудочно-кишечным, маточным) различной степени выраженности, анемией. Выявление тромбоцитопатии у детей требует тщательного лабораторного исследования системы гемостаза, проведения функциональных проб, пункции и исследования костного мозга и др. Лечение тромбоцитопатии у детей проводится детским гематологом и включает общую и местную гемостатическую терапию.
- Классификация тромбоцитопатий
- Причины тромбоцитопатий
- Симптомы тромбоцитопатий
- Диагностика тромбоцитопатий
- Лечение тромбоцитопатий
- Прогноз и профилактика тромбоцитопатии
- Цены на лечение
Общие сведения
Тромбоцитопатии – геморрагические диатезы, развивающиеся в результате нарушения первичного тромбоцитарного звена гемостаза. Популяционная частота тромбоцитопатий достигает 5-10%. Наследственные тромбоцитопатии являются наиболее частой причиной кровотечений неясного генеза у детей; на их долю приходится от 36 до 65%. Тромбоцитопатии представляют собой актуальную проблему для педиатрии и детской гематологии, поскольку их распространенность зачастую недооценивается, и многие дети с геморрагическим синдромом длительно и безуспешно лечатся у специалистов узкого профиля – детских отоларингологов, детских гинекологов, детских стоматологов, детских гастроэнтерологов, детских урологов.

Классификация тромбоцитопатий
Тромбоцитопатии объединяют в себе гетерогенную группу заболеваний, которые могут быть поделены на наследственные (врожденные) и приобретенные (симптоматические).
1. Наследственные тромбоцитопатии:
- с нарушением агрегационной функции тромбоцитов - дизагрегационные тромбоцитопатии (эссенциальная атромбия 1 типа, тромбастения Гланцмана, аномалия Пирсона-Стоба, аномалия Мея-Хегглина и др.)
- с дефектом реакции освобождения (эссенциальная атромбия 2 типа, аспириноподобный синдром и др.)
- с недостаточным хранением гранул и их компонентов (синдром «серых тромбоцитов», синдром Хержманского-Пудлака)
- с нарушением адгезии тромбоцитов (болезнь Виллебранда, макроцитарная тромбоцитодистрофия Бернара-Сулье)
- тромбоцитопатии, сочетающиеся с различными врожденными дефектами (врожденными пороками сердца, гликогенозами, синдромом Марфана, Элерса-Данлоса, Вискотта-Олдрича и др.)
2. Приобретенные тромбоцитопатии, развивающиеся в течение жизни на фоне других заболеваний.
В детском возрасте наследственные тромбоцитопатии встречаются в 3 раза чаще, чем приобретенные.
Причины тромбоцитопатий
Первичный тромбоцитарно-сосудистый гемостаз включает в себя ряд последовательных реакций: адгезии, агрегации, ретракции кровяного сгустка и активации плазменного гемостаза.
При повреждении кровеносного сосуда под воздействием главного стимулятора адгезии – коллагена эндотелия, тромбоциты набухают и приклеиваются к стенке сосуда. В реализации этапа первичного гемостаза участвуют ионы Ca, белок эндотелия - фактор Виллебранда и контактирующий с ним мембранный гликопротеин Ib тромбоцитов. Вслед за адгезией начинается фаза агрегации, в процессе которой происходит быстрое увеличение тромба. В эту фазу выделяются биологически активные вещества (тромбин, аденозинфосфат (АДФ), катехоламины, серотонин и мн. др.), вызывающие вазоконстрикцию и усиливающие адгезию и агрегацию тромбоцитов. Под влиянием происходящих процессов рыхлая тромбоцитарная пробка уплотняется и подвергается ретракции – сокращению с самопроизвольным отделением сыворотки от сгустка.
Причиной наследственных тромбоцитопатий выступают дефекты генов, кодирующих те или иные факторы, принимающие участие в обеспечении тромбоцитарно-сосудистого гемостаза. Врожденные тромбоцитопатии могут наследоваться по аутосомно-доминантному или аутосомно-рецессивному типу.
Функциональная неполноценность тромбоцитов при приобретенных тромбоцитопатиях может быть связана с приемом тромбоцитоактивных лекарственных препаратов (НПВС, аспирина, пенициллинов, антикоагулянтов и др.), В12-дефицитной анемией, ДВС-синдромом, лейкозом, циррозом печени, геморрагическим васкулитом, системной красной волчанкой, диффузным гломерулонефритом, почечной недостаточностью, гигантскими ангиомами, тромбозами, массивными гемотрансфузиями, лучевой болезнью и пр.
Симптомы тромбоцитопатий
Диапазон проявлений тромбоцитопатии у детей очень широк. Клиническая манифестация врожденной тромбоцитопатии может быть связана с перинатальной патологией (ацидозом, гипоксией), родовыми травмами, вирусными или бактериальными инфекциями, сепсисом, гиповитаминозом, инсоляцией, проведением физиотерапевтических процедур (УФО, УВЧ), массажа, прививки и др.
Ведущим в клинике различных форм тромбоцитопатии является рецидивирующий геморрагический синдром, тяжесть которого может варьировать от легкой кровоточивости до обильных кровотечений. У новорожденных тромбоцитопатия может проявляться кефалогематомами, внутричерепными кровоизлияниями, кровоточивостью и медленным заживлением пупочной ранки. Кровотечения микроциркулярного типа характеризуются петехиями, экхимозами, возникающими при незначительных травмах, трении тела одеждой. В отличие от гемофилии, для тромбоцитопатии не характерны гемартрозы и межмышечные гематомы.
При тромбоцтопатиях у детей раннего возраста отмечаются кровотечения при прорезывании зубов, рецидивирующие носовые кровотечения, повышенная кровоточивость десен, длительное заживление мелких повреждений. У девочек-подростков часто имеется «семейная» склонность к меноррагиям, ювенильным дисфункциональным маточным кровотечениям. У пациентов с тромбоцитопатиями даже малые хирургические вмешательства (удаление зуба, тонзиллэктомия и др.) сопровождаются обильными и длительными кровотечениями. Реже в клинике тромбоцитопатий встречаются желудочно-кишечные кровотечения, гематурия, кровоизлияния в склеры.
Вследствие повышенной кровопотери у детей с тромбоцитопатиями развивается анемический синдром, характеризующийся общей слабостью, бледностью кожных покровов, головокружениями, одышкой, тахикардией, артериальной гипотонией, склонностью к обморокам.
При сочетании тромбоцитопатии с дисплазией соединительной ткани у детей выявляются нарушения осанки, плоскостопие, нефроптоз, пролапс митрального клапана и др. аномалии развития.
Диагностика тромбоцитопатий
Как показывает практика, диагноз тромбоцитопатии у детей редко устанавливается своевременно. Участковые педиатры, как правило, не придают должного значения геморрагическим проявлениям и направляют детей к узким специалистам: детскому ЛОРу – при носовых кровотечениях; детскому гинекологу – при обильных менструациях; детскому стоматологу – при кровоточивости десен и т. д. Между тем, дети с тромбоцитопатиями нуждаются в как можно более ранней специализированной консультации гематолога для уточнения диагноза и формы тробоцитопатии.
Диагностика тромбоцитопатии включает несколько этапов, главными из которых являются анализ клинических проявлений и семейного анамнеза, углубленное исследование системы гемостаза. Функциональные эндотелиальные пробы (баночная, манжеточная, щипковая, проба жгута) при тромбоцитопатиях, как правило, положительные: на коже, в месте воздействия остаются многочисленные петехии или кровоподтек.
Лабораторный этап диагностики тромбоцитопатии начинается с клинического анализа крови, определения времени кровотечения, показателей коагулограммы. В процессе диагностического поиска тромбоцитопатии проводится определение количества тромбоцитов и тромбоцитарной формулы, изучение их морфометрических характеристик и функции (адгезивности; агрегационной активности тромбоцитов с АДФ, ристомицином, адреналином, тромбином, коллагеном; определение тромбоцитарных факторов свертывания и др.). Лабораторное обследование ребенка с тромбоцитопатией должно выполняться не менее 3-х раз в разные периоды заболевания (во время клинической ремиссии и в момент геморрагических проявлений).
Для оценки функции кроветворения в некоторых случаях назначается проведение стернальной пункции или трепанобиопсии и исследование миелограммы.
Лечение тромбоцитопатий
При наследственных тромбоцитопатиях проведение этиотропного лечения невозможно. Поэтому весь комплекс терапевтических мероприятий делится на неотложную терапию по купированию геморрагического синдрома и профилактическое лечение. В течение всей жизни пациентам с тромбоцитопатией запрещается употребление уксуса с пищей (в т. ч. в консервах), алкоголя. Рекомендуется обогащение рациона продуктами, богатыми витаминами А, С и Р; арахисом.
Медикаментозная терапия тромбоцитопатии проводится гемостатическими средствами (этамзилат натрия, адроксон, кальция глюконат, аминокапроновая кислота и др.), препаратами метаболического действия (инозин, АТФ, оротат калия, фолиевая кислота). Полезно употребление кровоостанавливающих фитосборов. Плановые профилактические курсы лечения тромбоцитопатии рекомендуется проводить 2-4 раза в год в зависимости от тяжести геморрагического синдрома.
Для локальной остановки кровотечений из поверхностных ран используется орошение кровоточащей поверхности охлажденным раствором аминокапроновой кислоты, нанесение адроксона, аппликации фибринной пленки с тромбином. При носовом кровотечении необходимо ведение в носовые ходы гемостатической губки, проведение анемизации слизистой носа. При маточных кровотечениях применяются препараты, усиливающие сокращение матки (этистерон), внутривенное введение аминокапроновой кислоты; РДВ полости матки при тромбоцитопатии должно проводится под прикрытием гемостатической терапии. При массивной кровопотере может потребоваться переливание эритроцитарной массы, тромбоцитов и плазмы.
При симптоматической тромбоцитопатии необходимо проведение лечения основного заболевания, исключение приема тромбоцитоактивных препаратов и других провоцирующих моментов.
Прогноз и профилактика тромбоцитопатии
Своевременное выявление тромбоцитопатии у ребенка и проведение адекватной профилактической терапии позволяет предупредить выраженную кровопотерю и повысить качество жизни. При массивных внутричерепных геморрагиях, сопровождающих течение некоторых форм тромоцитопатии, прогноз для жизни неблагоприятный.
Мерами профилактики тромбоцитопатий служат медико-генетическое консультирование семей с наследуемым геморрагическим синдромом, отказ от бесконтрольного приема медикаментов. Дети с установленным диагнозом тромбоцитопатии должны находиться на диспансерном учете у педиатра, детского гематолога, детского офтальмолога, ЛОРа, стоматолога; регулярно проходить полное лабораторное обследование, получать превентивное лечение, исключить занятия травмоопасными видами спорта. Вопрос о проведении профилактической вакцинации детей решается в индивидуальном порядке.
- Издательство «Медиа Сфера»
- Об издательстве
- Рекламодателям
- Доставка / Оплата
- Контакты
Кафедра челюстно-лицевой травматологии стоматологического факультета ГБОУ ВПО "Московский государственный медико-стоматологический университет им. А.И. Евдокимова" Минздрава России
ГБОУ ВПО "Северо-Западный государственный медицинский университет им. И.И. Мечникова", Санкт-Петербург
Особенности удаления ретинированных зубов у гематологических больных
Журнал: Стоматология. 2019;98(6): 121-123
Шинкевич Д. С., Афанасьев В. В. Особенности удаления ретинированных зубов у гематологических больных. Стоматология. 2019;98(6):121-123. https://doi.org/10.17116/stomat201998061121
Кафедра челюстно-лицевой травматологии стоматологического факультета ГБОУ ВПО "Московский государственный медико-стоматологический университет им. А.И. Евдокимова" Минздрава России





Операция сложного удаления зубов у больных с геморрагическим синдромом является трудной задачей. Авторы разработали метод сложного удаления зубов при их ретенции у больных с геморрагическим синдромом. В ходе исследования установлено, что предложенный метод позволил снизить риск развития геморрагических осложнений и оптимизировать заживление постэкстракционных ран. Всего осуществлено 11 операций сложного удаления зубов по поводу их ретенции и затрудненного прорезывания. Представлены достоинства и недостатки метода.
Кафедра челюстно-лицевой травматологии стоматологического факультета ГБОУ ВПО "Московский государственный медико-стоматологический университет им. А.И. Евдокимова" Минздрава России
ГБОУ ВПО "Северо-Западный государственный медицинский университет им. И.И. Мечникова", Санкт-Петербург
Операция удаления зуба является наиболее распространенной у больных с заболеваниями крови. Экстракция зубов у таких больных часто сопровождается длительными луночковыми кровотечениями с образованием гематом, которые могут преобразовываться в кистозные псевдоопухоли и вызывать деструкцию челюсти [1]. Кроме того, гематомы могут распространяться в мягкие ткани челюстно-лицевой области (ЧЛО) и шеи, а также приводить к стенозу верхних дыхательных путей и асфиксии [2].
Удаление зубов при геморрагическом синдроме вызывает необходимость сотрудничества стоматолога и гематолога [3]. Специалист-гематолог осуществляет общий гемостаз в дооперационном, интра- и послеоперационном периодах, а хирург-стоматолог обеспечивает местный гемостаз, который заключается в формировании и защите сгустка крови. Для местного гемостаза можно использовать пропитанный транексамовой кислотой марлевый тампон (на 30—60 мин) и др. [4, 5].
В настоящее время методика операции простого удаления зуба у гематологических больных хорошо разработана. Однако в отечественной и зарубежной литературе недостаточно освещена проблема сложного удаления зубов при их дистопии и ретенции. В связи с этим была проведена настоящая работа.
Цель исследования — повышение эффективности и безопасности оказания хирургической стоматологической помощи гематологическим больным с дистопией и ретенцией зубов путем усовершенствования методики их удаления.
Материал и методы
Под нашим наблюдением находились 12 больных, у которых диагностировали нарушение прорезывания различных групп зубов, что составило 6% от общего числа пациентов, страдавших следующими гематологическими заболеваниями: лимфома (Л) — 1 больной, апластическая анемия — 2, гемофилия (Г) — 6, болезнь Виллебранда — 2, и 1 больная с идиопатической тромбоцитопенической пурпурой.
Результаты
Затрудненное прорезывание зуба мудрости наблюдали наиболее часто — 11 случаев, редко — других зубов (у 2 больных). На нижней челюсти было 11 ретинированных зубов, на верхней — 2 зуба.
На всех зубах отмечали наличие кариозных полостей, что свидетельствовало о длительном их существовании с момента прорезывания и несвоевременном лечении. Клиническая картина у больных в основном не отличалась от таковой у пациентов без патологии крови, однако у 1 больного с гемофилией неоднократно возникало интенсивное кровотечение из кариозной полости и из-под десны, покрывавшей частично прорезавшийся зуб.
Обратились к стоматологу с направлением ортодонта 2 больных, остальные обратились в клинику в связи с развитием затрудненного прорезывания зуба.
Таким образом, наиболее частым показанием к удалению зуба у гематологических больных был перикоронит.
Оперативные вмешательства у всех больных проводили под местной анестезией в условиях стационара Национального медицинского исследовательского центра гематологии МЗ Р.Ф. Всего осуществили 11 операций сложного удаления ретинированных зубов на нижней челюсти по общепринятой методике. При этом модифицировали направление линии разреза: разрез слизистой оболочки выполняли в нижней трети крыловидно-нижнечелюстной складки, продолжая его над проекцией ретинированного зуба в ретромолярной области. Далее гладилкой отслаивали круговую связку впереди стоящего 2-го моляра на всем ее протяжении с вестибулярной стороны (см. рисунок, 
Схематическое обозначение направления разреза слизистой оболочки (а) и отведенного слизисто-надкостничного лоскута (б). а и далее). Разрез к переходной складке не делали. Таким образом, мы уменьшали площадь лоскута и кровоточащих тканей во время операции. Малая длина разреза приводила к плохой мобильности образовавшегося слизисто-надкостничного лоскута, что вынуждало врача оказывать большое давление крючком на ткани при его отведении, приводило к дополнительному сдавливало кровоточащих сосудов и способствовало прекращению кровотечения во время операции (см. рисунок, б).
С помощью бора удаляли костную ткань вокруг зуба и его извлекали. Особое внимание обращали на острые края кости, которые тщательно фрезеровали и сглаживали для предотвращения травмы мягких тканей с внутренней стороны лоскута. Стенки образовавшейся после извлечения зуба полости сдавливали тупым инструментом (возможно кусачками), разрушая и деформируя гаверсовы каналы для профилактики вторичного костного кровотечения. Слизисто-надкостничный лоскут возвращали на место и фиксировали швами. Иммобилизацию лоскута не проводили, чтобы избежать травмы надкостницы. В случае развития интраоперационного кровотечения рану зашивали наглухо. Если это не удавалось, сближали края раны швами, насколько было возможно, а лунку тампонировали марлевой йодсодержащей турундой.
У 2 больных с апластической анемией после удаления зубов мудрости лунки не тампонировали, так как интраоперационного кровотечения у них не было, и отмечена полная остановка кровотечения.
Сближающие швы на рану накладывали у 10 (из 12) больных, у 2 больных лечение проводили под турундой.
У 1 больного с перикоронитом зуба 4.8 диагностировали В-крупноклеточную лимфому с поражением поднижнечелюстных лимфатических узлов, мягкого неба и печени. Этот пациент находился в состоянии глубокой трехростковой цитопении, и ему проводился курс полихимиотерапии. В условиях резкого снижения иммунитета и высокого риска диссеминации гнойного процесса удаление зуба было нецелесообразно. Больному ежедневно обрабатывали патологический карман растворами антисептиков, проводили антибиотико- и десенсибилизирующую терапию.
Для предотвращения кровотечения проводили по мере выраженности геморрагического синдрома общую заместительную гемостатическую терапию (ОЗГТ) в пред- и постоперационном периодах. Так, 1 больному с легкой формой гемофилии, 5 больным с тяжелой формой гемофилии и 1 больному с болезнью Виллебранда вводили препараты рекомбинантных VIII и IX факторов свертывания крови. Одной больной с апластической анемией перед операцией вводили тромбоконцентрат. Дозы и кратность введения препаратов рассчитывали, а само введение осуществляли под контролем гематолога. Таким образом, ОЗГТ получили 8 (73%) из 11 прооперированных больных, 3 больных в гемостатической терапии не нуждались. У 1 больной с апластической анемией, у которой диагностировали ретенцию и дистопию зуба 4.8, при мониторинге системы крови (общий анализ крови, коагулограмма) уровень тромбоцитов в крови был 57,00·10 9 /л, что, по нашему мнению, являлось допустимым для экстренного оперативного вмешательства без предварительной ОЗГТ. По этой же причине не проводили ОЗГТ и у больной с идиопатической тромбоцитопенической пурпурой с ретенцией и дистопией зубов 1.3, 2.3, хроническим периодонтитом зубов 2.7, 2.8. У этой больной уровень тромбоцитов держался около 87,00·10 9 /л.
У больной с болезнью Виллебранда и ретенцией зуба 4.8 уровень фактора Виллебранда в предоперационной коагулограмме составил 92%, что является нормой.
Развитие гематомы мягких тканей лица в послеоперационном периоде наблюдали у 2 больных. У 1 из них с тяжелой формой гемофилии после удаления зуба 4.8 в 1-е сутки после операции сформировалась ограниченная гематома щеки, которая сочеталась с наружным кровотечением. Протекала в основном бессимптомно, однако больной отмечал неудобство при закрывании рта. Гематома возникла в результате неэффективной послеоперационной ОЗГТ, после ее коррекции гематома резорбировалась на 4-е стуки после возникновения.
У больной с идиопатической тромбоцитопенической пурпурой после удаления ретинированных зубов 1.3 и 2.3, а также корней зубов 2.7, 2.8 в 1-е сутки развилась гематома, распространявшаяся в обе подглазничные области, верхнюю губу и спускавшаяся на губоподбородочные складки с обеих сторон. Больной не проводили ОЗГТ в пред- и постоперационном периодах, так как показатели свертывающей системы крови были в пределах рефренсных значений. Мы полагаем, что образование гематомы было вызвано травмой тканей при проведении двусторонней инфраорбитальной анестезии. Гематома резорбировалась самостоятельно на 22-е сутки после возникновения.
В обоих случаях для ликвидации гематом мы не использовали физиопроцедуры, рассасывающие мази, механический массаж, так как считали, что сосудорасширяющее воздействие в условиях повышенной васкуляризации ЧЛО у больных с коагулопатиями может привести к бурному увеличению и распространению гематомы.
Больной с болезнью Виллебранда после удаления ретинированного зуба 4.8 по его просьбе был выписан из стационара на следующие сутки после операции. Пациент проводил послеоперационную общую заместительную гемостатическую терапию самостоятельно в домашних условиях, которую прекратил на 5-е сутки после операции. Самостоятельно перешел на употребление жесткой пищи, в результате чего на 7-е сутки из послеоперационной раны развилось кровотечение. Возобновление ОЗГТ эффекта не дало. Больной вновь обратился в НМИЦ МЗ РФ, где ему тампонировали послеоперационную рану марлевой турундой с аквазаном и скорректировали ОЗГТ под контролем гематолога. После предпринятых мер кровотечение прекратилось.
Таким образом, снижение дозы, увеличение кратности или полная отмена ОЗГТ приводили к развитию вторичного кровотечения. Окончательная эпителизация послеоперационной раны наступала в среднем на 19,0±7,0-е сутки. Швы снимали на 10,1±1,0-е сутки, что было примерно на 1 нед раньше, чем наступала окончательная эпителизация раны. Показаниями к снятию швов служили формирование устойчивого рубца, отсутствие кровотечения. Кроме того, случай с пациентом с болезнью Виллебранда показал, что даже после малоинвазивной операции (удаление ретинированных моляров на нижней челюсти) пациенты с выраженным геморрагическим синдромом (гемофилия, болезнь Виллебранда, идиопатическая тромбоцитопеническая пурпура, апластическая анемия) до конца раннего послеоперационного периода (до снятия швов) должны находиться в стационаре под контролем хирурга-стоматолога и гематолога.
Выводы
1. Проведение общей заместительной гемостатической терапии в пред- и постоперационном периодах у больных с патологией свертывающей системы крови является обязательным.
2. Для профилактики кровотечения из кости после удаления ретинированного зуба эффективно сдавливание стенок полости тупым инструментом (возможно костными кусачками) или зашлифовывание их бором с целью деформации гаверсовых каналов.
3. Интенсивное вторичное кровотечение в раннем послеоперационном периоде у больных с патологией крови может сдерживать процесс окончательной эпителизации раны более чем на 1 мес.
3. Хирургическое лечение гематологических больных с патологией прорезывания зубов следует проводить в стационаре совместно со специалистом-гематологом.
Авторы заявляют об отсутствии конфликта интересов.
The authors declare no conflicts of interest.
Ранее сообщалось, что накопительный эффект острых и хронических форм поражений полости рта в результате химио- и радиотерапии провоцирует развитие осложненных стоматологических патологий. В данной статье рассмотрены аспекты стоматологического лечения онкологических пациентов до, во время и после соответствующей противораковой терапии.
Рак представляет собой одно из наиболее сложных для лечения заболеваний, поскольку характеризуется неконтролируемым ростом тканей и наличием дисбаланса между процессами деления и апоптоза клеток. Большинство побочных эффектов химио- и радиотерапии могут быть вызваны токсическим воздействием на специфический орган или нарушением процесса деления нормальных клеток в структуре пораженного органа.
Ниже перечислены побочные эффекты химиотерапевтических агентов, используемых для лечения рака.
- Супрессия костного мозга:
- лейкопения;
- тромбоцитопения;
- анемия;
- повышение восприимчивости к инфекциям;
- увеличение частоты развития вторично злокачественных поражений;
- Поражения желудочно-кишечного тракта:
- тошнота;
- рвота;
- диарея;
- мукозит;
- Поражения кожи:
- эритема;
- макулопапулезная сыпь;
- эксфолиативный дерматит;
- алопеция;
- гиперпигментация;
- светочувствительность;
- Необратимая кардиомиопатия.
- Токсичное поражение легких.
- Гепатотоксичный эффект.
- Токсичное поражение почек.
- Нейротоксические эффекты по типу боли, периферической невропатии, судорог.
- Подавление сперматогенеза, оогенеза и менструального цикла.
- Поражения полости рта:
- мукозит;
- инфекционные поражения (бактериальные, вирусные, грибковые);
- кровотечения;
- ксеростомия.
Профилактика и терапевтическое лечение перед началом проведения противоопухолевой терапии
Перед началом каких-либо манипуляций, направленных на лечение рака, рекомендована предварительная диагностика состояния полости рта с целью:
- предупредить дальнейшее развитие заболеваний, которые могут обостриться во время терапии рака;
- получить данные об исходном состоянии полости рта, которые в дальнейшем будут использоваться в ходе мониторинга и анализа эффекта действия радио- и химиотерапии;
- своевременно выявить метастазы;
- минимизировать уровень дискомфорта в полости рта пациента в ходе противоопухолевой терапии.
Все пациенты с неопластическими поражениями, получающие химиотерапию, должны пройти тщательную стоматологическую диагностику, которая включает клинический осмотр и рентгенографическое исследование. Перед началом химиотерапии пациент должен быть проинструктирован и надлежащим образом мотивирован для осуществления гигиены полости рта.
В случае химиотерапии области головы и шеи нужно обязательно учесть следующие рекомендации:
- пародонтально или структурно скомпрометированные зубы подлежат удалению;
- зубы, связанные с абсцессами челюстно-лицевой области, также нужно удалять или лечить посредством эндодонтического вмешательства;
- все хирургические процедуры должны быть завершены не менее чем за 10—12 дней до начала развития нейтропении;
- желательно в полном объеме провести необходимое стоматологическое лечение, направленное на восстановление зубов, пораженных кариесом или патологической стираемостью, замену дефектных реставраций, удаление плохо фиксированных ортопедических конструкций и ортодонтических дуг;
- имеющиеся протезы следует тщательно очищать и ежедневно обрабатывать нистатином с целью профилактики развития грибковых поражений;
- у детей необходимо провести удаление подвижных молочных зубов, а также тех зубов, которые, вероятно, не удастся спасти после проведения химио- и радиотерапии, с учетом времени, необходимого для заживления лунок перед началом противоопухолевой терапии.
Рекомендации по удалению зубов у пациентов, которые планируют проходить процедуры радио- или химиотерапии
- Процедура экстракции должна быть минимально инвазивной и выполняться за 2, а лучше — за 3 недели до начала радиотерапии.
- На верхней челюсти экстракцию зубов следует проводить не менее чем за 5 дней до начала химиотерапии. На нижней челюсти — не менее чем за 7 дней.
Во избежание ранений слизистой оболочки полости рта острыми краями лунки следует сглаживать их сразу же после экстракции.
Необходимо обеспечить первичное закрытие раны.
Следует избегать внесения гемостатических препаратов внутрь лунки, поскольку в дальнейшем они могут стать очагом развития инфекции.
Если количество тромбоцитов менее 50 000 ед./мм3, процедура переливания крови обязательна.
Проведение экстракции следует отсрочить, если количество тромбоцитов в крови составляет менее 2000 ед./мм3 или же количество нейтрофилов менее 1000 ед./мм3. В качестве альтернативного подхода можно провести удаление зубов с обязательным назначением антибиотиков.
Пациенты, которые хотят сохранить собственные зубы, должны быть проинформированы о возможном развитии гипосаливации, повышении риска развития инфекционных поражений по типу кариеса или остеонекроза, ассоциированных именно с эффектом химио- и радиотерапии.
Уход за полостью рта во время химиотерапии
С самого начала химиотерапии следует уделять особое внимание надлежащей гигиене полости рта с целью минимизации риска развития возможных осложнений. На сегодняшний день не существует общепринятых протоколов профилактики и лечения мукозита, индуцированного проведением химиотерапии.
Полоскания полости рта физиологическим или бикарбонатным растворами способствуют купированию симптомов мукозита, удалению зубного налета, разбавлению кислот и токсинов в среде полости рта. Некоторые коммерчески доступные ополаскиватели, например перекись водорода, могут негативно воздействовать на полость рта при наличии мукозита, поэтому использование таковых пациентами должно быть прекращено.
Учитывая повышенную вероятность инфицирования полости рта во время прохождения химиотерапии и повышение кровоточивости мягких тканей, пациентам рекомендуется проводить чистку зубов 2—3 раза в день.
Пациенты, которые подвергаются общему облучению тела или химиотерапии, также имеют вероятность развития тромбоцитопении. Кровоточивость слизистой оболочки полости рта обычно развивается при количестве тромбоцитов менее 5000 ед./мм3. Для контроля кровотечения могут быть использованы местные средства, например давящая желатиновая губка с тромбином или микрофибриллярным коллагеном, а также антифибринолитические вещества в мягкой капе. Если подобные вмешательства не дают желаемого эффекта, необходимо рассмотреть возможность переливания тромбоцитов.
Стоматолог-хирург должен быть осведомлен о количестве лейкоцитов и тромбоцитов в крови пациента, проходящего химио- или радиотерапию, еще перед началом лечения. Если количество тромбоцитов выше 50 000 ед./мм3, пациенту можно выполнять большинство рутинных стоматологических манипуляций, однако, если уровень тромбоцитов ниже указанной цифры, нужно обязательно проконсультироваться с онкологом. В случае необходимости выполнения инвазивных стоматологических вмешательств следует рассмотреть возможность переливания крови или тромбоцитарного концентрата. Если же количество тромбоцитов менее 2000 ед./мм3, рекомендуется назначить антибиотикопрофилактику и консультацию с лечащим врачом.
Кроме того, пациентам необходимо рекомендовать:
- Пить много воды и других жидкостей, кроме кофе и чая.
- В ходе проведения радиотерапии и после нее зубы могут стать гиперчувствительными, что может быть связано с уменьшением секреции слюны и снижением ее рН. Местное применение фторидного геля позволяет купировать симптомы гиперчувствительности.
- Радиотерапия области головы и шеи может спровоцировать повреждение сосудов мышц, вызвать тризм жевательных мышц и суставной капсулы. Чтобы свести к минимуму влияние излучения на мышцы челюстно-лицевой области, при внешнем облучении необходимо использовать специальные защитные капы. Пациент также должен выполнять упражнения для растяжки мышц по крайней мере 3—4 раза в день.
- В течение первых 6 месяцев после завершения лучевой терапии пациентам следует избегать использования протезов.
- Установка дентальных имплантатов может проводиться через полтора года после лучевой терапии с учетом состояния тканей ротовой полости, уровня их васкуляризации и возможного прогноза заживления.
Профилактика является лучшим методом лечения кровоточивости мягких тканей в ротовой полости. Когда количество тромбоцитов невелико (например, Уход за пациентами после химиотерапии
Период после химиотерапии наиболее подходит для проведения большинства стоматологических процедур. Уход за полостью рта должен включать ежедневную чистку зубов мягкими щетками. Промывание полости рта физиологическим или бикарбонатным растворами, применение лубрикантов и поверхностной анестезии, а также полоскания хлоргексидином следует продолжать, чтобы предотвратить развитие инфекционных поражений и облегчить остаточные симптомы ксеростомии. Применение фтора и консультации по поводу коррекции диеты также полезны в программе профилактики развития кариеса, индуцированного эффектом ксеростомии.
Мониторинг за пациентами после противораковой терапии следует проводить по нескольким причинам:
- пациент с онкопатологией находится в группе риска развития дополнительных поражений;
- вероятность развития скрытых метастазов;
- вероятность рецидива первичных поражений;
- риск развития осложнений, связанных с терапией.
Лечение мукозита может проводиться посредством выполнения пациентом следующих рекомендаций:
- Умеренные полоскания полости рта (раствор соль + сода).
- Местные анестетики (лидокаин 5%) и антигистаминные растворы (бензидамин хлорид).
- Противомикробные полоскания, например полоскания хлоргексидином.
- Применение противовоспалительных средств: жидкость «Камилосан» (водно-спиртовой экстракт ромашки) или стероидные препараты местного действия (дексаметазон).
- Адекватное увлажнение полости рта.
- Применение пероральных лубрикантов.
- Увлажнение воздуха.
Если у пациента после химиотерапии развилась определенная форма иммуносупрессии, а количество лейкоцитов менее 2000 ед./мм3, иммунная система не в состоянии самостоятельно побороть большинство инфекций. Кроме того, у пациентов после химио- или радиотерапии часто отмечается уменьшение саливации и развитие оппортунистических инфекций. При кандидозном поражении слизистой следует использовать противогрибковые препараты (по типу нистатина).
Остеорадионекроз после лучевой терапии
Остеорадионекроз — патологическое состояние, характеризующееся обнажением костной ткани, участки которой не в состоянии регенерировать после значительной дозы облучения. Протоколы для снижения риска развития остеорадионекроза включают в себя адекватный выбор эндодонтического лечения вместо экстракции зубов, использование нелидокаиновых местных анестетиков без содержания адреналина или же с очень низкой его концентрацией, профилактический прием антибиотиков, а также их использование после операционного вмешательства в течение двух недель, применение гипербарической оксигенации перед началом инвазивных процедур.
На ранних стадиях развития некроза показано консервативное лечение. Обнаженную кость можно промыть физиологическим раствором или раствором антибиотика, также пациенты должны быть проинформированы о необходимости промывания пораженной области при помощи ирригатора. При образовании костного секвестра его сразу следует удалить для обеспечения процесса эпителизации.
Перевод: Мирослав Гончарук-Хомин, Юлия Девятко
Читайте также:

