При недостатке витамина в1 развивается цинга расстройство деятельности нервной системы рахит
Опубликовано: 29.04.2024
В дополнение к недостаткам диеты, действие витаминов в промежуточном метаболизме может быть нарушено аномально высокими потребностями, которые могут быть обусловлены питанием (например, избыток углеводов увеличивает потребность в витаминах группы В) или влиянием ингибирующих частиц, или повреждением белковой конфигурации апофермента, что также приводит к существенному повышению потребностей в витаминах. Некоторые врожденные дефекты метаболизма можно скорректировать при помощи больших доз конкретных витаминов.
а) Нарушения нервной системы при дефиците тиамина (витамина В 1 ). Тиамин играет важную роль в декарбоксилировании пирувата и альфа-кетоглутарата, двух ступеней цикла Кребса и в преобразовании 5-углеводных и 6-углеводных сахаров с помощью фермента транскетолазы. Следовательно, дефицит тиамина снижает объем доступной энергии в мозге и повышает концентрацию двух кетоновых кислот.
Клинические проявления дефицита тиамина различаются. Классический бери-бери, наблюдаемый в Азии и Африке, характерен внезапно начинающейся слабостью, вызываемой острой периферической нейропатией, ригидностью затылочных мышц, афонией и сердечной недостаточностью. В развитых странах случаи энцефалопатии Вернике иногда наблюдаются при парентеральном питании (Barrett et al., 1993), диализе (Jagadha et al., 1987), в случае злокачественных или истощающих заболеваний при обогащенном (насыщенном) углеводами питании (Pihko et al., 1989) и при противораковой химиотерапии (Vanhulle et al., 1997).
Клиническая картина значительно варьирует от внезапного коллапса и смерти до хронических познавательных нарушений, через классическую картину острой атаксии (Ogunlesi, 2004), общего беспокойства и зрительных нарушений. Диагноз часто пропускается, и он обязательно должен учитываться при соответствующих признаках, поскольку энцефалопатия Вернике является предотвратимой причиной смерти (Pihko et al., 1989; Barrett et al., 1993). Нейровизуализация может помочь, если выявляет участки пониженной плотности с контрастным усилением в паравентрикулярной области в таламусе с обеих сторон и вдоль водопровода мозга. МРТ точнее выявляет области с низкой интенсивностью (Weidauer et al., 2003).
Диффузионно-взвешенная MPT целесообразна при отрицательном результате МРТ в обычных режимах, отражая повышенную диффузию в тех же областях (Halavaara et al, 2003). У пациентов с парентеральным питанием наблюдалось необычное расположение геморрагических повреждений в верхнем черве мозжечка и нижних отделах ствола мозга без вовлечения сосцевидных тел (Vortmeyer et al, 1992). Это состояние может возникать даже у детей, получающих стандартные дозы витамина В1, если потребность повышена при употреблении углеводов. Лечение проводится внутривенным введением больших доз тиамина. Состояние необходимо отличать от болезни Ли, которая не поражает сосцевидные тела в большинстве случаев, в отличие от практически постоянного вовлечения при дефиците тиамина. Дефицит тиамина может способствовать развитию эпилептических судорог у пациентов со скрытой предрасположенностью (Кеуser и DeBruijn, 1991).
б) Нервная система при дефициет пиридоксина (витамина В6) и зависимость от пиридорксина. Витамин В6 в его форме производной альдегида пиридоксаль-5-фосфат необходим для правильного функционирования ЦНС. В частности, он требуется для декарбоксилирования глютаминовой кислоты до ГАМК, обязательного тормозящего нейротрансмиттера в коре мозга.
Дефицит пиридоксина отвечает за повышенную возбудимость головного мозга и судороги. Это наблюдалось на протяжении первого года жизни новорожденных, получавших менее 0,1 мг/день порошкового козьего молока (Johnson, 1982). Реже дефицит пиридоксина может развиваться при анастомозе тощей кишки или при лечении препаратами группы гидразидов, такими как изониазид или пеницилламин. В таких случаях, тем не менее, более часта периферическая нейропатия, чем судороги.
Пиридоксиновая зависимость является редким семейным заболеванием с аутосомно-рецессивным наследованием, характеризующимся тяжелыми или повторными судорогами, обычно вскоре после рождения и часто внутриутробно (Haenggeli et al., 1991; Gospe и Hecht, 1998). Неврологические и общие проявления, такие как вздутие живота, рвота и энцефалопатические проявления являются частыми, поэтому уместнее определение пиридоксин-зависимая энцефалопатия, создающая дифференциально-диагностическую проблему с гипоксически-ишемической энцефалопатией (Baxter et al., 1996). При нейровизуализации можно выявить прогрессирующее расширение желудочков или патологию белого вещества (Gospe и Hecht, 1998; Baxter, 2001). Диагноз ранее основывался на назначении пиридоксина, систематически вводившегося всем новорожденным и детям в возрасте до двух лет с необъяснимыми судорогами.
В последнее время выяснилось, что по повышению пипеколиновой кислоты в крови и моче можно, очевидно, проводить биохимическую диагностику (Gospe, 2006). В настоящее время диагноз может быть подтвержден при наличии мутации в гене антиквитин (Mills et al., 2006; Plecko et al., 2007), что позволяет избежать необходимости ждать повторения судорог после отмены лечения пиридоксином. Пиридоксин при раннем назначении может предупредить ухудшение и последствия, такие как микроцефалию (Tan et al., 2004) и задержку умственного развития.
В редких случаях форм с поздним началом (Baxter et al., 1996; Baxter et al., 2001) судороги как проявление пи-родоксиновой зависимости, развиваются относительно поздно, на 18-24 месяце. Такие приступы склонны развиваться повторно при эпилептическом статусе, но могут также проявляться в виде инфантильных спазмов или миоклонических приступов (Goutieres и Aicar-di, 1985). В некоторых случаях судороги могут отвечать на противосудорожные препараты и контролируются на протяжении нескольких недель или даже месяцев или такой же период времени после проведения терапии витамином В6.
Лечение пиридоксиновой зависимости требует витамина B6 в дозах, в среднем варьирующих между 0,2 и 30 мг/кг/сутки. В случаях с эпилептическим статусом внутривенное назначение 50-100 мг должно остановить судороги менее, чем за 10 минут. При кратковременных судорогах однократный пероральный прием 50 мг/сутки вызывает быстрое прекращение приступов. Внутривенное введение более 200 мг может привести к гипотонии и апноэ (Kroll, 1985). Однако наблюдались кома и дыхательные расстройства даже после введения лекарств через желудочный зонд у пациентов реагировавших на очень маленькие дозы (Grillo et al., 2001).
Имеются сообщения о случаях неонатальной эпилептической энцефалопатии, рефрактерной к пиридоксину, но резко чувствительной к фосфату пиридоксина (Кио и Wang, 2002; Clayton et al., 2003; Hoffmann et al., 2007). Таким образом, при наличии возможности, фосфат пиридоксина является лучшим терапевтическим выбором в случаях зависимости от пиридоксина, и как было показано, может спасти жизнь и предотвратить повреждение мозга (Hoffmann et al., 2007). В этих случаях была продемонстрирована мутация в гене PNPO, кодирующем фермент пиридокс (ам) ин-5’-фосфатазу, который преобразует пиридоксин в фосфат пиридоксина (Mills et al., 2005).
Некоторые судороги не связаны с зависимостью, но могут быть чувствительными к пиридоксину (Baxter, 2001). Возможна связь с несколькими механизмами (Clayton, 2006). Могут потребоваться высокие дозы пиридоксина в сочетании с противоэпилептическими препаратами. Мегадозы пиридоксина (более 1 г) способны вызывать хроническую нейропатию (Schaumburg et al„ 1983).
Неонатальные судороги, чувствительные к фолиевой кислоте, чрезвычайно редки, имеются сообщения только об отдельных случаях (Torres et al., 1999; Frye et al., 2003; Nicolai et al., 2006). Судороги были неонатальными во всех случаях, кроме одного ребенка, который изначально ответил на пиридоксин. Исследование нейротрансмиттеров в ЦСЖ, вероятно, необходимо для постановки диагноза (Hyland и Arnold, 2002).
в) Нервная система при дефиците цианокобаламина (витамин В12). Дефицит цианокобаламина у взрослых отвечает за классическую картину подострой дегенерации задних и боковых столбов спинного мозга. У детей такое состояние исключительно редко с возможным сочетанием с пернициозной анемией или с кишечным заболеванием.
Клинические проявления в таких случаях включают атаксию, слабость и спазмы в нижних конечностях, утрату вибрационной чувствительности и интеллектуальный дефицит (Facchini et al., 2001; Kumar, 2004).
Пищевая недостаточность цианокобаламина относительно распространена в Индии. В западных странах случаи наблюдались у детей на грудном вскармливании от матерей с дефицитом витамина В12, в результате пернициозной анемии или строгой вегетарианской (растительной) диеты с недостаточным содержанием витаминов (Grattan-Smith et al., 1997). В таких случаях присутствует выделение гомоцистеина и метилмалоновой кислоты, хотя не постоянно (Stollhoff и Schulte, 1987). Клиническая картина характеризуется нормальным развитием в течение первых месяцев жизни, затем отмечается регресс, симптомы пирамидального тракта и признаки атрофии мозга при выполнении нейровизуализации. Хореомиоклонические движения, наблюдающиеся у некоторых пациентов (Emery et al., 1987; Grattan-Smith et al., 1997), могут возникнуть во время начала приема витамина В (Ozer et al., 2001). С началом терапии наблюдается быстрое улучшение состояния, и атрофия может исчезать.

Последствия могут сохраняться при запоздалом лечении. Неврологическая патология может присутствовать и без анемии или макроцитоза (Lindenbaum et al., 1988).
Схожая клиника, но с более ранним началом с первых месяцев жизни, может встречаться у некоторых новорожденных с врожденными нарушениями обмена витамина В12.
Дефицит кобаламина обычно хорошо реагирует на лечение витамином В12. Назначения фолиевой кислоты следует избегать, поскольку она может ухудшить неврологические проявления. Существуют некоторые предположения, что спектр неврологических проявлений дефицита цианоколабина может быть широким у взрослых пациентов и включает психиатрические расстройства (Nijst et al., 1990). Essa et al. (1998) описали педиатрический случай смешанного психиатрического и неврологического заболевания, связанного с дефектом обмена цианокобаламина.
г) Нервная система при нарушении обмена фолиевой кислоты. Фолиевая кислота играет важную роль в развитии нервной системы (Greenblatt et al., 1994). Назначение фолиевой кислоты во время беременности предупреждает развитие большинства дефектов нервной трубки; этой проблеме уделено внимание в отдельной статье на сайте.
Церебральный дефицит фолиевой кислоты можно определить как любой неврологический синдром, связанный с низким уровнем 5-метилтетрагидрофола-та в ЦСЖ, активного метаболита фолиевой кислоты, при наличии нормального обмена фолиевой кислоты вне ЦНС (Ramaekers и Blau, 2004). Это состояние, связанное с выходом фолиевой кислоты или повышенным расходованием фолата в ЦНС; проблема обсуждалась в отдельной статье на сайте наряду с другими нарушениями обмена фолиевой кислоты.
Врожденная мальабсорбция фолиевой кислоты является редким метаболическим расстройством с избирательной неспособностью всасывания фолиевой кислоты из кишечника и через гематоэнцефалический барьер. Заболевание проявляется в раннем периоде новорожденности диареей, плохой прибавкой в весе и мегалобластической анемией. Неврологические проявления могут включать задержку умственного развития, судороги, атаксию, экстрапирамидную патологию и периферическую нейропатию (Steinschneider et al., 1990). Диагноз подтверждается на основании низких показателей фолиевой кислоты в плазме крови и ликворе. Лечение фолиниевой кислотой может быть более эффективным, чем фолиевой кислотой, и при раннем назначении состояние может быть полностью обратимым. Похожие проявления могут возникать у пациентов с дефицитом фолат-связывающего белка в ЦНС (Wevers et al., 1994).
д) Нервная система при дефиците никотиновой кислоты. Это редкое состояние, которое обычно наблюдается в местах, где кукуруза является основным пищевым продуктом. Дети с умеренной патологией апатичны и раздражительны. В тяжелых случаях отмечается полинейропатия и дегенерация клеток Беца в двигательной коре и в пирамидальных и спиномозжечковых путях спинного мозга. Клинически заболевание известно под названием пеллагра, вероятно, являясь результатом поливитаминной недостаточности, но реагирующей на никотиновую кислоту. Характерной особенностью является кожная сыпь. В дополнение к периферическому вовлечению может присутствовать оглушение или слабоумие, атрофия зрительного нерва и грубый тремор (Pitsavas et al., 2004).
е) Нервная система при дефиците жирорастворимых витаминов. Дефицит витамина А способен вызывать повышение внутричерепного давления, обратимое при витаминотерапии. Сходный эффект чаще бывает при избытке витамина А. В некоторых развивающихся странах дефицит витамина А является основной причиной расстройств зрения и слепоты (Kello и Gilbert, 2003).
Дефицит витамина Е встречается в случаях муковисцидоза (Willison et al., 1985), желчнокаменной болезни и других мальабсорбтивных состояниях, включающих синдром слепой петли (хирургически отведенная кишечная петля), и редко как изолированный дефицит (Jayaram et al., 2005). Генетически детерминированные случаи, связанные с мутацией в альфа-токоферол транспортном белке, симптоматически очень сходны с атаксией Фридрейха, частично реагирующей на назначение витамина В6 (Mariotti et al., 2004). Возникающая при этом нейропатия описана в главе 20. Вовлечение в процесс мышц с накоплением электроноплотного материала в мышечных волокнах является частым (Jackson et al., 1996) и может встречаться повышение креатинкиназы (Kohlschutter, 1993).
Нейропатия при абетолипопротеинемии, вероятно, имеет похожий механизм (Brin et al., 1986).
- Вернуться в оглавление раздела "Неврология."
Редактор: Искандер Милевски. Дата публикации: 16.1.2019

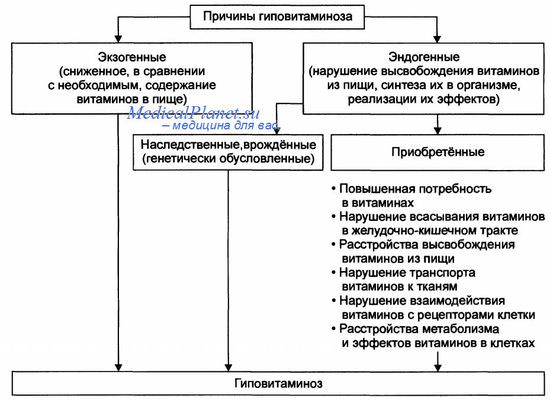
Нехватка витаминов может возникнуть по самым разным причинам. К основным из них относятся:
- однообразный рацион;
- неправильное приготовление продуктов;
- заболевания желудочно-кишечного тракта;
- беременность и период лактации;
- стрессовые состояния и нервные перегрузки;
Витамин B1
Клеточный энергетик, способствующий росту и развитию. Витамин B1 повышает умственную и физическую работоспособность, улучшает детоксикационную функцию и обмен веществ в нервной системе. Он также повышает настроение, обладает мягким обезболивающим и ранозаживляющим действием.
При дефиците витамина B1 возникают различные нарушения со стороны нервной, сердечно-сосудистой и пищеварительной систем. Чтобы восполнить его недостаток, включите в рацион гречку, кукурузу, кешью, чечевицу.
Основные симптомы дефицита витамина B1
- потеря аппетита;
- нарушение координации движения;
- депрессия, нервозность;
- ослабление когнитивных функций (снижение памяти);
- мышечная слабость.
Крайняя форма нехватки витамина — болезнь Бери-бери, при которой происходит поражение периферических нервов или сердечно-сосудистой системы. В результате этого истощаются мышцы, особенно ног, появляются сильные боли в икрах, развивается слабость и ухудшается походка.
Причины дефицита витамина B1
- постоянное употребление рафинированных продуктов (мука высших сортов и продукты из нее, шлифованный рис);
- повышенная потребность в витамине (беременность, кормление грудью, стресс, физические нагрузки, инфекции);
- хронические заболевания (сахарный диабет, тиреотоксикоз, отравление антибиотиками, алкоголизм);
- курение;
- чрезмерное употребление чая и кофе, так как кофеин разрушает витамин B1.
Если Вы заметили, что ухудшилось настроение, появились судороги в икроножных мышцах, на фоне постоянного стресса пропал аппетит, выполните в СИТИЛАБ исследование 95-10-201 — Витамин B1 (тиамин). Анализ помогает выявить дефицит витамина B1, своевременно назначить прием лекарственных препаратов и скорректировать режим питания.
Витамин B5
Пантотеновая кислота (витамин B5) оказывает стресс-протекторное действие и входит в состав кофермента А, который принимает участие в обменных процессах и белков, и жиров, и углеводов.
Витамин B5 необходим для синтеза жизненно важных веществ, таких как гемоглобин, холестерин, гистамин, ацетилхолин. Кроме этого, он активизирует синтез глюкокортикостероидов (гормоны надпочечников), которые обладают иммунорегулирующим, антиаллергическим, противовоспалительным действием. Важно понимать, что без пантотеновой кислоты плохо или вовсе не усваиваются и другие витамины. В рацион добавить порцию витамина помогут скумбрия, сардина, тунец, сладкий болгарский перец, кедровые орехи.
Основные симптомы дефицита витамина B5
- быстрая утомляемость, слабость, апатия;
- появления чувства жжения в пальцах ног, нередко — их онемении;
- при выраженном недостатке возникает синдром «горящих ступней» — мучительные боли в ногах в ночное время.
При нехватке пантотеновой кислоты снижается выработка желудочного сока, ухудшается работа сердца, развиваются невриты, повышается риск развития заболеваний кожи, язвы двенадцатиперстной кишки.
Причины дефицита витамина B5
- длительное неполноценное питание (бедная белками, жирами, витамином С и витаминами группы В пища);
- подавление кишечной микрофлоры, в том числе длительный прием антибиотиков и сульфаниламидных препаратов;
- заболевания кишечника различной природы.
Чтобы своевременно выявить дефицит пантотеновой кислоты, пройдите в СИТИЛАБ исследование 95-10-202 — Витамин B5 (пантотеновая кислота).
Витамин B6
По сути, витамин B6 (пиридоксин) — «активатор» метаболизма. Он необходим для регуляции усвоения белков, обмена аминокислот, принимающих участие в синтезе основных нейромедиаторов и гемоглобина. При участии пиридоксина происходит доставка глюкозы к клеткам, в том числе к клеткам мозга. Витамин B6 влияет на когнитивные функции: улучшает память, мышление, а также повышает настроение и помогает противостоять стрессу.
Содержится во многих растительных продуктах — бананы, орехи (фисташки, фундуку), авокадо, фасоль, соя, говяжья печень. Важно помнить, что при длительной или неправильной термической обработке продуктов данный витамин разрушается.
Основные симптомы дефицита витамина B6
- утомляемость, депрессия;
- выпадение волос;
- «заеды» в уголках губ.
Явная нехватка витамина B6 снижает синтез дофамина, серотонина, гамма-аминомасляной кислоты, мелатонина. Это может приводить к психологическим и физиологическим нарушениям, бессоннице, снижению интеллектуальных способностей, раздражительности, апатии или наоборот к агрессивному поведению.
Причины дефицита витамина B6
- ослабленное состояние, в том числе после операций, тяжелой болезни;
- атеросклероз;
- сердечно-сосудистые заболевания;
- беременность;
- длительное избыточное потребление белковой пищи;
- повышенные физические нагрузки;
- заболевания печени, гастриты;
- малокровие.
Если Вы заметили, что прическа стала не такой пышной, появилась сильная сухость кожи в области носогубной складки, над бровями, в целом кожа стала более сухой и шершавой, медленно заживают порезы и царапины — не откладываете визит к врачу. Первое, что Вам необходимо сделать, это сдать кровь в СИТИЛАБ для исследования 95-10-203 Витамин B6 (пиридоксин), которое поможет установить, есть ли дефицит витамина B6 в организме или его достаточно.
Витамин B12
Витамины B12 — это целая группа кобальтосодержащих биологически активных веществ. Одним из главных в ней является цианокобаламин. Он участвует в производстве эритроцитов и процессе кроветворения. Содержится преимущественно в продуктах животного происхождения — мясо, молоко, яйца. Поэтому чаще всего дефицит наблюдается у людей, соблюдающих строгую вегетарианскую диету, у беременных, которым требуется повышенное количество B12, а также при атрофическом гастрите, хронических воспалительных заболеваниях тонкой кишки.
Основные симптомы дефицита витамина B12
- онемение конечностей;
- мышечная слабость;
- расстройства зрения (двоение в глазах, размытые контуры предметов);
- бледность кожи;
- снижение памяти.
При нехватке витамина B12 возникает риск развития тромбозов, нарушается работа вегетативной нервной системы.
Причина дефицита витамина B12 — недостаточное всасывание его в кишечнике. Это может быть связано с нарушением внутреннего фактора в желудке, развитием патогенной микрофлоры, которая может препятствовать всасыванию в желудке.
С возрастом, после 40 лет, усвоение витамина B12 происходит хуже, поэтому важно своевременно выявить его дефицит, чтобы предотвратить серьезные болезни. Для этого пройдите в СИТИЛАБ исследование 33-20-045 — витамин B12.
Симптомы и течение:
Распространенное поражение периферических нервов (полиневрит) и сердечно-сосудистой системы. Больные жалуются на утомляемость, головную боль, одышку, сердцебиение при физической нагрузке. Беспокоят парестезии (ощущение "ползания мурашек") и понижение кожной чувствительности ног, а затем и других участков тела, ощущение слабости и тяжести в ногах, хромота, отеки, учащенный пульс, понижение артериального давления. Возможны расстройства функций органов пищеварения, зрения, психики.
Клиническая картина складывается из поражения периферической нервной системы (расстройство чувствительности, парезы, параличи разгибателей кисти и стопы), миокардиодистрофии правых отделов сердца с последующим развитием правожелудочковой недостаточности и выраженного отечного синдрома. Различают начальную, полиневритическую, или 'сухую' (безотечную), и сердечную (отечную) формы бери-бери; по течению различают острую и хроническую, по тяжести - легкую и злокачественную.
В острой форме признаки поражения периферических нервов возникают в течение суток, при этом ощущается боль по трассе нервных стволов и слабость конечностей, потеря нормальной чувствительности и слабовыраженные парезы и параличи кистей и стоп. Заметна раздражительность, состояние тревоги и беспокойства, возможен бред, корсаковский синдром.
Лечение возможно, и своевременные лечебные мероприятия гарантируют полное выздоровление. Однако продолжительный дефицит тиамина влечет за собой хронический полиневрит.
Бери-бери преимущественно распространена в странах Восточной и Юго-Восточной Азии, Южной Америки, Африки; в Европе встречаются единичные случаи болезни.
Заболевание развивается при отсутствии в пище витамина B1 (главный этиологический фактор) наряду с отсутствием других витаминов группы В, поэтому его следует рассматривать как комплексный В-авитаминоз. Имеют значение и предрасполагающие факторы: беременность, лактация, чрезмерный физический труд, алкоголизм, заболевания желудка и кишечника, связанные с нарушением всасывания (длительные поносы, рвоты, инфекции, лихорадочные заболевания, тиреотоксикоз).
Наблюдаются резкое общее истощение, распространенный или частичный отек. Сердце увеличено преимущественно вследствие расширения правых его отделов, резко расширен conus arteriosus. Надпочечники, гипофиз и щитовидная железа увеличены. Мышечные волокна сердца раздвинуты большим количеством серозной жидкости, отмечается жировая и водяночная дистрофия миокарда; дегенеративные изменения в периферической нервной системе - распад аксонов нервных волокон и их миелиновых оболочек.
Острая пернициозная бери-бери (по терминологии японских авторов, 'шошин' - сердечный толчок) - самая тяжелая, часто смертельная форма; протекает с резко выраженными и быстро развивающимися признаками сердечной недостаточности.
Распознавание:
Проводится на основании данных клинической картины, уровень тиамина в суточной моче ниже 100 мкг, содержание кокарбоксилазы в эритроцитах ниже 20-40 мкг/л.
Назначают витамин B1 в комплексе с другими витаминами (никотиновая кислота, рибофлавин, витамин В 6 ), проводят симптоматическую терапию. Употребляют пищу с высоким содержанием витамина B1: пшеничный и ржаной хлеб, дрожжи, горох, желток яиц, свинину.
Постельный режим, особенно при поражениях сердца или выраженных симптомах полиневрита; парэнтерально - 20-50 мг витамина Л, ежедневно до наступления выраженного улучшения, затем 10-20 мг в день в течение длительного времени (2-3 месяцев). Целесообразно одновременно с витамином В1 назначать никотиновую кислоту или ее амид (25 и 50 мг), рибофлавин (10-20 мг), витамин В6 (10- 50 мг). Пища должна быть высококалорийной и содержать большое количество белков.
Профилактика
Питание, богатое витаминами группы В, прежде всего витамином B1. При беременности, лактации, физической работе следует рекомендовать прием больших, чем обычно, доз витамина B1. Профилактическое значение имеет и лечение всех заболеваний, при которых нарушается всасывание витамина В1,. См. также Витаминная недостаточность.
Никакая информация, размещенная на этой или любой другой странице нашего сайта, не может служить заменой личного обращения к специалисту. Информация не должна использоваться для самолечения и приведена только для ознакомления.
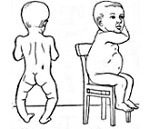
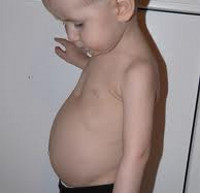
Рахит – заболевание быстрорастущего организма, характеризующееся нарушением минерального обмена и костеобразования. Рахит проявляется множественными изменениями со стороны опорно-двигательного аппарата (размягчением плоских костей черепа, уплощением затылка, деформацией грудной клетки, искривлением трубчатых костей и позвоночника, мышечной гипотонией и др.), нервной системы, внутренних органов. Диагноз устанавливается на основании выявления лабораторных и рентгенологических маркеров рахита. Специфическая терапия рахита предполагает назначение витамина D в комплексе с лечебными ваннами, массажем, гимнастикой, УФО.
- Патогенез рахита
- Причины рахита
- Классификация рахита
- Симптомы рахита
- Диагностика рахита
- Лечение рахита
- Прогноз и профилактика
- Цены на лечение
Общие сведения
Рахит – полиэтиологическое заболевание обмена веществ, в основе которого лежит дисбаланс между потребностью детского организма в минеральных веществах (фосфоре, кальции и др.) и их транспортировкой и метаболизмом. Поскольку рахитом страдают преимущественно дети в возрасте от 2-х месяцев до 3-х лет, в педиатрии его часто называют «болезнью растущего организма». У детей старшего возраста и взрослых для обозначения подобного состояния используют термины остеомаляция и остеопороз.
В России распространенность рахита (включая его легкие формы) составляет 54-66% среди доношенных детей раннего возраста и 80% - среди недоношенных. У большинства детей в 3-4-месяца имеются 2-3 нерезко выраженных признака рахита, в связи с чем некоторые педиатры предлагают рассматривать данное состояние как парафизиологическое, пограничное (аналогично диатезу - аномалиям конституции), которое самостоятельно ликвидируется по мере взросления организма.

Патогенез рахита
Определяющая роль в развитии рахита принадлежит экзо- или эндогенному дефициту витамина D: недостаточному образованию холекальциферола в коже, недостаточному поступлению витамина D с пищей и нарушению его метаболизма, что приводит к расстройству фосфорно-кальциевого обмена в печени, почках, кишечнике. Кроме этого, развитию рахита способствуют и другие метаболические нарушения – расстройство обмена белка и микроэлементов (магния, железа, цинка, меди, кобальта и др.), активизация перекисного окисления липидов, поливитаминная недостаточность (дефицит витаминов А, В1, В5, В6, С, Е) и пр.
Основными физиологическими функциями витамина D (точнее – его активных метаболитов 25-гидроксихолекальциферола и 1,25-дигидроксихолекальциферола) в организме служат: усиление всасывания солей кальция (Ca) и фосфора (P) в кишечнике; препятствие выведению Ca и P с мочой за счет усиления их реабсорбции в канальцах почек; минерализация костной ткани; стимуляция образования эритроцитов и др. При гиповитаминозе D и рахите замедляются все вышеперечисленные процессы, что приводит к гипофосфатемии и гипокальциемии (пониженному содержанию P и Ca в крови).
Вследствие гипокальциемии по принципу обратной связи развивается вторичный гиперпаратиреоз. Увеличение продукции паратиреоидного гормона обусловливает выход Ca из костей и поддержание его достаточно высокого уровня в крови.
Изменение кислотно-щелочного равновесия в сторону ацидоза препятствует отложению соединений P и Сa в костях, что сопровождается нарушением обызвествления растущих костей, их размягчением и склонностью к деформации. Взамен полноценной костной ткани в зонах роста образуется остеоидная необызвествленная ткань, которая разрастается в виде утолщений, бугров и т. д.
Кроме минерального обмена, при рахите нарушаются и другие виды обмена (углеводный, белковый, жировой), развиваются расстройства функции нервной системы и внутренних органов.
Причины рахита
Развитие рахита в большей степени связано не с экзогенным дефицитом витамина D, а с его недостаточным эндогенным синтезом. Известно, что более 90% витамина D образуется в коже вследствие инсоляции (УФО) и лишь 10% поступает извне с пищей. Всего 10-минутное локальное облучение лица или кистей рук способно обеспечить синтез необходимого организму уровня витамина D. Поэтому рахит чаще встречается у детей, рожденных осенью и зимой, когда солнечная активность крайне низка. Кроме этого, рахит наиболее распространен среди детей, проживающих в регионах с холодным климатом, недостаточным уровнем естественной инсоляции, частыми туманами и облачностью, неблагополучной экологической обстановкой (смогом).
Между тем, гиповитаминоз D является ведущей, но не единственной причиной рахита. Дефицит солей кальция, фосфатов и других остеотропных микро- и макроэлементов, витаминов у детей раннего возраста может быть вызван множественными рахитогенными факторами. Поскольку наиболее усиленное поступление Ca и P к плоду отмечается на последних месяцах беременности, то к развитию рахита более склонны недоношенные дети.
К возникновению рахита предрасполагает повышенная физиологическая потребность в минеральных веществах в условиях интенсивного роста. Дефицит витаминов и минералов в организме ребенка может быть следствием неправильного рациона беременной или кормящей женщины, либо самого грудничка. Нарушению всасывания и транспортировки Ca и P способствует незрелость ферментных систем либо патология ЖКТ, печени, почек, щитовидной и паращитовидных желез (гастрит, дисбактериоз, синдром мальабсорбции, кишечные инфекции, гепатит, атрезия желчных путей, ХПН и др.).
К группе риска по развитию рахита относятся дети с неблагополучным перинатальным анамнезом. Неблагоприятными факторами со стороны матери служат гестозы беременных; гиподинамия в период беременности; оперативные, стимулированные или стремительные роды; возраст матери моложе 18 и старше 36 лет; экстрагенитальная патология.
Со стороны ребенка определенную роль в развитии рахита могут играть большая масса (более 4 кг) при рождении, чрезмерная прибавка в весе или гипотрофия; ранний перевод на искусственное либо смешанное вскармливание; ограничение двигательного режима ребенка (слишком тугое пеленание, отсутствие детского массажа и гимнастики, необходимость длительной иммобилизации при дисплазии тазобедренных суставов), прием некоторых лекарств (фенобарбитала, глюкокортикоидов, гепарина и др.). Доказана роль гендерных и наследственных факторов: так, к развитию рахита более предрасположены мальчики, дети со смуглой кожей, II (А) группой крови; реже рахит встречается среди детей с I (0) группой крови.
Классификация рахита
Этиологическая классификация предполагает выделение следующих форм рахита и рахитоподобных заболеваний:
- Витамин-D-дефицитногорахита (кальцийпенического, фосфоропенического варианта)
- Витамин-D-зависимого (псевдодефицитного) рахита при генетическом дефекте синтеза в почках 1,25-дигидроксихолекальциферола (тип 1) и при генетической резистентности рецепторов органов-мишеней к 1,25-дигидроксихолекальциферолу (тип 2).
- Витамин D-резистентного рахита (врожденного гипофосфатемического рахита, болезни Дебре-де-Тони-Фанкони, гипофосфатазии, ренального тубулярного ацидоза).
- Вторичного рахита при заболеваниях ЖКТ, почек, обмена веществ или индуцированного лекарственными препаратами.
Клиническое течение рахита может быть острым, подострым и рецидивирующим; степень тяжести – легкой (I), среднетяжелой (II) и тяжелой (III). В развитии заболевания выделяют периоды: начальный, разгара болезни, реконвалесценции, остаточных явлений.
Симптомы рахита
Начальный период рахита приходится на 2-3-й месяц жизни, а у недоношенных на середину – конец 1-го месяца жизни. Ранними признаками рахита служат изменения со стороны нервной системы: плаксивость, пугливость, беспокойство, гипервозбудимость, поверхностный, тревожный сон, частые вздрагивания во сне. У ребенка усиливается потливость, особенно в области волосистой части головы и затылка. Клейкий, с кисловатым запахом пот раздражает кожу, вызывая появление стойких опрелостей. Трение головой о подушку приводит к образованию на затылке очагов облысения. Со стороны костно-мышечной системы характерно появление мышечной гипотонии (вместо физиологического гипертонуса мышц), податливости черепных швов и краев родничка, утолщений на ребрах («рахитических четок»). Продолжительность течения начального периода рахита составляет 1–3 месяца.
В период разгара рахита, который обычно приходится на 5-6-ой месяц жизни, отмечается прогрессирование процесса остеомаляции. Следствием острого течения рахита может служить размягчение черепных костей (краниотабес) и одностороннее уплощение затылка; деформация грудной клетки с вдавлением («грудь сапожника») или выбуханием грудины (килевидная грудь); формирование кифоза («рахитический горб»), возможно - лордоза, сколиоза; О-образное искривление трубчатых костей, плоскостопие; формирование плоскорахитического узкого таза. Кроме костных деформаций, рахит сопровождается увеличением печени и селезенки, выраженной анемией, мышечной гипотонией («лягушачьим» животом), разболтанностью суставов.
При подостром течении рахита возникает гипертрофия лобных и теменных бугров, утолщение межфаланговых суставов пальцев рук («нити жемчуга») и запястий («браслетки»), реберно-хрящевых сочленений («рахитические четки»).
Изменения со стороны внутренних органов при рахите обусловлены ацидозом, гипофосфатемией, расстройствами микроциркуляции и могут включать одышку, тахикардию, снижение аппетита, неустойчивый стул (диарею и запоры), псевдоасцит.
В период реконвалесценции нормализуется сон, уменьшается потливость, улучшаются статические функции, лабораторные и рентгенологические данные. Период остаточных явлений рахита (2-3 года) характеризуется остаточной деформацией скелета, мышечной гипотонией.
У многих детей рахит протекает в легкой форме и не диагностируется в детском возрасте. Дети, страдающие рахитом, часто болеют ОРВИ, пневмонией, бронхитом, инфекциями мочевыводящих путей, атопическим дерматитом. Отмечается тесная связь рахита и спазмофилии (детской тетании). В дальнейшем у детей, перенесших рахит, часто отмечается нарушение сроков и последовательности прорезывания зубов, нарушение прикуса, гипоплазия эмали.
Диагностика рахита
Диагноз рахита устанавливается на основании клинических признаков, подтвержденных лабораторными и рентгенологическими данными. Для уточнения степени нарушения минерального обмена проводится биохимическое исследование крови и мочи. Важнейшими лабораторными признаками, позволяющими думать о рахите, служат гипокальциемия и гипофосфатемия; увеличение активности щелочной фосфатазы; снижение уровня лимонной кислоты, кальцидиола и кальцитриола. При исследовании КОС крови выявляется ацидоз. Изменения в анализах мочи характеризуются гипераминоацидурией, гиперфосфатурией, гипокальциурией. Проба Сулковича при рахите отрицательная.
При рентгенографии трубчатых костей выявляются характерные для рахита изменения: бокаловидное расширение метафизов, нечеткость границ между метафизом и эпифизом, истончение коркового слоя диафизов, неотчетливая визуализация ядер окостенения, остеопороз. Для оценки состояния костной ткани может использоваться денситометрия и КТ трубчатых костей. Проведение рентгенографии позвоночника, ребер, черепа, нецелесообразно ввиду выраженности и специфичности в них клинических изменений.
Дифференциальная диагностика при рахите проводится с рахитоподобными заболеваниями (D-резистентным рахитом, витамин-D-зависимый рахитом, болезнью де Тони-Дебре-Фанкони и почечным тубулярным ацидозом и др.), гидроцефалией, ДЦП, врожденным вывихом бедра, хондродистрофией, несовершенным остеогенезом.
Лечение рахита
Комплексная медицинская помощь ребенку с рахитом складывается из организации правильного режима дня, рационального питания, медикаментозной и немедикаментозной терапии. Детям, страдающим рахитом, необходимы ежедневное пребывание на свежем воздухе в течение 2-3 часов, достаточная инсоляция, более раннее введение прикорма, закаливающие процедуры (воздушные ванны, обтирания). Важное значение имеет правильное питание кормящей мамы с приемом витаминно-минеральных комплексов.
Специфическая терапия рахита требует назначения витамина D в лечебных дозах в зависимости от степени тяжести заболевания: при I ст. – в суточной дозе 1000-1500 МЕ (курс 30 дней), при II - 2000-2500 МЕ (курс 30 дней); при III - 3000-4000 МЕ (курс – 45 дней). После окончания основного курса витамин D назначается в профилактической дозе (100-200 МЕ/сут.). Лечение рахита следует проводить под контролем пробы Сулковича и биохимических маркеров для исключения развития гипервитаминоза D. Поскольку при рахите часто отмечается полигиповитаминоз, детям показан прием мультивитаминных комплексов, препаратов кальция, фосфора.
Прогноз и профилактика
Начальные стадии рахита хорошо поддаются лечению; после адекватной терапии отдаленные последствия не развиваются. Тяжелые формы рахита могут вызывать выраженные деформации скелета, замедление физического и нервно-психического развития ребенка. Наблюдение за детьми, перенесшими рахит, проводится ежеквартально, не менее 3 лет. Рахит не является противопоказанием для профилактической вакцинации детей: проведение прививок возможно уже через 2-3 недели после начала специфической терапии.
Профилактика рахита делится на антенатальную и постнатальную. Дородовая профилактика включает прием беременной специальных микронутриентных комплексов, достаточное пребывание на свежем воздухе, полноценное питание. После родов необходимо продолжать прием витаминов и минералов, осуществлять грудное вскармливание, придерживаться четкого распорядка дня, проводить ребенку профилактический массаж. Во время ежедневных прогулок личико ребенка следует оставлять открытым для доступа к коже солнечных лучей. Специфическая профилактика рахита новорожденным, находящимся на естественном вскармливании, осуществляется в осенне-зимне-весенний период с помощью витамина D и УФО.
Дефицит витамина В1
Витамин В1 (тиамин) – водорастворимый витамин, участвующий в процессах метаболизма углеводов и жиров и энергетическом обмене организма человека. Данный витамин необходим нормального роста и развития ребенка, опосредованно обуславливает нормальную работу сердца, нервной и пищеварительной систем.
Тиамин не вырабатывается организмом человека самостоятельно, однако в малых количествах может синтезироваться некоторыми видами бактерий, составляющих микрофлору толстого кишечника. Витамин В1 поступает с пищей, не накапливается,
избытки выделяются с мочой, он хорошо растворяется в воде, быстро разрушается при нагревании.
Тиамин участвует в процессах углеводного и жирового обменов, его дефицит приводит к накоплению виноградной кислоты, повреждающей в первую очередь клетки нервной системы. Помимо этого, витамин В1 необходим для синтеза ацетилхолина – специального вещества, участвующего в передаче нервного импульса.
Основным источником тиамина является растительная пища. Богаты тиамином такие растительные продукты, как цельные злаки, соя, фасоль, горох, шпинат, картофель, морковь, капуста. Из животных продуктов следует выделить печень, почки, мозг, свинину, говядину, также он содержится в дрожжах.
Суточная потребность в тиамине у детей зависит от возраста и составляет 0,2-1,4 мг
Наиболее часто недостаток тиамина в организме возникает вследствие нарушения питания, что было доказано при его открытии (лица употреблявшие в пищу шлифованный рис развивали клиническую картину гиповитаминоза В1 чаще чем те кто употреблял нешлифованный) или при наличии в продуктах так называемых тиаминаз, разрушающих данный витамин (рыба, морепродукты), или веществ, ухудшающих его всасывание (чай, кофе). Кроме того, авитаминоз (болезнь бери-бери) выявляется у лиц с нарушением всасывания в желудочно-кишечном тракте, особенно при специфических операциях на желудке. У взрослых также встречаются вторичные формы гиповитаминоза, которые связаны с чрезмерным приемом алкоголя, декомпенсированным сахарным диабетом, хронические расстройства пищеварения, в том числе и при злокачественных опухолях, а также их лечении. В литературе описано всего несколько случаев врожденной толерантности к тиамину (невозможность всасывания). Учитывая водорастворимость и отсутствие накопления, гипервитаминоз В1 нехарактерен.
Клинические проявления. Ранние признаки гиповитаминоза неспецифичны и включают такие симптомы как повышенная утомляемость, сонливость, раздражительность, апатия, детям тяжелее сконцентрироваться, страдает память, внимание, также возможны тошнота и ощущение дискомфорта в животе. По мере прогрессирования заболевания появляются симптомы поражения нервной системы. Ребенка могут беспокоить непривычные беспричинные неприятные ощущения такие как жжение, покалывание, онемение, зуд кожи особенно в областях кистей и стоп. В дальнейшем поражения со стороны нервной системы прогрессируют – отмечаются явления мышечной слабости, головокружения, возможно нарушение зрения, опущение одного или обеих век, изменения голоса, нарушения моторной функции желудочно-кишечного тракта, судороги, повышение частоты сердечных сокращений. Кроме того, возможно увеличение сердца и печени. При глубоком некорригируемом дефиците Витамина В1 возможна летаргия и даже смерть вследствие нарушение сердечной деятельности или внутричерепного кровоизлияния.
Постановка диагноза на ранних этапах развития дефицитного состояния затруднена вследствие неспецифичности симптомов заболевания. Возможно проведение нагрузочных тестов с тиамином с последующим контролем его концентрации (или продуктов обмена витамина В1) в моче (выполняется редко).
Профилактика гиповитаминоза не составляет трудностей и сводится к употреблению продуктов богатых тиамином, уменьшению в рационе рафинированных жиров и муки высшего сорта.
Лечение дефицита витамина В1 осуществляется путем применения препаратов тиамина. При легких нарушениях, как правило, применяются пероральные препараты или короткие курсы внутримышечных введений. При более тяжелых формах – внутримышечно и внутривенно вводятся большие (до 50 мг) дозы тиамина, может также потребоваться сопроводительная терапия, направленная на стабилизацию состояния ребенка или лечение осложнений.
При легких и среднетяжелых состояниях прогноз благоприятный.
Данный материал предназначен для родителей и рассчитан на лиц старше 18 лет, имеющих образование не ниже чем полное среднее/ среднее специальное и свободно владеющих русским языком. Он не является пособием по диагностике, лечению или тактике ведения того или иного заболевания или состояния, не может являться учебным пособием для студентов или других учащихся и представлен лишь с ознакомительной целью. В целях безопасности Вашего ребенка некоторые специфические аспекты диагностики и терапии заболеваний или состояний были умышленно опущены.
Не пытайтесь самостоятельно устанавливать у ребенка диагноз. Не пытайтесь лечить ребенка самостоятельно или по совету лиц, не имеющих юридического и морального права на лечение детей. Помните, Ваши взгляды, оценка полученной самостоятельно медицинской информации могут быть непрофессиональны и заведомо ошибочны, а действия – нанести вред Вашему ребенку. Если у Вас есть вопросы/сомнения/подозрения/опасения по поводу состояния здоровья Вашего ребенка, пожалуйста, обратитесь к врачу, имеющему действующий профессиональный сертификат и допущенному к работе с детьми. Если состояние Вашего ребенка кажется Вам угрожающим – не сомневайтесь – вызовите Врача или позвоните в Скорую Медицинскую Помощь.
Читайте также:

