Состав микробной бляшки при гингивите и пародонтите
Опубликовано: 18.05.2024
у разных людей он различается, но в целом не изменяется
3различается и постоянно меняется по мере развития обоих заболеваний
Фазы роста микробной бляшки:
жгутиковые, спириллы и спирохеты, грамположительные кокки
спириллы и спирохеты, грамположительные кокки и палочки, грамотрицательные кокки, жгутиковые
3)грамположительные кокки и палочки, грамотрицательные кокки, жгутиковые, спириллы и спирохеты
10. Увеличение массы микробного налета в течение суток обусловлено ростом:
лактобацилл и спирилл
В). Структура содержания темы, основные понятия и положения темы.
Местные факторы полости рта, способствующие возникновению болезней пародонта.
Функциональная перегрузка или функциональная недогрузка пародонта.
Общие факторы, способствующие развитию болезней пародонта.
Студенты ведут приём пародонтальных больных, выявляют общие и местные этиологические факторы возникновения болезней пародонта, собирают анамнез заболевания и анамнез жизни, заполняют медицинскую документацию.
Сбор анамнеза пародонтологического больного (о.О.Д.).
Критерии самоконтроля
Выяснение жалоб пациента
Беседа с пациентом, амбулаторная карта
На наличие заболеваний пародонта указывает наличие следующих жалоб:
изменение цвета десны, ее увеличение или припухлость;
повышенная чувствительность зубов;
обнажение корней зубов;
зубной камень и выделение гноя;
неприятный запах изо рта.
Сбор анамнеза заболевания
Беседа с пациентом, амбулаторная карта
Выяснены ранние проявления болезни, сроки, когда, по мнению больного, началось заболевание, уточнено о течении болезни— менялись ли болезненные ощущения (усиливались, ослабевали, оставались без изменения). Пациент рассказал о лечении, которое проводилось ранее( если проводилось)и об его эффективности.
Сбор анамнеза жизни
Беседа с пациентом, амбулаторная карта
Найдена связь с перенесенными и сопутствующими заболеваниями
Обращено внимание на режим дня, характер питания, пищевой рацион, досуг и активный отдых, продолжительность сна, вредные привычки, отношение к занятию спортом, физиологические изменения организма у подростков в пубертатном периоде, у женщин репродуктивного возраста и у пожилых людей.
Пациент опрошен на наличие индивидуальной непереносимости на прием лекарственных препаратов, особенно связанные с лечением у стоматолога. Выяснено принимает ли пациент препараты для лечения хронических заболеваний.
Выходной контроль: Тестовые задачи:
Состав микробной бляшки при гингивите и пародонтите:
всегда не изменен
у разных людей он различается, но в целом не изменяется
различается и постоянно меняется по мере развития обоих заболеваний
В патогенезе функциональной перегрузки пародонта ведущая роль принадлежит:
патологической подвижности зуба
микроциркуляторным нарушениям в пародонте
увеличению силы и продолжительности нагрузки
воспалительной резорбции костной ткани альвеолы
Общесоматическая патология влияет на воспаление в пародонте:
является причиной болезни
не влияет на течение воспаления
влияет на отдельные звенья в патогенезе воспаления пародонта
Витамин С (аскорбиновая кислота) в организме человека:
продуцируется и накапливается
не продуцируется, но накапливается
продуцируется, но не накапливается
не продуцируется и не накапливается
В патогенезе поражений пародонта при ВИЧ-инфекции ведущим механизмом является:
патологические изменения носят первичный дистрофический характер
затруднение поступления микроэлементов и диффузии кислорода в ткани пародонта
развитие дисбаланса между иммунными и не специфическим механизмами защиты
В механизме остеопороза при заболеваниях печени и почек имеют значение:
нарушение обмена и эндогенная недостаточность витамина D,
гипосаливация, способствующая увеличению зубных отложений и фибринолитической активности слюны,
угнетение построения костной ткани, вызванное продукцией глюкокортикоидов и усилением продукции АКТГ.
Тут вы можете оставить комментарий к выбранному абзацу или сообщить об ошибке.
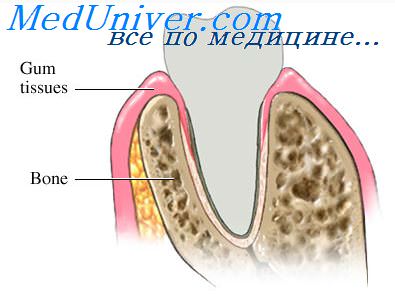
1. Пелликула, или вторичная кутикула. Пелликула образуется из компонентов слюны и десневой жидкости, бактерий, тканей и пищевых остатков. Состав специфических компонентов пелликулы в разных участках полости рта сильно различается.
Механизму образования пелликулы способствуют электростатические силы (силы Ван-дер-Ваальса), обеспечивающие крепкую связь поверхности гидроксиапатитов эмали зубов с положительно заряженными компонентами слюны или десневой жидкости..
2. Первичное микробное обсеменение происходит уже в первые часы образования пелликулы. Первичный покрывающий пелликулу слой составляют Act. viscosus и Str. sanguis, за счет наличия у них специальных адгезивных молекул, с помощью которых эти микроорганизмы избирательно прикрепляются к аналогичным адгезивным очагам на пелликуле. У Str. sanguis такими адгезивными участками являются молекулы декстрана, у Act. viscosus — это белковые фимбрии, которые прикрепляются к белкам пролина на пелликуле.
В связи с размножением прикрепленных бактерий экологический состав микробного налета изменяется. Создаются условия и для внедрения в ее состав облигатных анаэробов — наступает третий этап формирования зубной бляшки.
3. Вторичная колонизация и созревание бляшки. На этом этапе появляются новые пародонтопатогенные микроорганизмы:
• Prevotella intermedia;
• Fusobacterium nucleatum;
• Porphyromonas gingivalis;
• Capnocytophaga saprofytum.
Переход грамположительного состава бляшки к грамотрицательному — это строгое и последовательное структурное изменение. Формирование достаточно устойчивых микробных ассоциаций объясняется целесообразностью или взаимовыгодными отношениями между микробными ассоциациями, в которых продукты метаболизма одних микроорганизмов служат источником питания для других.
В частности, в ходе разрушения и утилизации тканевых белков выделяется аммиак, который микробы используют в качестве источника оксида азота. Продукт распада гемоглобина — гемин — необходим для роста Porphyromonas gingivalis, стероиды — для роста Prevotella intermedia.
Установленный факт различной патогенности микробных скоплений и отдельных микроорганизмов в отношении тканей хозяина (в нашем случае — тканей пародонта) тоже имеет объяснение. Так, источником питания для грамположительных микроорганизмов являются углеводы. В процессе их утилизации микроорганизмы выделяют экзотоксины, к которым ткани организма устойчивы. Для грамотрицательных микроорганизмов источником питания являются тканевые белки. Именно поэтому в целях обеспечения условий для своей жизнедеятельности грамотрицательные микроорганизмы растворяют живые ткани с помощью мощных эндотоксинов и ферментов.
Кроме плотно прикрепленной к зубу бляшки существуют рыхлые микробные скопления на стенках внутри кармана. Роль зубной бляшки и неприкрепленных микроорганизмов в развитии патологического процесса неодинакова: доминирует влияние бляшки, но в ряде случаев именно рыхло прикрепленные микроорганизмы играют значительную роль в течении агрессивных форм пародонтита и в наступлении фазы обострения воспаления.
Таким образом, прогрессирующий рост бляшки и динамика ее микробного состава в своей основе являются весьма упорядоченным процессом, который в то же время отличается и существенной индивидуальностью.
Различают три фазы созревания микробной бляшки, или биопленки.
• Через 2 дня после прекращения чистки зубов происходит пролиферация грамположительных кокков. Формируется бактериальная пленка толщиной менее 1 мм, состоящая преимущественно из коков. Такой состав пленки характерен и для нормального состояния тканей пародонтная медицинская • Через 1—4 дня появляются в значительном количестве фузобактерии и филаменты. В течение этого времени может возникнуть гингивит. Состав флоры в этот период типичен для гингивита: множество кокков, филаментов, грамположительные и грамотрицательные формы.
• Через 4—9 дней появляются спирохеты и спириллы. Состав флоры может быть идентичен таковому при пародонтите.
Представленные закономерности в большей степени присущи типичной, или хронической, форме гингивита и пародонтита.
Следует особо выделить состав микрофлоры при атипичных формах пародонтита, в частности при ювенильном пародонтите. Для этой формы заболевания характерно очень скудное скопление микробных масс и зубных отложений. Поверхность цемента зубов покрывают слабо прикрепленные филаменты. В основном в налете прослеживается грамотрицательная микрофлора, состав которой гораздо проще, чем при хроническом гингивите или пародонтите.
Что такое гингивит? Причины возникновения, диагностику и методы лечения разберем в статье доктора Карелина Андрея Сергеевича, стоматолога-хирурга со стажем в 11 лет.

Определение болезни. Причины заболевания
Гингивит — воспалительное заболевание дёсен, которое проявляется болезненностью, отёчностью, кровоточивостью и выделением экссудата (жидкости, которую продуцируют ткани в ответ на воспаление).
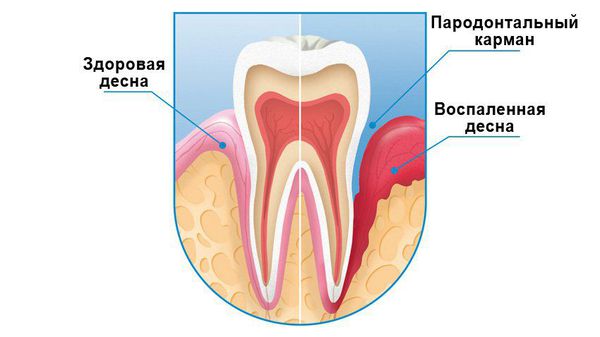
Воспалённая десна становится мягкой, шероховатой, неплотно прилегает к коронкам зубов. По данным Всемирной организации здравоохранения, более чем у 90-95 % взрослых людей присутствуют воспалительные процессы мягких тканей ротовой полости, а утрата зубов из-за воспаления дёсен и пародонта (тканей, окружающих зуб) случается в 5 раз чаще, чем от кариозных поражений [1] .
В большинстве случаев гингивит возникает из-за скопления зубного налёта в результате плохой гигиены ротовой полости. Бляшки из налёта постоянно раздражают слизистую, формируют карманы (увеличивают расстояние между зубом и мягкими тканями), в которых активно размножаются бактерии. Т. е. чаще всего причиной воспаления дёсен являются бактерии. Кроме того, гингивит может быть следствием аллергии, грибковых и вирусных инфекций.
Провоцирующие факторы в развитии воспаления дёсен:
- изменения гормонального фона;
- сахарный диабет;
- авитаминоз;
- приобретённые (ВИЧ) и врождённые иммунодефициты (синдром Ди Джорджи);
- беременность;
- лейкоз;
- недостаток витамина С;
- отягощённая наследственность (есть близкие родственники, которые страдали воспалительными заболеваниями дёсен);
- повреждение десны [1] .
Повреждения слизистой могут возникать при неправильном прикусе, стоматологических манипуляциях, воздействии агрессивных химических веществ, использовании жёсткой зубной щётки, употреблении твёрдой пищи. Даже незначительная травма эпителия — это входные ворота для инфекции.
К ятрогенным (связанным с врачебными манипуляциями) факторам, способствующим воспалению, относятся острые края зубных протезов, коронок, неотполированные пломбы, прилегающие к десне.
Симптомы гингивита
На начальной стадии заболевания пациенты жалуются на дискомфорт в ротовой полости. При осмотре поражённый участок десны гиперемирован (т. е. имеется покраснение), увеличен в объёме. Возможна кровоточивость во время употребления твёрдой пищи и чистки зубов. Боли на ранней стадии заболевания, как правило, ещё нет. Многие пациенты жалуются на повышенное слюновыделение.
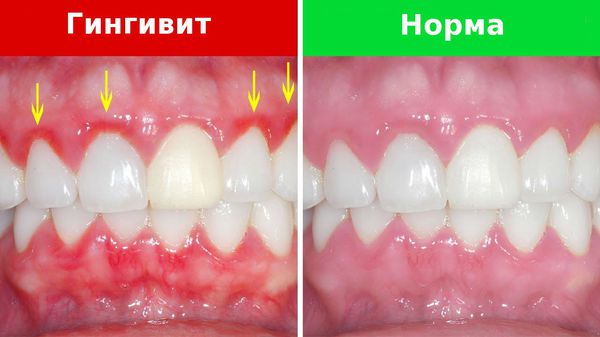
Воспалённая десна отстаёт от поверхности зуба, в образовавшейся полости скапливаются остатки пищи, появляется неприятный запах изо рта. Если не лечить заболевание, в кармане активно размножаются бактерии, развивается кариес шейки зуба [2] .
Со временем появляется боль в десне, которая усиливается во время приёма пищи и при стоматологическом осмотре. Особенно болевой синдром выражен при употреблении горячего, холодного и кислого. При выраженном воспалении или распространённом процессе могут появляться не только местные, но и общие симптомы: повышение температуры, слабость, повышенная утомляемость, раздражительность.
При осмотре стоматолог видит изменение цвета поражённых участков слизистой, гипертрофию (увеличение объёма) межзубных сосочков и края десны. Обычно в области воспаления присутствует зубной налёт, зубной камень и поражения кариесом. При обследовании стоматологическим инструментом десна может кровоточить. При хроническом воспалении клиническая картина стёрта, но может наблюдаться выраженная гипертрофия мягких тканей. При длительно текущем процессе разросшаяся десна может закрывать практически всю коронку зуба. При десквамативной ( с появлением пузырьков на дёснах) и язвенной форме гингивита на десне могут образовываться пузырьки и язвочки [3] .
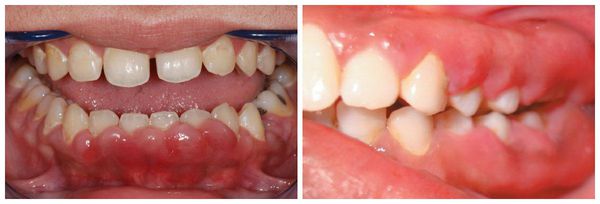
Патогенез гингивита
Развитие гингивита начинается с формирования бляшек из зубного налёта. Они образуются после отсутствия полноценной гигиены ротовой полости в течение 1-2 дней. Наиболее частые места образования бляшек — межзубные промежутки и пришеечная зона.
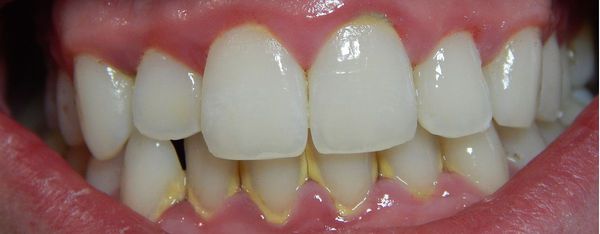
Из слюны и выделяемой десной жидкости формируется плёнка — пелликула. В норме она выполняет защитную функцию, но на начальных стадиях гингивита способствует адгезии (прилипанию) бактерий, которые присутствуют в ротовой полости даже у здорового человека. Обычно это аэробные кокки и палочки.
Микроорганизмы активно размножаются, в глубине их колонии образуется анаэробная (бескислородная) среда. Это создает оптимальные условия для размножения агрессивной грамотрицательной микрофлоры. Эти бактерии продуцируют токсины, которые способны проникать в ткани и разрушать слизистую оболочку, что приводит к эрозивным изменениям эпителия.
Организм пытается противостоять повреждающему действию и в ответ запускает воспалительную реакцию с целью уничтожения патогенных факторов . В некоторых случаях иммунитет самостоятельно справляется с микрофлорой, но чаще воспаление прогрессирует или приобретает хронический характер.
Разрушающее действие микроорганизмов и воспалительный процесс ведут к ухудшению микроциркуляции в десне, снижению активности антиоксидантных защитных механизмов. Это приводит к агрессивному воздействию на эпителий факторов системы комплемента (защитных белков, циркулирующих в крови), что вызывает прогрессирующее разрушение слизистой. У пациентов с дефектами иммунитета, гормональными нарушениями, болезнями крови, травматическим повреждением дёсен и истончённой слизистой мягкие ткани более уязвимы, процесс их деструкции идёт более активно.
Если патологический процесс активно развивается, в мягких тканях возрастает количество клеток иммунной системы (лимфоцитов и макрофагов). Они разрушают клетки и фибриллярные структуры цитоплазмы ( жесткие, параллельно расположенные волокна, которые определяют форму клетки) . Это приводит к расширению пространства между десной и зубом, истончению эпителиального слоя.
Воспаление может полностью пройти с наступлением выздоровления, либо перейти в хроническую форму. Во втором случае процессы регенерации нарушаются, эпителий замещается грануляционной тканью (соединительной тканью, которая образуется при заживлении тканевых дефектов), которая может сильно разрастаться, прикрывая коронку зуба [4] .
Классификация и стадии развития гингивита
Согласно Международной классификации болезней 10 пересмотра (МКБ-10), выделяют острое и хроническое течение гингивита:
- При остром течении пациент ощущает болезненность и дискомфорт, часто бывают кровотечения, мягкие ткани гиперемированы.
- Хроническое воспаление иногда вызывает дискомфорт, пациента беспокоит неприятный запах изо рта, край десны часто утолщён в виде валика. Хроническую форму гингивита делят на такие виды:
- хронический без дополнительных уточнений;
- десквамативный (с появлением пузырьков на дёснах);
- гиперпластический (проявляется разрастанием десны);
- простой маргинальный (поражающий край десны);
- язвенный [5] .
По распространённости воспалительного процесса гингивит может быть локальным либо генерализованным (распространённым). В последнем случае часто выявляются общие симптомы в виде повышения температуры и слабости.
По тяжести течения:
- Лёгкие поражения слизистой — поражаются только межзубные сосочки.
- Поражения средней тяжести — в воспалительный процесс вовлекается свободный край десны.
- Тяжёлые поражения слизистой — воспаляются мягкие ткани, прикреплённые к зубу.
По морфологическим признакам:
- Катаральный гингивит. Х арактерно выделение большого количества экссудата, выраженное покраснение слизистой, отёчность, болезненность, локальное повышение температуры.
- Гипертрофический гингивит. Сосочки между зубами увеличиваются, со временем они могут полностью закрывать коронки зубов. Десна приобретает синюшный оттенок, кровоточит во время еды, чистки зубов или при стоматологическом осмотре, формируются глубокие десневые карманы.
- Язвенный гингивит. Слизистая приобретает серый оттенок, видны очаги деструкции [6] .
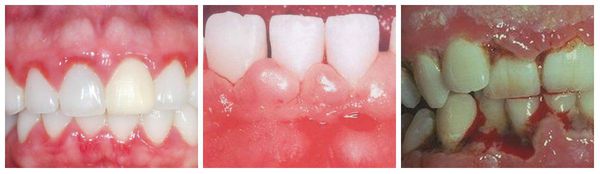
На ранней стадии заболевания отмечается покраснение, припухлость, кровоточивость дёсен. Если вовремя обратиться к стоматологу, можно быстро снять воспаление и полностью восстановить мягкие ткани. Если не лечить заболевание, развиваются деструктивные процессы в десне, дефекты замещаются грануляционной тканью. Если воспаление будет прогрессировать и дальше, процесс может перейти на ткани пародонта, что может привести к утрате зубов.
Осложнения гингивита
Гингивит — это не такое безобидное заболевание, как кажется некоторым пациентам. Многие полагают, что воспаление пройдёт само, не оставив следа. Это возможно только при небольшом очаге поражения и хорошем иммунитете. Следует помнить, что воспалённая десна — это источник инфекции, которая может распространяться в ротовой полости и вызывать серьёзные последствия. Именно поэтому при первых симптомах нужно обращаться за медицинской помощью. Самые распространённые осложнения гингивита:
- язвенно-некротические изменения слизистой;
- пародонтит (воспаление пародонта);
- периодонтит (воспаление соединительной связки, фиксирующей зуб в кости челюсти) ;
- распространение инфекции за пределы ротовой полости.
При гингивите на слизистую полости рта действуют иммунные силы организма (лимфоциты и макрофаги) и токсины, которые выделяют бактерии. Если воспалительный процесс вовремя не купировать, эпителий начнёт разрушаться. На начальных стадиях этот процесс обратим, но при длительном течении заболевания десна гипертрофируется за счёт грануляционной ткани. В этом случае терапевтическое лечение может быть неэффективным.
Микрофлора, которая поразила десну, может распространяться на ткани пародонта. Это приводит к шаткости зубов, а со временем — к их утрате. Таким образом, вследствие заболеваний дёсен можно потерять совершенно здоровые зубы.
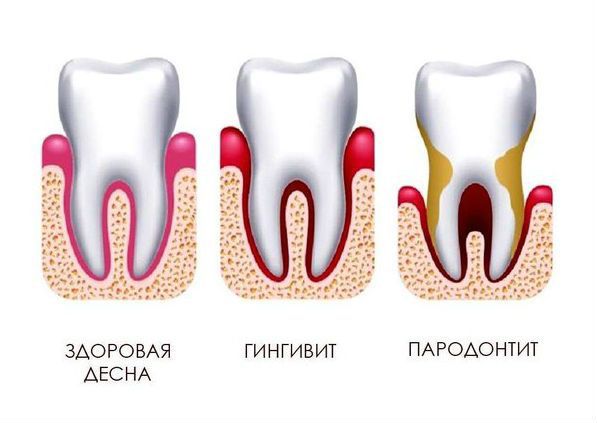
Бактерии, размножающиеся между десной и зубом, могут вызывать пришеечный кариес. Кроме того, это постоянный источник неприятного запаха изо рта, от которого не избавит даже чистка зубов и использование растворов для полоскания и освежения дыхания.
В тяжёлых случаях воспалительный процесс переходит на костную ткань челюсти. Это очень опасное осложнение, которое сложно поддаётся лечению и может привести к необратимым изменениям лицевого скелета, утрате нескольких или всех зубов. Возможно развитие остеомиелита челюсти, когда разрушается костная ткань и образуются свищи — ходы, через которые гной из области корня зуба выходит в ротовую полость. Заболевание существенно ухудшает состояние пациента, приводит к общей интоксикации: слабости, снижению работоспособности, повышению температуры тела, боли в мышцах и суставах.
Инфекция по кровеносному руслу может распространяться далеко за пределы ротовой полости. В этом случае возможно развитие воспалительных заболеваний ЛОР-органов: ангины Винсента, парафарингеального абсцесса. Воспаляться могут не только соседние органы. С током крови инфекция может попасть в любой орган. Если гингивит вызван стрептококком, у пациента может развиться миокардит (воспаление сердечной мышцы) или пиелонефрит ( воспаление ткани почек) [7] .
Диагностика гингивита
Диагностика начинается с того, что врач слушает жалобы пациента и собирает анамнез. Обычно клиническая картина довольно типична. Необходимо выяснить, как давно появились первые симптомы, проводилось ли какое-либо лечение. При сборе анамнеза нужно обратить внимание на наличие хронических заболеваний, гормональных нарушений, оценить состояние иммунитета. Эти факторы важны при выборе тактики лечения.
При осмотре стоматолог без труда выявит изменённый участок десны. Задача доктора — определить тяжесть поражения, оценить распространённость процесса, выявить, задействованы ли в воспалении ткани пародонта и периодонта. Также нужно выяснить причину гингивита и устранить её. Если десна постоянно повреждается острым краем коронки, то снятие воспаления — это временная мера. Без устранения повреждающего фактора болезнь будет рецидивировать.
Если есть подозрение на распространение процесса за пределы десны, необходимы дополнительные обследования, позволяющие оценить состояние корня зуба, костной ткани челюсти, пародонта. С этой целью широко используют рентгенографию [8] .
Если процесс генерализован (распространён по организму), пациенту необходимо сдать общий анализ крови. Он позволяет оценить ответ организма на воспаление и определить степень тяжести состояния.
Для диагностики используют и дополнительные методы:
- проба Шиллера — Писарева — определение гликогена, содержание которого резко возрастает при воспалении;
- определение индекса кровоточивости;
- проба Кулаженко — определение стойкости и проницаемости микроциркуляторного русла;
- полярография — определение уровня кислорода в тканях пародонта;
- реопародонтография — исследование функционального состояния сосудов тканей пародонта путём регистрации пульсирующего в них потока крови .
Часто гингивит выявляется во время профилактического осмотра. При этом пациенты не предъявляют жалоб, так как на ранних стадиях процесс может протекать бессимптомно. Именно поэтому важно каждые 6 месяцев посещать стоматолога.
Лечение гингивита
Для успешного лечения нужно в первую очередь устранить причину воспаления. С этой целью обязательно проводится удаление налёта и зубного камня.
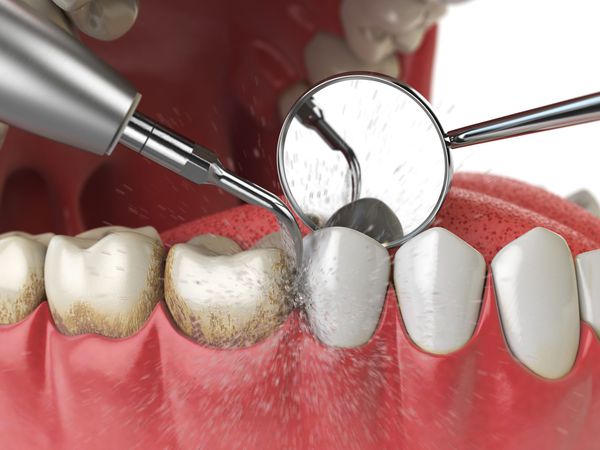
При начальных стадиях заболевания этой процедуры и использования местных антисептиков достаточно. Для снятия воспаления используется метронидазол, хлоргексидин, настои шалфея и ромашки. Для улучшения регенерации показано местное применение "Солкосерила", облепихового масла.
Если коронка, пломба или скол зуба приводят к постоянному повреждению десны, необходимо провести лечение зуба и устранить повреждающий фактор. К десне должна прилегать гладкая поверхность без шероховатостей и острых краёв.
Если воспаление имеет распространённый характер, нарушено общее самочувствие пациента, а в анализе крови есть признаки воспаления, назначают курс антибиотиков, активных в отношении грамотрицательной флоры. Также используют иммуностимуляторы и витамины [2] .
Если у пациента выражен болевой синдром, к терапии добавляют обезболивающие препараты. С этой целью используют препараты из группы НПВС (нестероидных противовоспалительных средств).
В комплексной терапии гингивита в качестве дополнительного лечения иногда используются физиотерапевтические методы лечения:
- электрофорез с алоэ, аскорбиновой кислотой;
- фонофорез с гепариновой мазью;
- облучение кварцевой лампой;
- лазеротерапия [12] ;
- дарсонвализация;
- вакуумный массаж десен [9] .
При гипертрофической форме гингивита перечисленные лечебные мероприятия могут не дать положительного результата. В таком случае для уплотнения разросшихся мягких тканей в межзубные сосочки делают инъекции склерозирующих средств. Если таким способом устранить разросшуюся грануляционную ткань не удалось, используют криодеструкцию (заморозку и удаление тканей с помощью жидкого азота), диатермокоагуляцию (иссечение слизистых тканей при помощи горячего инструмента) или удаление с помощью скальпеля — гингивэктомию [10] .
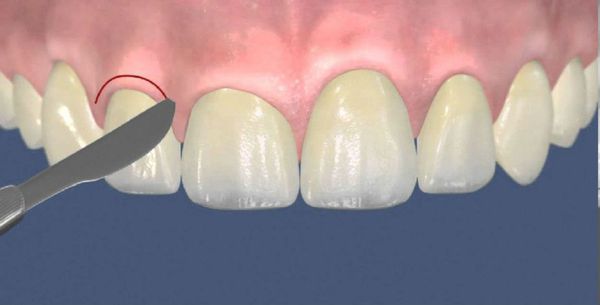
Прогноз. Профилактика
При своевременном начале лечения заболевания, особенно при катаральной форме (характеризуется покраснением и отёчностью дёсен), прогноз всегда благоприятный. Мягкие ткани полностью восстанавливаются, а при устранении причины воспаления оно не развивается снова.
При обширном поражении и разрастании десны приходится частично удалять десневые сосочки, это может привести к обнажению шеек зубов. Если таким пациентам регулярно не проводить профилактические мероприятия, быстро развивается пародонтит.
Если не пройти курс лечения, воспаление дёсен, как правило, заканчивается утратой зубов. Микрофлора поражает ткани пародонта, фиксирующие зуб, он начинает шататься и со временем выпадает.
Часто неблагоприятный прогноз при гингивите бывает у больных сахарным диабетом. Нарушение микроциркуляции, обусловленное основным заболеванием, приводит к нарушению трофики тканей, замедляет процессы регенерации. Таким пациентам необходима постоянная поддерживающая терапия, которая замедляет наступление необратимых изменений, а также контроль уровня глюкозы в крови.
Для профилактики гингивита нужно соблюдать следующие рекомендации:
- регулярно чистить зубы (2 раза в день);
- использовать щётку с мягкой щетиной;
- после еды пользоваться зубной нитью и ополаскивателем;
- каждые шесть месяцев проводить профессиональную чистку зубов у стоматолога;
- не пропускать плановые визиты к доктору;
- своевременно лечить кариес;
- если пломба или коронка травмирует десну, срочно обращаться к стоматологу;
- избегать употребления твёрдой пищи, травмирующей дёсны.
Если кровоточивость дёсен отмечается более трёх суток, не нужно заниматься самолечением, необходимо обратиться за медицинской помощью. Начальные стадии гингивита можно быстро вылечить с помощью местной терапии. Запущенное заболевание плохо поддаётся лечению и может закончиться необратимыми последствиями [11] .
Согласно современным представлениям, важнейшую роль в возникновении и развитии кариеса играет инфекционный фактор. Кариесогенное действие микроорганизмов связывают с образованием ими зубной бляшки. По данным Bowden (1985), зубная бляшка содержит следующие виды микроорганизмов: факультативные стрептококки — 27 %, факультативные дифтероиды — 23 %, анаэробные дифтероиды — 18 %, пентостреп-тококки — 13 %, вейлонеллы — 6 %, бактероиды — 4 %, фузобактерии — 4 %, нейссерии — 3 %, вибрионы — 2 %. Из стрептококков преобладают Str. mutans, Str. sanguis, Str. mitis.
Установлено, что кариесогенные микробы избирательно накапливаются на поверхностях зубов, наиболее часто поражающихся кариесом (области фиссур и межзубные поверхности). Особено много Str. mutans у лиц, подверженных кариесу, и при множественном кариесе.
Зубная бляшка представляет собой структурированное образование, состоящее из микроорганизмов, расположенных на полисахаридной основе, плотно прикрепленное к поверхности зуба. В состав зубной бляшки, кроме микроорганизмов, входят лейкоциты, эпителиальные клетки, макрофаги. Она растет за счет постепенного наслоения новых бактерий. Кариесогенность зубной бляшки во многом зависит от степени ее накопления и давности.
В течение 1-2-х суток образования бляшки в ней преобладает Str. mutans, кариесогенность которого определяется выработкой им больших количеств молочной кислоты в присутствии углеводов. Это приводит к повышению проницаемости эмали, происходит кислотное растворение в наименее устойчивых участках эмали с последующим проникновением кислот в подповерхностный слой эмали и ее деминерализацией. Дальнейшее образование органических кислот на поверхности эмали усиливает процессы деминерализации, что приводит к образованию микрополостей в эмали, заполненных микроорганизмами и продуктами их метаболизма.
Определено, что чем выше скорость образования зубной бляшки, тем более выражено ее кариесогенное действие. У детей, имеющих повышенный индекс зубной бляшки, прирост интенсивности кариеса происходит в три раза быстрее, чем у детей с низким индексом. Помимо этого, кариес у детей развивается в тех случаях, если в микрофлоре зубной бляшки преобладает Str. mutans.
Однако на кариесогенность зубной бляшки влияют многочисленные факторы, в частности, микрофлора полости рта, количество употребляемых углеводов, количественный и качественный состав слюны, ее физико-химические свойства, содержание в ней минеральных компонентов: чем выше уровень кальция и фосфора, тем меньше кариесогенный потенциал бляшки.
В механизме влияния зубной бляшки на эмаль большая роль принадлежит ферментам микроорганизмов. Ферментативная деятельность этих бактерий приводит к повышенной проницаемости эмали. Известно также, что кариесогенные штаммы микроорганизмов зубной бляшки могут влиять на органическую фракцию эмали зуба. Их действие может особенно проявляться после растворения неорганической фазы эмали.
В то же время зубная бляшка на поверхности зуба механически изолирует подлежащую эмаль от воздействия слюны, являющейся немаловажным минерализующим и защитным фактором.
Определенное влияние на активность зубной бляшки оказывает фтор. Под действием фтора частично теряется способность микроорганизмов вырабатывать кислоту.
Зубная бляшка играет важную роль в развитии болезней пародонта. В возникновении воспалительного процесса в тканях пародонта участвуют микроорганизмы бляшки.
Характер влияния микроорганизмов зубной бляшки на пародонт разносторонний. Микробные ферменты способны повышать проницаемость капилляров, вызывать нарушение проницаемости эпителиальной мембраны и проникать в подэпителиальную соединительнотканную основу слизистой оболочки десны.
Конечно, на состояние зубной бляшки значительное влияние оказывают факторы окружающей среды. К ним относятся иммунобиологическая система жидкости десневой борозды, гидролитические ферменты секретов слюнных желез и ротовой жидкости, секреторные иммуноглобулины, бактериофаги, кислоты, углеводы. Эти биологические факторы находятся в сложном взаимодействии с микрофлорой полости рта и способны ослаблять или усиливать ее патогенный потенциал. Важную роль в поддержании биологического равновесия между бактериальным симбиозом и тканями полости рта играют общие факторы, регулирующие метаболизм тканей полости рта и от которых зависит соответствующая реакция на различные патологические воздействия.
Зубной камень образуется в результате отложения в зубном налете неорганических веществ: в коллоидной основе налета откладываются минеральные соли. При этом изменяется соотношение между микроорганизмами, спущенным эпителием, мукопротеидами и происходит импрегнация зубного налета кристаллами фосфата кальция. Обычно начало минерализации зубного налета происходит через 1-2 дня после его образования.
Механизм влияния зубного камня на пародонт разносторонний. Ввиду плотной консистенции зубной камень оказывает механическое давление, создает условия микротравмы эпителия десны и маргинальных волокон периодонта. Следует также учитывать химическое воздействие зубного камня на пародонт вследствие наличия в нем некоторых токсических элементов. Последние образуют в камне оксиды металлов (пентаксид ванадия, оксид свинца, меди, железа и др.).

Изучение микробиологических аспектов этиологии и патогенеза болезней пародонта является актуальной проблемой стоматологии. Обоснование роли определенных видов микроорганизмов в развитии патологического процесса, определение условий и механизмов реализации неповреждающего действия открывают новые перспективы для профилактики и лечения данных заболеваний. Уже установлена ведущая роль стрептококков в возникновении кариозных повреждений эмали зубов, а также значение отдельных сероваров Streptococcus mutans в этом процессе [1]. Продолжается выяснение влияния инфекционного фактора на этиологию и других форм патологических процессов в полости рта.
В полости рта местные микроорганизмы часто ассоциируются с этиологией двух широко распространенных патологических процессов - кариес и перидонтальные заболевания. Оральная патология, как правило, развивается после нарушения сбалансированного состояния среди местной микрофлоры, что приводит к появлению потенциально патогенных микроорганизмов [2].
В полости рта существующая важная среда обеспечивает относительно стабильную температуру (от 34º до 36 ºС) и рН ближе к нейтральной в большинстве участков, таким образом, поддерживается рост широкого разнообразия микроорганизмов. Вместе с тем ротовую полость нельзя рассматривать как однообразную среду. В ней можно определить несколько участков - мест для обитания микроорганизмов, каждое из которых характеризуется разнообразными физико-химическими факторами и таким образом поддерживает рост и развитие разной микробной общины. Это происходит частично из-за большого анатомического разнообразия полости рта, а также взаимосвязи между разными анатомическими структурами [3, 4].
Оральная микрофлора у людей весьма сложная и разнообразная. Она включает более чем 300 бактериальных видов, к которым можно добавить Protozoa, грибы, а также микоплазмы и актиномицеты. Их распространение меняется качественно и количественно в зависимости от их местообитания [5].
Как известно, количественный критерий имеет важное значение при установлении возбудителя инфекционного процесса. Возрастание доли определенного вида среди остальных микроорганизмов в течение заболевания, а также доминирование его в популяции, населяющей очаг поражения, может косвенно свидетельствовать об этиологической роли данного вида [6, 7]. У здоровых людей десневая бороздка содержит ограниченное количество матрикса зубной бляшки. Более 30% всей культивируемой микрофлоры такой бляшки составляют грамположительные палочки. Около 90% из них - это представители актиномицетов (Actinomyces viscosus, A.naeslundii, A.israelli) [1]. Прекращение гигиенического ухода за полостью рта ведет к накоплению матрикса бляшки. Это сопровождается, с одной стороны, развитием гингивита, а с другой - возрастанием доли актиномицетов, которые постепенно становятся доминирующей флорой. В зрелой, ненарушенной зубной бляшке актиномицеты составляют примерно половину всех микроорганизмов: A.viscosus и A.naeslundii - 38,4 %, A.israelli - 10 %, A.odontolyticus - 3,5 % [1].
На модели экспериментального гингивита показано, что количество A.viscosus и A. israelli увеличивается параллельно с нарастанием интенсивности воспаления десен. Другими исследователями также отмечена прямая корреляция между выраженностью клинических симптомов гингивита и содержанием A.viscosus в материале зубной бляшки.
При микробиологическом исследовании десневой жидкости и зубной бляшки у больных пародонтитом определено, что численность популяции A.viscosus и Rothia dentocariosa в области поражения оказалась больше, чем в непораженных участках. На преобладание актиномицетов в зубной бляшке при пародонтите указывают, в то время как другие авторы наблюдали высокое содержание R.dentocariosa, A.naeslundii, A.viscosus лишь у больных с минимальной активностью процесса.
Другая форма патологии органов рта, при которой доминируют актиномицеты - пришеечный кариес. В таких кариозных поражениях обнаружено более 50% A.viscosus, A.naeslundii, A.odontolyticus.
Поверхность слизистой полости рта омывается стабильно двумя важными физиологическими жидкостями - слюна и жидкость гингивальной щели. Они существенно важны для поддержания экосистемы оральной полости, обеспечивая ее при этом водой, питательными веществами, адгезией микроорганизмов, а также антимикробными факторами. Супрагингивальная среда промывается слюной, в то время сабгингивальный регион (гингивальная щель) промывается в основном жидкостью гингивальной щели [5].
В настоящей работе рассматривается вопрос о патологическом значении ферментирующих актиномицетов, а также микробиологические и иммунологические аспекты при пародонтите и гингивите с антиномикотической этиологией.
Материал и методы
Микробиологические исследования патологического материала проводились на кафедре микробиологии и иммунологии АМУ. Проведено микробиологическое исследование мазков ротовой полости больных пародонтитом и гингивитом. В ходе работы 139 больных, проходивших обследование и лечение в стоматологической поликлинике АМУ, были разделены на 2 группы. 1 группу составили 56 больных пародонтитом, 2 группу - 83 больных с гингивитом. А также каждая группа была разделена на две подгруппы: «а» - с актиномикотической этиологической, «b» - больные, у которых этиологическим аспектом служили другие микроорганизмы (бактерии и грибы).
Материалом для исследования служили мазки из ротовой полости, материалы пародонтального кармана зубов и из гингивиальной щели. Параллельно приготовлениям мазков образец поместили в 5 м транспортную среду (0,06 % обогащенную тиогликолевую среду), морфологические и тинктональные свойства изучали при окрашивании препаратов по Грамму, Цилью Нельсону и Романовскому Гимзе.
Для выделения культур Actinomyces в качестве плотной среды использовали тиогликолевую, крахмаламмиачную, а также среду Сабуро, кровяной агар.
Инкубации при 35-37 ºС проводили в анаэробных и аэробных условиях в течение 15 дней. Исследовали морфологические, культуральные, физиологические и биохимические свойства выделенных изолятов по общепринятому методу. Колонии изучали при помощи лупы и микроскопа.
Концентрацию иммуноглобулинов классов А, М, G провоспалительных цитокинов (TNFα, IL-1) в сыворотке крови, а также уровня sIgA в слюне определяли методом твердофазного иммуноферментного анализа. Для изучения количества субпопуляции Т-лимфоцитов (СD3, СD4, СD8), а также CD22 в крови был использован коммерческий тест-набор, «колоноспектр», предназначенный для определения дифференцированных антигенов лейкоцитов человека методом «иммуноперексидазного окрашивания клеток».
Результаты и обсуждение
В результате бактериологического и бактериоскопического анализа больных гингивитом и пародонтитом был выявлен актиномицет в ассоциации с другими микроорганизмами. У больных пародонтитом (50 человек) у 23 (46%) были выделены актиномицеты в ассоциации с другими микроорганизмами, у 27 (54,0%) были выделены лишь другие микроорганизмы. У больных гингивитом (83 человека) у 33 (40%) были выделены актиномицеты в ассоциации с другими микроорганизмами, а у 50 (60%) только другие микроорганизмы. При пародонтите часто выделены Act.odontolyticus, Act.viscosus, Act.israelii, Act.eriocsonii, Act.albicans, Act.nauslandii, Act.spp. А при гингивите были выделены актиномицеты - Act.odontolyticus, Act.viscosus, Act.israelii, Act.eriocsonii. Все эти актиномицеты были выделены в ассоциации с аэробными и анаэробными микроорганизмами.
При пародонтите были выделены следующие микроорганизмы: S.aureus, α гемолитические стрептококки, E.coli, C.albicans, A.actinomycetimocomitans, Fuzabacterium spp., грамположительные анаэробные кокки, бактероиды. А при гингивите актиномицеты были выделены в ассоциации с аэробными бактериями - S.aureus, α гемолитические стрептококки, Neisseria spp., C.albicans, Micrococcus spp., A.actinomycetemcomitans, из анаэробных - грамположительные анаэробные кокки, Porphyromonos qinqivalis.
Исходя из этих данных, можно предположить, что при возникновении таких болезней, как гингивит и пародонтит ротовой полости, значительную роль играют актиномицеты и так называемые «сопутствующие микроорганизмы» (бактерии и грибы), и они создают локальные условия для патологического процесса [6]. Поэтому необходимо изолировать и идентифицировать выделенные актиномицеты, а также другие микроорганизмы из очагов актиномикотических поражений. Развитие актиномикоза следует рассматривать как проявление аутоинфекции, которая возникает и прогрессирует на фоне гнойно-воспалительных заболеваний, травм, иммунодефицитных состояний. В ряде случаев для возникновения заболевания необходимо наличие гиперсенсибилизации или ассоциации с другими бактериями, обитающими в организме (микст инфекция) [8, 9]. При этом сопутствующая микрофлора значительно усугубляет тяжесть поражения и нередко способствует ошибкам при лабораторной диагностике заболевания, поскольку актиномицеты часто при микроскопическом исследовании не выявляются, а на питательных средах их видимый рост проявляется намного позже (на 7-14 день) сопутствующей микрофлоры, к тому же в зависимости от вида актиномицетов для их культивирования необходимы аэробные или анаэробные условия, что не всегда учитывается в практике врачей. Необходимо отметить, что при воспалительных заболеваниях пародонта наряду с увеличением количества актиномицетов наблюдается изменение морфологии этих бактерий. В частности, зубная бляшка здоровых людей представлена палочко- и кокковидными бактериями, а у больных гингивитом, пародонтитом она содержит плотные агрегаты нитевидных грамположительных бактерий.
В дальнейших исследованиях были проанализированы сравнительные показатели иммунной системы у больных пародонтитом и гингивитом актиномикотической этиологии, а также без нее.
У больных пародонтитом (IgA - 1,70±0,09 мг/ мл, IgM - 1,5±0,01 мг/ мл, IgG - 13,8±0,09 мг/ мл) и гингивитом (IgA - 1,25±0,1 мг/мл, IgM - 0,98±0,01 мг/ мл, IgG - 6,0±0,1 мг/мл) с актиномикотической этиологией анализ средних уровней иммуноглобулинов в сыворотке крови показал достоверное понижение, чем у больных, у которых этиологическим агентом служили другие бактерии и грибы (пародонтиты: IgA - 8,77±0,1 мг/ мл, IgM - 3,91±0,2 мг/мл, IgG - 23,7±0,04 мг/ мл; гингивиты: IgA - 2,72±0,02 мг/мл, IgM - 1,7±0,01 мг/мл, IgG - 12,7±0,02 мг/мл). А концентрация sIgA у больных с актиномикотическкой этиологией была заметно понижена (пародонтит - 56,4±10,1 мг/ мл, гингивит - 45,3±9,1 мг/мл) по сравнению с нормой, а также у больных, у которых выделены другие микроорганизмы, так как в норме уровень sIgA составляет 207,5±92,2 мг/мл.
У больных пародонтитом и гингивитом, у которых заболевания вызваны актиномицетами в сочетании с другими микроорганизмами, в уровне цитокинов в сыворотке крови отмечалось незначительное увеличение (у больных гингивитом: TNFα - 77,3±3,5, IL-1 - 78,4±3,3; у больных пародонтитом: TNFα - 71,8±6,3, IL-1 - 72,3±7,5). Можно полагать, что отмеченные изменения в концентрации цитокинов обусловлены у больных с остротой воспалительных процессов. По всей вероятности, как пародонтиту, так и гингивиту, обусловленным актиномицетами в ассоциации с другими микроорганизмами, свойственно было хроническое течение заболевания. Напротив, у больных пародонтитом и гингивитом, вызванным другими микроорганизмами, воспалительный процесс (как гнойный, так и без него) протекал остро, что сказывалось на содержании провоспалительных цитокинов (у больных гингивитом: TNFα - 102,5±10,4, IL-1 - 106,5±10,7; у больных пародонтитом: TNFα - 169,6±13,0, IL-1 - 236,8±11,5).
Результаты количественного определения субпопуляции Т-лимфоцитов показали, что содержание CD3 (у больных гингивитом - 48,2±10,0%, у больных пародонтитом - 38,6±8,3%), CD4 (гингивит - 29,9±7,5%, пародонтит - 27,3±7,0%), CD8 (гингивит - 21,0±5,9%, пародонтит - 14,5±3,5%), а также CD22 (гингивит - 9,5±3,1%, пародонтит - 4,5±1,1%) у всех больных с актиномикотической этиологией, были снижены по сравнению с лицами контрольной группы (CD3 - 65,5%, CD4 - 38,5%, CD8 - 29,5%, CD22 - 12,8%) (р
Читайте также:

