Типы реакции гиперчувствительности в тканях пародонта
Опубликовано: 25.04.2024
Содержание иммуноглобулинов различных классов в сыворотке крови определяют по методу Manchini и соавт. (1965). Систематическое изучение иммунологических показателей у пациентов с заболеваниями пародонта не выявило у них существенных нарушений гуморального иммунитета. Об этом же свидетельствуют результаты исследований McArthur, Clark (1993), которые указывают на отсутствие значимых изменений уровня иммуноглобулинов при ВЗП.
Вместе с тем показатели сывороточных антител к пародонтопатогенным бактериям могут быть в определенной мере использованы с целью прогноза течения процесса либо объяснения его повышенной активности.
Так, иммунологические исследования показали, что у пациентов с ювенильным пародонтитом и БПП происходит значительное повышение количества сывороточных антител IgG к A. actinomycetemcomitans, в частности IgG 1 и IgG3, по сравнению с пациентами с типичными формами пародонтита. В отдельных работах выявлено наличие высокого титра IgG2 к липополисахаридам пяти серотипов Л. actinomycetemcomitans у пациентов с БПП, который не зависел от серотипа А.
Цитотоксические реакции наблюдаются в случаях, когда антитела реагируют непосредственно с антигенами, присутствующими на клетках тканей, либо с антигенами — натуральными тканевыми компонентами. Итогом этих взаимодействий является разрушение тканевых структур. Чаще всего такие цитотоксические антитела представлены иммуноглобулинами классов G и М. Кроме того, в процессе их связывания с антигенами обычно активируется и система комплемента.
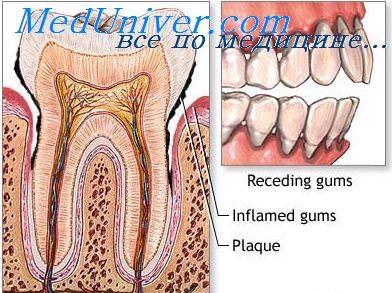
Подтверждением наличия цитотоксических реакций является повышение содержания в десневой жидкости компонентов расщепления комплемента — белков G3a, G5a, а также иммуноглобулинов и ряда белков, принимающих активное участие в индуцировании и течении воспаления: а2-макроглобулин, а,-антитрипсин, трансферрин и медленно реагирующая субстанция а.
Активация указанных соединений характерна для хронических форм воспаления пародонта.
Активация фрагмента комплемента С4 наблюдается при атипичных формах пародонтита, а именно при ювенильном пародонтите. Наличие активированного белка С4 позволяет дифференцировать типичные и атипичные формы поражений пародонта. Изучение динамики а2-макроглобулина, а,-антитрипсина в процессе лечения позволяет объективировать эффективность лечебных воздействий и прогнозировать течение процесса в пародонте.
Исследования последних лет позволяют расширить представления о патогенезе возникновения и развития заболеваний пародонта. Появилось новое направление о ключевой роли нарушений структуры и функций клеточных мембран в развитии воспаления.
Патогенные бактерии могут приводить к тканевому поражению в силу двух причин:
• собственно бактериальные и токсические воздействия;
• ответная реакция тканей пародонта на бактериальную агрессию.
Стремясь к локализации агрессии микроорганизмов, ответные реакции в тканях пародонта сами могут приводить к воспалительным и дегенеративным изменениям.
Собственно бактериальные и токсические воздействия заключаются в том, что высвобождаемые бактериями зубной бляшки ферменты оказывают литическое действие на соединительнотканный волоконный каркас пародонта (коллагеназа, протеаза), эпителиальные структуры (кератаза), поверхностные структуры клеток (нейраминидаза).
Ответные реакции тканей пародонта на повреждение включают массированную активацию комплемента и аккумуляцию лейкоцитов, прежде всего ПМЯЛ и макрофагов, а также фибробластов и тучных клеток, подвергшихся деструктивному воздействию микробных агентов. Происходит их активация с высвобождением свободнорадикальных продуктов и дегрануляция с высвобождением протеолитических ферментов и цитокинов (простагландины, лейкотриены, ин-терлейкины, фактор некроза опухолей). Эта защитная реакция направлена на разрушение бактериальных патогенов, но одновременно приводит к воспалительным и деструктивным поражениям тканей пародонта.
Микробная инвазия, первичная сосудистая реакция, различные иммунные реакции приводят к практически однотипной реакции эндотелиальной выстилки микрососудов, а именно к изменению ее адгезивных и тромбогенных свойств. Происходит гиперактивация и прикрепление ПМЯЛ и тромбоцитов к эндотелию сосудов.
Процесс накопления в очагах воспаления гиперактивированных лейкоцитов и тромбоцитов является основой развития деструкции тканей.
- Вернуться в оглавление раздела "Стоматология."
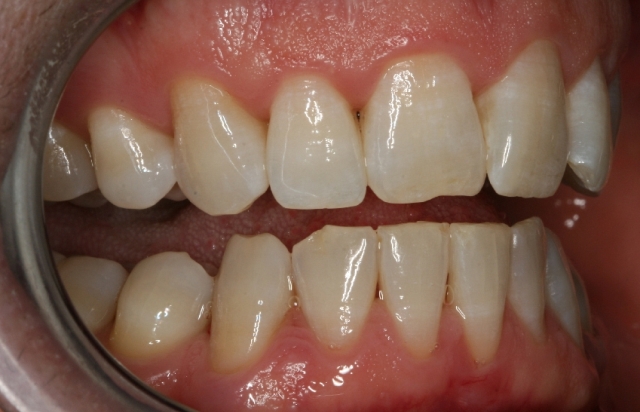
Наиболее мощным фактором, способствующим развитию и поддержанию болезней пародонта, является развитие дисбиоза в полости рта, который развивается на фоне сниженного иммунитета, или сам приводит к его изменению. Дисбиотические изменения протекают часто на фоне вторичного иммунодефицита
Воспалительные поражения пародонта возникают в результате сложного взаимодействия бактериальной инфекции и ответной реакции организма. Системные факторы и факторы внешней среды, способствующие их развитию, могут влиять и на течение процессов. Для пародонтита характерен комплекс патологических изменений, в основе которых лежат неуклонно прогрессирующее и волнообразно текущее хроническое воспаление, распространяющееся из десны на нижние отделы пародонта, и связанные с ним деструктивные процессы. Таким образом, при пародонтите, как правило, обнаруживается картина сопутствующего ему гингивита, органично входящего в комплекс патологических изменений, характерных для развившихся форм воспалительных заболеваний пародонта.
Развитие хронического пародонтита сопровождается существенными изменениями состояния иммунных механизмов защиты ротовой полости, проявляющимися в местных изменениях состава клеток крови десны (в том числе количественного соотношения популяций и субпопуляций лимфоцитов), а также содержания в слюне иммуноглобулинов и цитокинов. Данные изменения варьируют в зависимости от степени повреждения пародонта и отражают процессы местного воспаления и активации иммунных механизмов защиты. Ингибирование иммунных реакций сопровождается хронизацией патологического процесса и потерей зубов, ведущую роль в патогенезе играет дисбаланс местных иммунных реакций.
Иммунологические исследования пациентов с тяжелыми формами генерализованного пародонтита показали, что в общем изолированный патологический процесс сопровождался существенными изменениями Т- и В-звеньев иммунитета. При хроническом генерализованном пародонтите в тканях пародонта развивается поликлональная активация В-лимфоцитов, что привлекает в зону поражения нейтрофильные лейкоциты. Последнее, в условиях активации В-лимфоцитов приводит к неадекватному ответу на присутствие патогенных микроорганизмов.
Снижение функциональной активности авангардной линии антимикробной защиты, представленной нейтрофильными гранулоцитами и макрофагами, способствует пролонгированию течения и хроиизации процесса.
Хронические воспалительные заболевания пародонта развиваются на фоне подавленных механизмов фагоцитарной защиты, при этом характер местной иммунной реакции в зависимости от степени тяжести процесса существенно не различается. У одного и того же пациента выраженность воспалительного процесса в пародонте может колебаться от катарального гингивита до легкой или тяжелой форм пародонтита.
Современные открытия в области расшифровки механизмов естественного и адаптивного иммунитета на наноуровне позволили изучить роль образ-распознающих рецепторов эпителиальных клеток (pattern recognition receptors), идентифицирующих молекулярный образ микроорганизмов, запускающих активацию про- и противовоспалительных цитокиновых каскадов. Так, у больных с хроническим генерализованным пародонтитом в десневой жидкости наблю-. дается- увеличение содержания как про-, так и противовоспалительных медиаторов с наличием признаков ПтД-девиации (снижение уровня INF-y и повышение уровня IL-4). В пародонтальном комплексе у этих пациентов отмечалось выраженное увеличение концентраций Ig классов G, М и А, что, по-видимому, является следствием локальной поликлональной активации В-лимфоцитов. В десневой жидкости больных с хроническим генерализованным пародонтитом установлено повышение уровня цитокинов RANKL, TNF-a, TL-1 и снижение концентрации OPG, ч то может быть причиной активации остеокластов и последующей деструкции костной ткани. В зоне пародонта при этом развивается «нетипичное» для хронического процесса воспаление, характеризующееся повышенным уровнем IL-8 и преобладанием количества нейтрофилов над численностью других форм лейкоцитов.
Опосредованное образ-распознающими рецепторами преодоление эпителиального барьера микробами с формированием хронического очага инфекции возможно при внедрении как патогенной, так и условно-патогенной нормальной микрофлоры, если развивается утрата местной толерантности к ней. Известно, что интактный пародонт представляет собой достаточно эффективный барьер для бактерий. Инвазии пародонтопатоге-нов препятствует соединительнотканный эпителий и комплекс иммунных факторов защиты. В тех случаях, когда общая масса бактерий или вирулентность некоторых их видов достигает определенного критического уровня, происходит их внедрение в ткани пародонта. Возможно, этому способствует травма пародонта, а также сбои в иммунной системе.
В процессе инвазии бактерии могут вырабатывать соединения, ингибирующие или полностью блокирующие активность защитных сил. Инвазия бактерий приводит к гибели тканей и образованию микроабсцессов. Гистологически, в коронковой части пародонтального кармана внедрившиеся бактерии окружены мощными инфильтратами плазматических клеток, защищающими нижележащие ткани от инфекции. Уничтожение бактерий, внедрившихся в клетки и ткани пародонта, осуществляется посредством клеток фагоцитарной и лимфоцито-макрофаговой систем. Эти системы сами по себе обладают большим деструктивным потенциалом и могут стать причиной нарушения тканей пародонта вследствие дегрануляции и выработки цитокинов.
Иммунный ответ организма на присутствие пародонтопатогенов основан на взаимодействии нескольких систем: слизисто-секреторной, нейтрофильной, гуморальной, комплементарной и иммунорегуляторной. Предполагают, что основным механизмом слизисто-секреторной системы защиты является препятствие прикреплению на поверхности клеток адгезивных элементов пародонтопатогенов. Микроорганизмы с более активной адгезивной системой, например, трепонемы, прикрепляются к поверхностной мембране эпителиальных клеток. Другие микробы, отторгнутые защитной системой, прикрепляются к трепонеме и продолжают колонизацию.
Бактерицидные свойства слюны предотвращает развитие патогенной микрофлоры зубного налета, ведущего этиологического фактора заболеваний пародонта. Доказательством участия слизистосекреторной системы в защите от инвазии пародонтопатогенов являются фактические данные об увеличении содержания секреторного иммуноглобулина А (slgA) в слюне у больных пародонтитом. Однако эти данные противоречивы. Так, Орехова Л.Ю. с соавт. (2001) обнаружили снижение уровня секреторного иммуноглобулина в ротовой жидкости при пародонтитах.
Барер Г.М., Лемецкая Т.И. (1996) выявили повышенный уровень иммуноглобулинов основных классов вследствие их местного синтеза в воспаленной десне, а также транссудации из пораженных тканей с последующим поступлением десневой жидкости в смешанную слюну. В крови больных с данной‘Патологией снижается концентрация Ig А, М, G. По данным А.А. Кунина с соавт. (2001) при хроническом генерализованном пародонтите в стадии обострения содержание в ротовой жидкости Ig А, Е, G и лизоцима повышено, в то же время содержание slgA понижено, появляются следы Ig М. В десневой жидкости значительно увеличено количество макрофагов, нейтрофилов, лимфоцитов и эпителиоцитов. При этом в три раза снижена функциональная активность Т-лимфоцитов капиллярной крови десны.
Таким образом, хронический гингивит и пародонтит представляют собой многокомпонентные процессы, ключевыми из которых, с одной стороны, являются воспалительно-инфильтративные и деструктивные, а с другой стороны — компенсаторные. Ремиссия, которая наступает самостоятельно либо достигается проведением эффективного лечения, есть результат мобилизации и компенсаторной перестройки тканевых систем пародонта с их выведением на новый уровень гомеостаза. Наиболее мощным фактором, способствующим развитию и поддержанию болезней пародонта, является развитие дисбиоза в полости рта, который развивается или на фоне сниженного иммунитета, или сам приводит к его изменению.
Существует также механическая теория, которая позволяет по-новому взглянуть на патогенез воспалительного процесса в тканях пародонта. Весьма существенными явились результаты изучения изменений в системе иммунитета при длительной гиподинамии. Было обнаружено снижение способности лимфоцитов к активации и пролиферации, что повышает степень риска развития инфекционного процесса. Хорошо известно, что в полости рта лимфоциты относят к факторам местной защиты. Они мигрируют из лимфоидной ткани глоточного кольца и крови, через стенки микрососудов, обильно кровоснабжающих ткани десны. При длительной гипокинезии количество функционирующих микрососудов значительно уменьшается. Для тканей пародонта очень важно, что уменьшение кровоснабжения снижает уровень миграции клеток крови в десневую и ротовую жидкости. Это-касается также и сывороточных иммуноглобулинов, и компонентов комплементов, являющихся гуморальными факторами местной защиты тканей полости рта.
Можно представить, что снижение активности лимфоцитов влечет за собой уменьшение продуцирования секреторного иммуноглобулина IgA плазматическими клетками, образующимися из местных В-лимфоцитов в слизистой оболочке десны. Снижение же способности лимфоцитов к пролиферации, ведет к уменьшению связанных с ними иммуноглобулинов, что в свою очередь ослабляет защитные реакции в тканях пародонта. Становится понятным, что именно снижением активности лимфоцитов по причине регионарной гиподинамии и гипокинезии можно объяснить тот факт, что защитная реакция в пародонте начинается не с активации лимфоцитов антигенами микробов зубной бляшки, а с нейтрофильного хемотаксиса — увеличения числа нейтрофилов в зубодесневой борозде.
Для понимания механизмов развития деструктивных процессов в пародонте чрезвычайно важным явилось обнаружение при изучении иммунной системы в условиях гипокинезии достоверного увеличения продукции лимфоцитами остеокластактивирующего фактора, который вызывает потерю Са костной тканью. Совершенно очевидно также, что снижение интенсивности жевательной функции сопровождается снижением уровня саливации, что в свою очередь, ослабляет естественную резистентность тканей полости рта (в частности за счет таких факторов, как лизоцим, муцин и пр.). С уменьшением, саливации страдает и такой путь, снижения количества микроорганизмов в полости рта, как смыв их ротовой жидкостью.
Все вместе взятое благоприятствует микробной агрессии в полости рта и развитию воспаления в тканях пародонта, которые имеют наибольший контакт со скоплением микробов в зубной бляшке. Для развития воспаления в пародонте не менее важным является то, что гиподинамия способствует нарастанию устойчивости патогенных микробов к антибиотикам и возникновению аутоинфекции, а также сенсибилизации аллергенами аутомикрофлоры. Последнее, как установлено, вызывает потерю костной ткани в пародонте.
Благодаря изучению проблем гипокинезии и гиподинамии, стало очевидным, что малоподвижный образ жизни, который ведет человек в нашем столетии, отрицательно сказывается на состоянии его иммунной системы и сопротивляемости микробным инфекциям. Следует полагать, что это усугубляет последствия снижения факторов местной защиты полости рта, связанные с регионарной гиподинамией и гипокинезией (гипофункцией) в жевательной системе. Дополнением к этому являются многочисленные соматические заболевания, которые еще больше ослабляют иммунные силы организма и приводят в своем патогенезе к убыли костной ткани.
Таким образом, хронические очаги инфекции в полости рта вносят существенный вклад в развитие иммунологических дисбалансов, постоянно отвлекая на себя иммунологические ресурсы организма и истощая общий потенциал противоинфекционной защиты, что множит число вновь возникающих инфекционных очагов и хронизирует их. С другой стороны, полость рта у этих больных становится постоянно существующим источником распространения инфекции в нижележащие органы, а также лимфогенно и гематогенно по всему организму. Персистирующий антигенный инфекционный стимул неизбежно обусловливает аллергическую сенсибилизацию организма, что еще более грубо нарушает равновесие иммунной системы»больных, оказывая на нее угнетающее и дезорганизующее влияние.

Приглашаем подписаться на наш канал в Яндекс Дзен
В первую очередь, автореферат "Современные иммунологические аспекты в патогенезе заболеваний пародонта" будет интересен специалистам в области стоматологии, а также широкому кругу читателей, кто интересуется современными тенденциями в исследованиях и научными взглядами в лечении пародонтита.
Что особо хотелось отметить - это возраст исследуемых. Средний возраст - всего 38 (!) ле т. Заболевания пародонта "молодеют", причем процент наблюдаемых мужчин составил около 30 процентов, женщин - чуть менее 70 процентов. Пародонтит становится серьезнейшей проблемой, затрагивающей 99-100 процентов взрослого населения России.
Работа выполнена в Государственном бюджетном образовательном учреждении высшего профессионального образования «Московский медико-стоматологический университет имени А.И.Евдокимова» Министерства здравоохранения Российской Федерации (ГБОУ ВПО МГМСУ имени А.И.Евдокимова Минздрава России).
Научные консультанты:
- Янушевич Олег Олегович , Заслуженный врач РФ, Лауреат премии Правительства Российской Федерации в области науки и техники, доктор медицинских наук, профессор
- Гуревич Константин Георгиевич , доктор медицинских наук, профессор
Официальными оппонентами в диссертации выступили:
- Аванесов Анатолий Михайлович , доктор медицинских наук, профессор, заведующий кафедрой общей и клинической стоматологии медицинского института Федерального государственного автономного образовательного учреждения высшего образования «Российский университет дружбы народов».
- Иванова Елена Владимировна , доктор медицинских наук, доцент кафедры терапевтической стоматологии Государственного бюджетного образовательного учреждения дополнительного профессионального образования «Российская медицинская академия последипломного образования» Минздрава РФ.
- Панченко Леонид Фёдорович , доктор медицинских наук, профессор, заслуженный деятель науки РФ, академик РАН, заведующий лабораторией биохимии филиала ФГБУ «Федеральный медицинский исследовательский центр психиатрии и наркологии им. В.П. Сербского» Минздрава РФ.
С моей диссертацией в полном объеме можно ознакомиться в библиотеке ГБОУ ВПО МГМСУ имени А.И. Евдокимова МЗ РФ по адресу 127206, Москва, ул. Вучетича, д.10а
Актуальность проводимого исследования
Согласно последним исследованиям ВОЗ, более 90% населения старше 40 лет страдает заболеваниями пародонта: в Российской Федерации у взрослого населения распространенность заболеваний пародонта достигает 99- 100% . Лечение заболеваний пародонта до настоящего времени остается сложной и не до конца решенной медицинской проблемой. Функциональные расстройства зубочелюстной системы, обусловленные потерей зубов от заболеваний пародонта, развиваются в 5 раз чаще, чем при осложнениях кариеса (Грудянов А.И, 2009). Более того, воспалительные заболевания пародонта осложняются психологическими факторами, и проблема становится не только медицинской, но и социальной (Дмитриева Л.А, 2001).
Известно, что развитие заболеваний пародонта определяется сложным взаимодействием иммунной системы и патогенов, переоценка роли каждого из которых может привести к предвзятым выводам (Pollreisz A, Huang Y, Roth GA, et all, 2010).
Эти знания необходимы для развития иммуномодулирующих стратегий при лечении пародонтита , а также для максимальной защиты и минимизации разрушений тканей пародонта. В рамках расширенной парадигмы Th1/Th2/Th17, вероятно, можно будет объяснить, чем обуславливается защитная или деструктивная реакция в пародонте отдельных клеток, и тогда вероятно, появится возможность разработать адекватные терапевтические вмешательства, максимизирующие защитные и минимизирующие деструктивные функции T-клеток при заболеваниях пародонта.
Цель исследования
Изучение иммунологических аспектов хронического генерализованного пародонтита для разработки персонифицированного подхода к лечению и оценке прогноза течения заболевания.
Задачи исследования
- Выявить факторы риска развития хронического генерализованного пародонтита
- Провести индексную оценку состояния полости рта при пародонтите до и после лечения
- Выявить факторы, связанные с неэффективностью лечения пародонтита
- Исследовать показатели клеточного иммунитета при пародонтите.
- Изучить содержание цитокинов в десневой жидкости и плазме крови у пациентов с пародонтитом
- Определить уровень антител к P.gingivalis у здоровых лиц и больных пародонтитом
- Провести оценку состояния иммуно-интерфероновой системы при пародонтите
- Исследовать особенности дифференцировки лимфоцитов при заболеваниях пародонта
- Изучить влияние лечения на иммунологические показатели
Научная новизна полученных результатов исследования
- Показано , что развитие и неэффективность лечения хронического генерализованного пародонтита сопряжены с наличием модифицируемых и немодицицируемых факторов риска. Среди немодифицируемых основными являются: женский пол, возраст. Основными модифицируемыми факторами риска являются: нерациональное питание, гиподинамия, курение, ожирение.
- Показано , что при пародонтите изменяются показатели клеточного звена иммунитета.
- Выявлено , что содержание TNFα, IL-18, IL-17 и IFNγ в десневой жидкости и плазме крови больных пародонтитом выше, чем у контрольных лиц.
- Доказано , что содержание IL-4 и IL-10 в десневой жидкости и плазме крови при пародонтите ниже, чем у практически здоровых лиц. В десневой жидкости и плазе крови наблюдается дисбаланс цитокинов остеокластогенеза. У 5% клинически здоровых лиц определены значимые титры IgA и IgM к P.gingivalis. Данные антитела выявлены у 100% больных пародонтитом. У 1 / 10 больных отсутствует выработка IgG к P.gingivalis.
- Обнаружено , что эффективность иммунного ответа на P.gingivalis, определяемая по выработке антител, связана с социально-демографическими, поведенческими и клиническими факторами.
- Выявлено три типа изменений системы интерферона при пародонтите: а) резкое снижение продукции IFNα и IFNγ, повышение уровень сывороточного IFN, б) снижение уровней сывороточного IFN, существенное снижение продукции IFNα и IFNγ на фоне повышения спонтанного синтеза IFN, в) снижение продукции IFNα и IFNγ, повышением уровня сывороточного IFN.
- Доказано , что при пародонтите снижается экспрессия CD14 и повышается экспрессия CD16 и CD45RA на лимфоцитах периферической крови.
- При пародонтите выявлено два основных типа изменений со стороны лимфоцитов: а) снижение числа цитототоксических Т-лимфоцитов (CD3 + CD8 + ), увеличение CD3 - CD8 + клеток (73,2% пациентов), б) повышение числа В-лимфоцитов и NK-клеток, выраженное снижение уровня Т-лимфоцитов (15,4% пациентов). При увеличении числа NK- клеток у 100% пациентов наблюдаются признаки резорбции костной ткани, а последующее лечение в 2/3 случаев будет неэффективным.
Какие научные положения были вынесены на защиту моей докторской диссертации
- Развитие и неэффективность лечения хронического генерализованного пародонтита сопряжены с наличием модифицируемых и немодифицируемых факторов риска.
- При пародонтите изменяются показатели клеточного звена иммунитета.
- Пародонтит сопряжен с дисбалансом про- и противо-воспалительных цитокинов как в десневой жидкости, так и в крови.
- Эффективность иммунного ответа на P.gingivalis, определяемая по выработке антител, связана с социально-демографическими, поведенческими и клиническими факторами.
- При хроническом пародонтите наблюдается три типа изменений системы интерферона и два основных типа изменений со стороны лимфоцитов.
Теоретическая и практическая значимость полученных результатов
- Разработана методология персонифицированной оценки течения пародонтита.
- Показана высокая иммунологическая эффективность лечения хронического генерализованного пародонтита методом root planing, которая позволяет добиться клинического улучшения состояния больного в 81% случаев через 6 месяцев . Данный метод также имеет положительное влияние на изучаемые показатели иммунной системы.
- Выявлены факторы, приводящие к снижению эффективности лечения хронического генерализованного пародонтита. К немодифицируемым относятся возраст и женский пол. К модифицируемым относятся курение, питание, низкая двигательная активность. Воздействие на них может повысить эффективность лечения пародонтита.
- Наиболее информативным методом изучения иммунного статуса при пародонтите является исследование малых субпопуляций лимфоцитов.
- Интерфероновый статус и уровень антител к P.gingivalis обладают прогностической информативностью в отношении течения хронического генерализованного пародонтита.
- Результаты работы послужили основанием для информационно-методического письма главного внештатного специалиста стоматолога МЗ РФ от 04.03.2015 года, главного внештатного стоматолога здравоохранения Ростовской области от 16.02.2015 года.
Внедрение результатов исследования
Результаты исследования послужили основанием для написания информационно-методических писем главного внештатного специалиста стоматолога МЗ РФ и главного внештатного стоматолога здравоохранения Ростовской области. Результаты используются в работе Министерства здравоохранения Республика Мордовия, в клинике ГБОУ ВПО КДМК МГМСУ им. А.И. Евдокимова МЗ РФ, ГБОУ ВПО Ростовский государственный медицинский университет МЗ РФ, поликлиническом отделении ФГБУ «РНИИАиП» МЗ РФ, ГАУ Ростовской области «Стоматологическая поликлиника», «Стоматологической поликлинике №4» Ростовской области.
Апробация результатов исследования
Материалы диссертации были доложены и обсуждены на заседании:
- кафедры «Пародонтологии»,
- кафедры ЮНЕСКО «Здоровый образ жизни-залог успешного развития»,
- кафедры патофизиологии,
- кафедры клинической стоматологии №3 ГБОУ ВПО Московский государственный медико-стоматологический университет МЗ РФ.
- III международной студенческой Научно-практической конференции, РУДН, Москва (2011),
- 7 конгрессе European Federation of Periodontology (2012) Vienna, Austria,
- VIII Всероссийской конференции «Иммунологические чтения в Челябинске» (2013),
- 8 конгрессе European Federation of Periodontology (2015) London.
По теме моей диссертации " Современные иммунологические аспекты в патогенезе заболеваний пародонта опубликовано 26 работ , из них - 19 в журналах рекомендованных ВАК (Высшей Аттестационной Комиссией).
Я самостоятельно осуществляла подбор пациентов в исследование. Проводила клиническое, инструментальное и лабораторное обследование. Мной проведён анализ отечественной и зарубежной литературы, сформулированы цель, задачи, этапы и методы исследования, научные положения, выносимые на защиту, выводы и практические рекомендации. Я участвовала в иммунологических исследованиях, заполняла специально разработанные учетные формы и клинические карты. Также мной проведена статистическая обработка обобщенного материала, результаты статистической обработки вы сможете увидеть в этой статье.
У вас наблюдаются симптомы пародонтита? Все предыдущее лечение пародонтита оказалось неэффективным?
Записаться на прием к д.м.н. Теблоевой Лауре Михайловне!
В исследование было включено 340 пациентов с пародонтитом
Итак, в мое исследование включено 340 пациентов с хроническим генерализованным пародонтитом, обратившихся в момент обострения заболевания, которые составили основную группу.
Средний возраст обратившихся был 38+0,5 лет , из них 30,1% составили мужчины. То есть женщины в исследовании составили чуть меньше 70%. Все обратившиеся - жители Москвы и Московской области. Обследованные удовлетворяли перечисленным ниже критериям включения, невключения и исключения из исследования.
Критерии включения в исследование:
мужчины и женщины в возрасте от 21 до 50 лет; постоянное проживание в Москве или Подмосковье; верифицированный диагноз «пародонтит средней степени тяжести»; отсутствие предшествующего лечения пародонтита в течение не менее 6 месяцев; прикус ортогнатический, вторичная адентия – III класс дефектов зубных рядов по Кеннеди Е. (1974) – включенные дефекты в области моляров или премоляров с одной стороны – отсутствие не более 2 зубов; наличие несъемных ортопедических конструкций – одиночные искусственные коронки, мостовидные протезы – время изготовления менее 3-х лет, удовлетворяющие гигиеническим требованиям; способность свободно читать и заполнять анкеты; у женщин на основании опроса – отсутствие беременности и кормления грудью, климактерического синдрома; высказанное в письменном виде письменное добровольное согласие на участие в исследовании.
Критерии исключения из исследования:
пародонтит легкой или тяжелой степени тяжести; предшествующее лечение пародонтита в течение 6 месяцев и менее до первого визита; для женщин – беременность или послеродовый период, а также климактерический синдром (отсутствие менструаций со слов женщины более 1 месяца); другие воспалительные или дегенеративные заболевания полости рта; системные заболевания; патологические виды прикуса; частичная вторичная адентия – I, II, IV классы дефектов зубных рядов по Кеннеди Е. (1974); III класс по Кеннеди Е. – отсутствие более 2 зубов; наличие съемных ортопедических конструкций; наличие несъемных ортопедических конструкций, время изготовления которых более 3-х лет, не удовлетворяющих гигиеническим требованиям; трудности с чтением и заполнением анкет; отсутствие письменного добровольного согласия на участие в исследовании.
Критерии невключения в исследование:
лица, находящиеся под действием алкоголя или наркотиков; пациенты, не способные обслуживать себя самостоятельно; наличие острых воспалительных заболеваний вне полости рта; возраст менее 21 лет и более 50 лет;
Чтобы отобрать указанных пациентов, было осмотрено 668 пациентов , обратившихся по поводу пародонтита.
Социальный статус пациента оценивали на основании специальной анкеты. Индекс массы тела рассчитывали на основании сообщенных пациентом данных о росте и весе.
Комплексное обследование пациентов с пародонтитом включало клиническое, индексное и рентгенологическое исследования.
При постановке диагноза использована классификация, в основу которой положена клиническая форма заболевания, с определением характера тяжести течения. Данная классификация принята в 1983 г. на 16 Пленуме Всесоюзного общества стоматологов в г. Ереван. Для индексной оценки состояния тканей пародонта использовали метод Силнеса и Лоэ, индекс РМА, индекс CPITN, метод Muhleman в модификации Cower, индекс гигиены Грина Вермильона, измерение глубины пародонтальных карманов с помощью зондов Уильямса.
Антитела к P.gingivalis определяли в плазме крови. Использовался иммуно-ферментный анализ (ИФА) для определения IgG, IgM, IgE. Все реактивы были производства фирмы Sigma (США). В работе использован "сэндвич"-вариант твердофазного ИФА. Исследования выполнены ФГБУ «ФНИЦ эпидемиологии и микробиологии имени Н.Ф. Гамалеи» МЗ РФ.
Показатели интерферонового-статуса определяли микрометодом в цельной крови по методике Григорян С.С и др. (1988). Исследования выполнены в лаборатории интерферонов и интерфероногенеза в ФГБУ «ФНИЦ эпидемиологии и микробиологии имени Н.Ф. Гамалеи» МЗ РФ.
Исследование субпопуляционного состава лимфоцитов периферической крови проводили с применением проточного цитофлюориметра на базе лаборатории клеточной иммунологии ФГБУ «ФНКЦ ДГОИ им. Дмитрия Рогачёва МЗ РФ. В работе использована двух-платформенная технология: при подсчете абсолютного количества клеток задействованы 2 прибора – проточный цитофлюориметр и гематологический анализатор.
Анализ содержания цитокинов IFN-γ, IFN-α, IL-4, IL-10 и TNF-α проводили с помощью твердофазного иммуноферментного анализа. Исследования выполнены в лаборатории интерферонов и в ФГБУ «ФНИЦ эпидемиологии и микробиологии имени Н.Ф. Гамалеи» МЗ РФ.
Законы распределения параметров устанавливали с помощью λ-критерия Колмогорова-Смирнова. При непротиворечии гипотезе о нормальном распределении сравнение дисперсий проводили при помощи F-критерия Фишера. При равенстве дисперсий для сравнения средних применяли t-критерий Стьюдента, иначе – критерий Уэлча. При противоречии гипотезе о нормальном распределении средние величины сравнивали с использованием U-статистики Вилкоксона-Мана-Уитни и X критерий Ван-дер Вардена. Для изучения механизмов взаимосвязи параметров применен корреляционный анализ. Вычисляли коэффициент ранговой корреляции Кэндалла, что позволило не учитывать закон распределения изучаемых параметров. Полученные коэффициенты корреляции сравнивали с нулем для определения их значимости и между собой для определения различий (Лакин Г.Ф., 1990; Харламов и соавт., 1994). Частоты встречаемости признаков оценивали методом «случай-контроль» с расчетом отношения шансов (OR, odds ratio). 95% доверительные интервалы рассчитывали методом Фишера (OR-Cl95%) (Гржибовский А.М., 2008).
Результаты собственных исследований
До начала лечения пациенты предъявляли жалобы на кровоточивость дёсен при чистке зубов, подвижность зубов, запах изо рта. В анамнезе у пациентов выявлены следующие поведенческие факторы риска: курение, нерациональное питание, гиподинамия, ожирение, аборты. У 35% мужчин и 12% женщин установлено предшествующее неэффективное лечение пародонтита, причем среди женщин это число достоверно ниже (таблица 1).
Типичная анамнестическая картина у пациентов до начала лечения пародонтита в зависимости от пола
8.3. ПАТОГЕНЕЗ ПЕРИОДОНТИТА
Чаще всего воспалительный процесс в периодонте обусловлен поступлением инфекционно-токсического содержимого корневых каналов через верхушечное отверстие. Причем вирулентности микрофлоры в настоящее время придают меньшее значение, чем влиянию на околоверхушечные ткани эндотоксина, образующегося при повреждении оболочки грамотрицательных бактерий. Попадание эндотоксина в периодонт ведет к образованию биологически активных продуктов, усиливающих проницаемость сосудов. Развивается острый периодонтит. В период острого воспаления в периодонте накапливаются антигены, которые медленно элиминируют из этой зоны вследствие того, что периодонт ограничен кортикальной пластинкой альвеолы. Эндотоксины оказывают сильное антигенное воздействие на иммунологическую систему периодонта и окружающих его тканей.
Интенсивность острого периодонтита и степень вовлечения в воспаление окружающих зуб тканей зависит как от вирулентности инфекции, так и от иммунологического статуса организма. Когда иммунологические защитные механизмы ослаблены, затрудняется отграничение местного патологического процесса и развивается острое диффузное воспаление, распространяющееся на тело челюсти с формированием в тканях абсцессов и флегмон, с типичными явлениями интоксикации организма.
Если иммунологические защитные механизмы способны локализовать воспаление у верхушки зуба путем формирования защитного барьера, то процесс не распространяется и приостанавливается на ранней стадии своего развития, признаков острой интоксикации организма не возникает. Развивается хронический воспалительный процесс, так как сохраняется источник инфекции.
Реакция тканей периодонта на непрерывное раздражение антигенами, поступающими из корневого канала, проявляется в виде антителозависимых и клеточно-обусловленных процессов. К антителозависимым относятся иммунокомплексные и IgE-обусловленные реакции. К клеточно-обусловленным относятся реакции гиперчувствительности замедленного типа.
Для развития иммунокомплексной реакции при хроническом верхушечном периодонтите, как утверждает А. И. Воложин, необходимы три условия: наличие плохо фагоцитируемых иммунных комплексов, системы комплемента и большого количества полиморфно-ядерных лейкоцитов. Все эти условия имеют место в тканях при хроническом воспалении в периодонте.
Сходство с иммунокомплексными имеет IgE-обусловленная реакция. При хроническом периодонтите в периапикальных тканях обнаружены IgE-продуцирующие и тучные клетки. IgE идентифицирован как основной фактор, вызывающий атопическую реакцию, он обладает способностью в течение длительного времени фиксироваться на рецепторах базофилов и тучных клеток. Антиген связывается на поверхности тучной клетки двумя молекулами IgE, вследствие чего из клетки высвобождаются гистамин, серотонин и другие медиаторы воспаления. Благодаря этим медиаторам повышается проницаемость сосудов и при их расширении в ткани периодонта поступает большое количество лейкоцитов, которые являются источником ферментов, разрушающих нежизнеспособные ткани.
Реакции гиперчувствительности замедленного типа отличаются от иммунокомплексных тем, что при них нет необходимости в антителах, так как со специфическим антигеном реагирует сенсибилизированный Т-лимфоцит-эффектор. Реакция гиперчувствительности замедленного типа возникает вследствие взаимодействия уже сенсибилизированных лимфоцитов и главным образом клеточных антигенов, что стимулирует размножение лимфоцитов и выделение из них лимфокинов. Некоторые лимфокины вызывают разрушение клеток периодонта (например, лимфотоксин). К лимфокинам также относится фактор, активирующий остеокласты, которые осуществляют резорбцию кости. В зоне воспаления макрофаги и нейтрофилы выделяют фермент коллагеназу, которая способствует растворению коллагеновых волокон и вызывает деструкцию костной ткани.
8. Осложнения периодонтита. Радикулярные кисты челюсти
8. Осложнения периодонтита. Радикулярные кисты челюсти Выделяют следующие осложнения: местные и общие. К общим осложнениям относят явления интоксикации как следствие всасывания продуктов жизнедеятельности микроорганизмов из очага воспаления. Диссеминация бактерий в
2. Патогенез
2. Патогенез Установлены следующие варианты течения сифилитической инфекции: классический (стадийный) и бессимптомный.Сифилису присуще стадийное, волнообразное течение с чередованием периодов манифестации и скрытого состояния. Другая особенность течения сифилиса –
8.2. ЭТИОЛОГИЯ ПЕРИОДОНТИТА
8.2. ЭТИОЛОГИЯ ПЕРИОДОНТИТА По происхождению различают периодонтит инфекционный, травматический и медикаментозный. Учитывая, что от патогенетической терапии ожидают максимального эффекта, современные классификации периодонтита должны отражать сущность
8.4. КЛАССИФИКАЦИЯ ПЕРИОДОНТИТА
8.4. КЛАССИФИКАЦИЯ ПЕРИОДОНТИТА По клиническому течению выделяют острый и хронический периодонтит.Острый периодонтит (periodontitis acuta) в зависимости от характера экссудата многие авторы разделяют на острый, серозный и острый гнойный. Следует сказать, что подобное
8.5. КЛИНИЧЕСКАЯ ХАРАКТЕРИСТИКА ПЕРИОДОНТИТА
8.5. КЛИНИЧЕСКАЯ ХАРАКТЕРИСТИКА ПЕРИОДОНТИТА 8.5.1. Острый верхушечный периодонтит Эта форма характеризуется бурно протекающим и прогрессирующим воспалением с нарастающей сменой одних симптомов другими. Для острого периодонтита характерно наличие резкой локализованной
8.6.1. Лечение острого верхушечного периодонтита
8.6.1. Лечение острого верхушечного периодонтита Острый медикаментозный (токсический) периодонтит в стадии интоксикации. Эта форма периодонтита, как правило, возникает в результате длительного пребывания в полости зуба мышьяковистой пасты или ее передозировки при
8.6.2. Лечение хронического верхушечного периодонтита
8.6.2. Лечение хронического верхушечного периодонтита В настоящее время подавляющее большинство клиницистов относят хронический периодонтит к инфекционным очагам. Поэтому выбор метода лечения при хроническом периодонтите будет зависеть от степени выраженности местных
8.7. ОСЛОЖНЕНИЯ ПРИ ЛЕЧЕНИИ ПЕРИОДОНТИТА
8.7. ОСЛОЖНЕНИЯ ПРИ ЛЕЧЕНИИ ПЕРИОДОНТИТА Осложнения могут наблюдаться как в процессе лечения периодонтита, так и после пломбирования корневого канала. Обработка корневого канала сильнодействующими препаратами (высокая концентрация формалина, фенола, резорцин-формалина
Патогенез
Патогенез ДН возникает в связи с нарушением альвеолярной вентиляции, легочного кровотока и альвеолокапиллярной диффузии газов.Физиологические механизмы нарушения вентиляцииАдекватность вентиляции зависит от следующих взаимосвязанных факторов:1. активности
4.4. Патогенез
4.4. Патогенез По нашему глубокому убеждению, патогенез всегда определяет клиническую картину того или иного заболевания. Может быть, гипертермия является одним из наиболее показательных примеров этого тезиса. Достаточно взглянуть на рисунок 30, приведенный нами из
Патогенез
Патогенез Под действием холода прежде всего повышается тонус гладких мышц стенок кровеносных сосудов, что приводит к снижению кровотока вначале в капиллярах, затем в венулах и артериолах. Дальнейшее снижение температуры вызывает сгущение крови в сосудах охлажденной
Патогенез
Патогенез Патогенез СДС сложен. Как известно, основные клинические проявления синдрома возникаюоГ после освобождения, когда наступает восстановление кровообращения сдавленной части тела.В патогенезе СДС наибольшее значение имеют три фактора:1. болевое раздражение,
Патогенез.
Патогенез. Изначально существовала масса теорий возникновения токсикоза: рефлекторная, неврогенная, гормональная, аллергическая, иммунная, кортико-висцеральная. На настоящий момент ведущей теорией можно назвать нарушение функционального состояния центральной
Патогенез
Патогенез Непосредственной причиной, лежащей в основе данного вида патологии родовой деятельности, является нарушение функционального равновесия вегетативной нервной системы. Также нередко отмечаются снижение функции симпатико-адреналовой и преобладание тонуса
Патогенез
Патогенез Редко встречается ситуация травматизации задней стенки влагалища, мышц тазового дна и кожи промежности, тогда как задняя спайка и сфинктер заднего прохода остаются целыми. В этом случае роды происходят через искусственно образованный канал.Разрывы
Содержание
- Периодонтит
- Причина возникновения (этиология) периодонтита
- Развитие (патогенез) периодонтита
- Классификация периодонтита
- Клинические симптомы периодонтита
- Диагностика периодонтита
- Лечение периодонтита
Периодонтит
Периодонт — это часть тканевого комплекса пародонта, возглавляющего морфофункциональное единство тканей, окружающих зуб, — представлен высокодифференцированной соединительной тканью, которая расположена в замкнутом пространстве между компактной пластинкой альвеолы и цементом корня зуба.
Периодонтит — это воспаление тканей периодонта.
Причина возникновения (этиология) периодонтита
По своему происхождению верхушечный периодонтит делится на:
- инфекционный периодонтит
- травматический периодонтит
- медикаментозный периодонтит
Инфекционный верхушечный периодонтит чаще возникает при попадании в периодонт микроорганизмов (золотистый и белый стафилококк, негемолитический стрептококк и гемолитический стрептококк, фузобактерии, спирохеты, грибы), их токсинов, продуктов распада пульпы и дентина в периодонт из корневого канала или пародонтального кармана.
По способу проникновения бактерий инфекционный периодонтит делят на интрадентальный и экстрадентальный, внутризубной и внезубной. К последнему может быть отнесён инфекционный периодонтит, развивающийся в результате перехода воспалительного процесса из окружающих тканей при остеомиелите, остите, периостите, гайморите, рините, пародонтите. Возможны также гематогенный и лимфогенный пути заболевания периодонта при туберкулёзе, гепатите, тифе, гриппе. Интрадентальный путь проникновения микроорганизмов в периодонт связан с их поступлением из кариозной полости или корневого канала самостоятельно или насильственно при выполнении эндодонтических манипуляций.
Травматический верхушечный периодонтит возникает при травмировании околоверхушечных тканей эндоканальными инструментами или в процессе проталкивания за верхушечное отверстие корневой пломбы, штифта. К травматическим причинам верхушечного периодонтита относятся также удар по зубу, ушиб, падение, толчок, случайное накусывание на твёрдые предметы. Острая травма нередко вызывает сравнительно быстро проходящее раздражение периодонта и его восстановление. Но иногда эти повреждения сопровождаются кровоизлиянием, нарушением кровообращения в пульпе с последующим её некрозом. Такое состояние не проявляется длительное время и сопровождается только изменением цвета зуба и отсутствием чувствительности к различным раздражителям. Высокая пломба и искусственная коронка, завышающие прикус, часто являются причиной развития травматического периодонтита в связи с хронической микротравмой периодонта.
Медикаментозный верхушечный периодонтит может возникнуть вследствие попадания в периодонт сильнодействующих химических и лекарственных веществ: мышьяковистой кислоты, фенола, формалина. Причиной верхушечного периодонтита может стать выведение за апекс фосфат-цемента, резорцин-формалиновой и цинк-эвгенольной пасты, штифт и другие пломбировочные материалы. Сюда же относятся периодонтиты, развившиеся в результате местной иммунологической реакции в ответ на попадание за верхушку корня антибиотиков, эвгенола, хлорамина, хлоргексидина, димексида, йода.
Развитие (патогенез) периодонтита
Развитие воспаления периодонта связано с поступлением в периодонтальную щель инфекционно-токсического содержимого корневого канала, необходимо наличие раздражающего агента-кокка, продуктов его жизнедеятельности, лекарственных препаратов. В прохождении воспалительного процесса в периодонте не последнюю роль играет эндотоксины, которые образуются при повреждении оболочки грамположительных бактерий, вегетирующих в корневых каналах зубов, лишённых пульпы, в частности, бактериальный эндотоксин, оказывающий токсическое и пирогенное действие.
При периодонтите наблюдается множественное повреждение клеток соединительной ткани и массивный выброс лизосомальных ферментов. Эндотоксин, попавший в заверхушечные ткани, приводит к дегрануляции тучных клеток, которые являются источником гепарина и гистамина.
Биологически активные компоненты вызывают резкое повышение сосудистой проницаемости, нарастают отёк и инфильтрация. Нарушается микроциркуляция, наблюдается тромбоз, гиперфибринолиз и вторичная гипоксия, что приводит к деполимеризации основного вещества. Нарастает гипоксия, нарушается трофика, ярко проявляются признаки воспаления: местное повышение температуры, боль, отёк, гиперемия, нарушение функции. Ткань становится проницаемой за счёт образования пустот в основном веществе, выполняется её главная функция — защитная. Резко нарушается трофическая функция: клетка не в состоянии получить кислород и БАК из основного вещества и, наоборот, отдавать в него отработанные продукты. Отмечается зашлаковывание как клеток, так и межклеточного вещества, последнее связано с дисфункцией сосудистой стенки.
Бактериальные эндотоксины активируют компоненты комплемента, образуются биологически активные вещества, усиливающие проницаемость сосудов, и следствием этого является накопление мононуклеарных лимфоцитов и макрофагов. Эти клетки выделяют ферменты, повышающие активность остеокластов, которые обуславливают деструкцию костной ткани.
Классификация периодонтита
В практике терапевтической стоматологии за основу принята классификация периодонтита, позволяющая характеризовать степень повреждения периодонтальных тканей.
Классификация верхушечного периодонтита:
- Острый верхушечный периодонтит:
- фаза интоксикации;
- фаза экссудации: серозная, гнойная.
- Хронический верхушечный периодонтит:
- хронический верхушечный фиброзный периодонтит;
- хронический верхушечный гранулирующий периодонтит;
- хронический верхушечный гранулематозный периодонтит.
- Хронический верхушечный периодонтит в стадии обострения:
- хронический верхушечный фиброзный периодонтит в стадии обострения;
- хронический верхушечный гранулирующий периодонтит в стадии обострения;
- хронический верхушечный гранулематозный периодонтит в стадии обострени.
Клинические симптомы периодонтита
Диагностика периодонтита
Острый верхушечный периодонтит
Основным симптомом острого верхушечного периодонтита является постоянная локализованная боль. Характер боли, её выраженность, как и другие признаки течения острого верхушечного периодонтита, имеют местные и общие проявления, зависят от накопления в области верхушки корня экссудата серозного или гнойного.
Клинические проявления острого верхушечного периодонтита обусловлены фазой течения острого воспаления периодонта. Выделяют две основные фазы:
- Фаза интоксикации — для этой стадии характерны жалобы больного на постоянную локализованную боль различной интенсивности, усиливающиеся при накусывании и прикосновении к зубу. Больной всегда точно определяет поражённый зуб.
Объективно: лицо симметрично, открывание рта свободное. Слизистая оболочка в проекции поражённого зуба бледно-розового цвета. Коронка зуба не изменена в цвете, имеется кариозная полость или постоянная пломба. Перкуссия слабо болезненна, проявляются признаки повышенной чувствительности периодонта. - Фаза экссудации — в этой стадии выраженность симптомов воспаления зависит от характера экссудата. Жалобы больного на непрерывную боль, которая может держаться на одном уровне или усиливаться. Больной точно указывает на поражённый зуб, чувство «выросшего» зуба, болезненность при накусывании или даже лёгком прикосновении к зубу.
Объективно: перкуссия болезненна в вертикальном направлении, а затем в горизонтальном. Зуб подвижен, в цвете не изменён. Часто коронка интактна, а при наличии кариозной полости зондирование стенок и дна кариозной полости безболезненно. Полость зуба обычно не вскрыта, а при вскрытии её (в полости зуба и корневых каналах) наблюдается некротический распад пульпы. Слизистая оболочка в проекции больного зуба гиперемированна и отёчна, пальпация болезненна.
Фаза экссудации характеризуется всеми пятью признаками воспаления: местное повышение температуры, боль, отёк, гиперемия, нарушение функции. Прогрессирование острого воспалительного процесса в стадии экссудации может привести к значительному коллатеральному отёку околочелюстных тканей. Регионарные лимфатические узлы без изменений или несколько увеличены на стороне больного зуба, при пальпации безболезненны, подвижны. Температура тела нормальная. Общее состояние не нарушено.
Серозная фаза острого периодонтита может перейти в гнойную, которая длиться около 20 дней. Клиническая картина становится ярче, боль усиливается, становится пульсирующей, приобретает чаще всего непрерывный характер, иррадиирует по ходу ветвей тройничного нерва. Особенно боль усиливается при прикосновению к зубу, и поэтому больной держит рот полуоткрытым.
Состояние поражённого зуба аналогично состоянию при серозном остром верхушечном периодонтите. Цвет зуба не изменён, коронка зуба может быть интактна или разрушена, с наличием глубокой кариозной полости, наполненной некротическим дентином. Полость зуба чаще не вскрыта, зондирование стенок, дна кариозной полости безболезненно. Поражённый зуб патологически подвижен, перкуссия резко болезненно. Слизистая оболочка переходной складки, нёба, иногда альвеолярного отростка язычной поверхности в области поражённого и смежных зубов отёчна, гиперемированна. Лимфатические узлы подчелюстные, подбородочные, реже щёчные увеличены, болезнены при пальпации, подвижны.
Все эти явления нарастают по мере накопления экссудата в периодонтальной щели. Мучительная боль может продолжаться в течение нескольких дней. Как только гнойный экссудат находит выход, чаще через надкостницу, болевой синдром ослабевает, больные могут отмечать боль в челюсти, ухудшение общего состояния, развивается осложнение острого гнойного верхушечного периодонтита — периостит, а в более запущенных случаях — флегмоны околочелюстной области, острый одонтогенный остеомиелит.
Лечение периодонтита
Объектом вмешательства при лечении верхушечного периодонтита являются корневой канал с его многочисленными разветвлениями, дентинные канальцы с обильной микрофлорой, а также ткань периодонта, находящаяся в состоянии острого или хронического воспаления.
Лечение острого верхушечного периодонтита
- лечение в стадии интоксикации (производится в одно посещение):
- обезболивание (современные высокоэффективные анестетики — 4% ультракаин, 4% альфакаин, 4% раствор септонеста, 2% раствор лидокаина).
Для усиления обезболивающего эффекта и продления действия анестетика можно добавить 0,1% раствор адреналина гидрохлорида (1 капля на 10-15 мл анестетика).
Но надо помнить, что вазоконстрикторы противопоказаны пациентам с заболеваниями сердечно-сосудистой системы, сахарным диабетом в стадии декомпенсации, а также лицам преклонного возраста. - удаление повязки или старой пломбы, препарирование кариозной полости;
- раскрытие полости зуба (создание широкого и удобного доступа инструмента к полостям зуба и устью корневого канала);
- расширение устья корневого канала;
- эвакуация распада пульпы из корневого канала (работу всеми эндодонтическими инструментами следует проводить поэтапно, пристеночно и вполоборота).
- медикаментозная обработка корневого канала (соответствующими антидотами, нераздражающими антисептиками, подогретыми до 40°, 0,1% раствор перманганата калия, 3% раствор гипохлорида натрия, 0,02% раствор фурацилина, 0,1 % раствор димексида, 0,06% раствор хлоргексидина биглюконата.
После медикаментозной обработки корневой канал обезжиривают и высушивают сухими стерильными турундами на корневой игле или бумажными пинами соответствующего размера. - пломбирование корневого канала (завершение процедуры — рентгенологический контроль);
- наложение постоянной пломбы.
- обезболивание (современные высокоэффективные анестетики — 4% ультракаин, 4% альфакаин, 4% раствор септонеста, 2% раствор лидокаина).
- лечение в фазе экссудации (проводится в два посещения)
В первое посещение проводят с обезболиванием препарирование кариозной полости или трепанацию коронки зуба турбинным наконечником, раскрытие полости зуба, расширение устья корневого канала, удаление распада пульпы из корневого канала и раскрытие верхушечного отверстия. Критерием контроля раскрытия верхушечного отверстия служит появление экссудата в просвете корневого канала. С первого посещения зуб оставляем открытым, больного предупредить о том, что необходимо перед едой в зуб ввести маленький ватный тампон, а после приёма пищи ватный тампон удалить из кариозной полости и полость рта прополоскать водой. Если верхушечный периодонтит осложняется периоститом, отмечается гиперемия и отёк слизистой оболочки, болезненная пальпация и сглаженность переходной складки в области больного зуба, повышение температуры тела, изменение формулы крови, то назначают курс антибиотиков широкого спектра действия, десенсибилизирующие препараты. В это же время выполняют разрез по переходной складке, с рассечением надкостницы, рану дренируют.
Во второе посещение осуществляют сбор анамнеза (болел ли зуб, возникала ли боль при пережёвывании пищи), после чего оценивают объективный статус: состояние слизистой оболочки, окружающим больной зуб, лимфатических узлов, данные перкуссии, наличие или отсутствие экссудата в корневом канале.
При отсутствии жалоб и удовлетворительном общем и местном состоянии больного приступают к инструментальной обработке корневого канала. Далее – медикаментозная обработка корневого канала: применяют растворы протеолитических ферментов, антисептики.
Затем обезжиривают, высушивают, пломбируют, делают контрольное рентгенографическое исследование пломбированного корневого канала, ставится постоянная пломба.
Лечение хронических форм верхушечного периодонтита.
Цель лечения хронического верхушечного периодонтита — исключить корневой канал как источник воспаления периодонта и активно воздействовать на деструктивные процессы в околоверхушечных тканях.
Лечение любых форм хронического верхушечного периодонтита показано в одно посещение:
- препарирование кариозной полости с соблюдением всех правил и этапов;
- раскрытие полости зуба;
- расширение устья корневого канала и создание хорошего доступа к нему;
- удаление путридных масс и некротического дентина под антисептической ванночкой с использованием всего ассортимента эндодонтического инструментария.
- Обезжиривание и обезвоживание стенок корневого канала: с этой целью современная стоматология рекомендует использовать препараты: Netispad, Styptic, Largal ultra, Canal plus.
- Пломбирование корневого канала до физиологического апекса с последующей рентгенографией, констатирующее качество обтурации корневого канала. Показано пломбирование корневого канала твердеющими пастами и гуттаперчей. Первую порцию пломбировочного материала вносят в корневой канал на кончике иглы Миллера и подводят под давлением к верхушке корня зуба с помощью ватной турунды, что позволяет качественно обтурировать апекс; вторую порцию — на каналонаполнителе.
- Наложение постоянной пломбы.
Пациенты с деструктивными формами верхушечного периодонтита ставятся на диспансерный учёт. Повторное клинико-рентгенологическое исследование проводят спустя 3, 6, 12 месяцев. Если при обследовании через 12 месяцев больной не предъявляет жалоб, а на рентгенограмме в области верхушки корня не обнаруживается патологические изменения, то дальнейшее наблюдение не требуется, пациент снимается с диспансерного учёта. Если же через 12 месяцев, даже при отсутствии жалоб больного, рентгенологически определяется деструкция околоверхушечных тканей, требуется повторное лечение — удаление корневой пломбы, медикаментозная обработка и механическая обработка корневых каналов с последующим их пломбированием.
Читайте также:

