Очаг деструкции костной ткани зуба
Опубликовано: 26.04.2024
Случается, что, потеряв зуб, человек задумывается о протезировании только спустя несколько лет. Выбирает надежную современную технологию — дентальную имплантацию. И обнаруживает, что за прошедшее время костная ткань «расслабилась» — ее объем и плотность стали недостаточны для полноценной установки имплантата. О том, почему возникает разрежение костной ткани челюсти и возможна ли имплантация без наращивания костной ткани — читайте в нашем обзоре.
Что такое атрофия костной ткани челюсти
Костная ткань — сложная, живая, постоянно изменяющаяся структура. Как и в любой живой ткани, в ней есть вода — около 10% [1] . В среднем 25% состава кости — органическая, «живая» составляющая. Это белки, в основном коллаген, и клетки, регулирующие состав и структуру ткани. Оставшаяся доля — неорганические вещества (в основном гидроксиапатиты). Это именно те вещества, которые придают костной ткани прочность и жесткость. Процентное соотношение может меняться в зависимости от того, идет ли речь о губчатой или компактной костной ткани:
- Губчатая кость — пористая и легкая, в ней между костными структурами (трабекулами) много свободного пространства, где проходят кровеносные сосуды. В структуре преобладают органические компоненты.
- Компактная (кортикальная) кость — плотно скомпонованная и очень прочная. В ней преобладают неорганические субстанции.
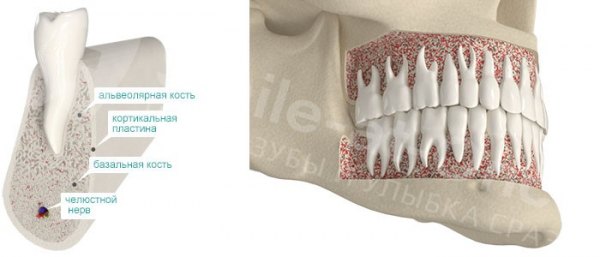
Живая ткань кости формируется костными клетками: остеоцитами и остеокластами.
Остеоциты — это клетки костной ткани, которые ее формируют и регулируют процесс кальцификации. Они синтезируют белковые структуры кости, регулируют минерализацию — концентрацию солей кальция и фосфора, таким образом поддерживая баланс между органической и неорганической составляющей.
Остеокласты уничтожают «отслужившие свое» или поврежденные костные структуры.
В нормальном состоянии живого организма непрерывно поддерживается баланс между разрушением и созиданием — для того чтобы создать что-то новое нужно «расчистить площадку». Но когда по каким-то причинам процесс резорбции (рассасывания) костной ткани начинает преобладать, наступает атрофия костной ткани.
Чаще всего убыль костной ткани развивается после удаления зуба. Любой орган для того, чтобы сохранить нормальное состояние, должен работать, а нерабочие структуры атрофируются — у организма нет возможности тратить питательные вещества и энергию на подержание в работоспособном состоянии нефункционирующего органа. Костная ткань челюсти поддерживается в «рабочем» состоянии нагрузкой, которая передается при жевании через корни зубов. Как только зуб удаляется, нагрузка исчезает. Постепенно перестают функционировать сосуды, которые питали удаленный зуб, а значит, перестает поступать питание и в ткань челюсти. Ткань челюсти в области удаленного зуба начинает рассасываться — атрофироваться. Как показало исследование немецких ученых, после потери зубов такие изменения возникают в 95% случаев [2] . В течение 1 года после потери зуба объем костной ткани уменьшается на 25% [3] . Именно поэтому врачи-стоматологи рекомендуют как можно быстрее после потери зуба поставить на его место имплантат.
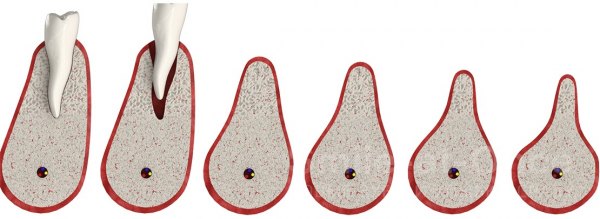
В клинической практике выделяют 4 степени атрофии [4] :
- незначительная;
- умеренная;
- выраженная;
- грубая.
При незначительном снижении плотности костной ткани возможна имплантация зубов с помощью дентальных имплантатов оптимального размера. При грубой атрофии имплантация возможна только после реконструкции челюсти.
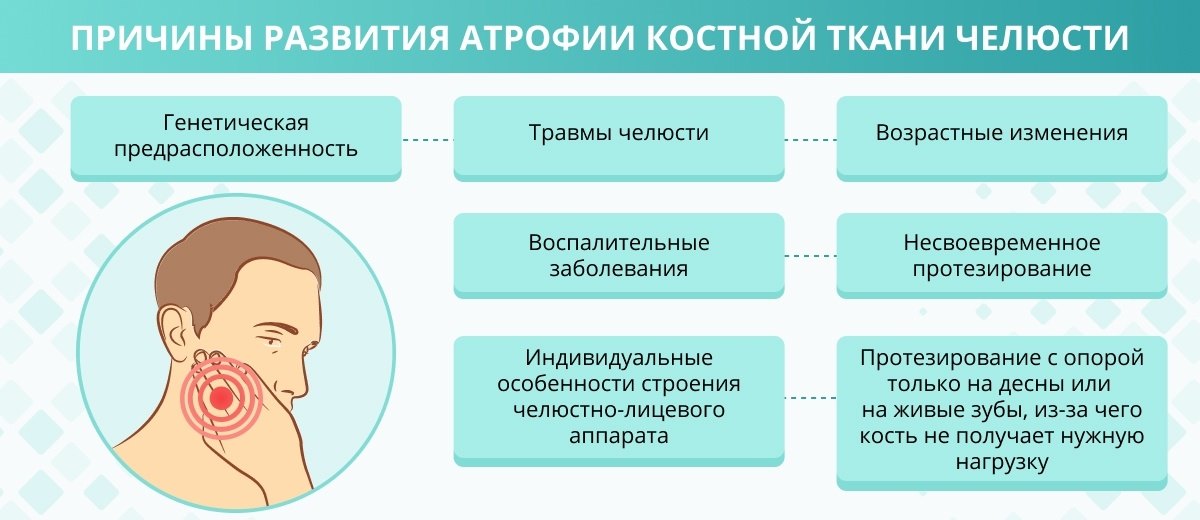
Причины потери плотности и убыли костной ткани челюсти
Потеря зуба — не единственная причина изменения костной структуры. Такими причинами могут стать:
- воспаление десен и периодонта — структур, окружающих зубы и обеспечивающих их стабильность;
- кисты и воспаления в области корней зубов или верхнечелюстных пазух;
- травмы челюсти;
- остеопороз;
- врожденные анатомические особенности.
Тем не менее основные причины развития атрофии костной ткани челюсти — несвоевременное протезирование после удаления зуба.
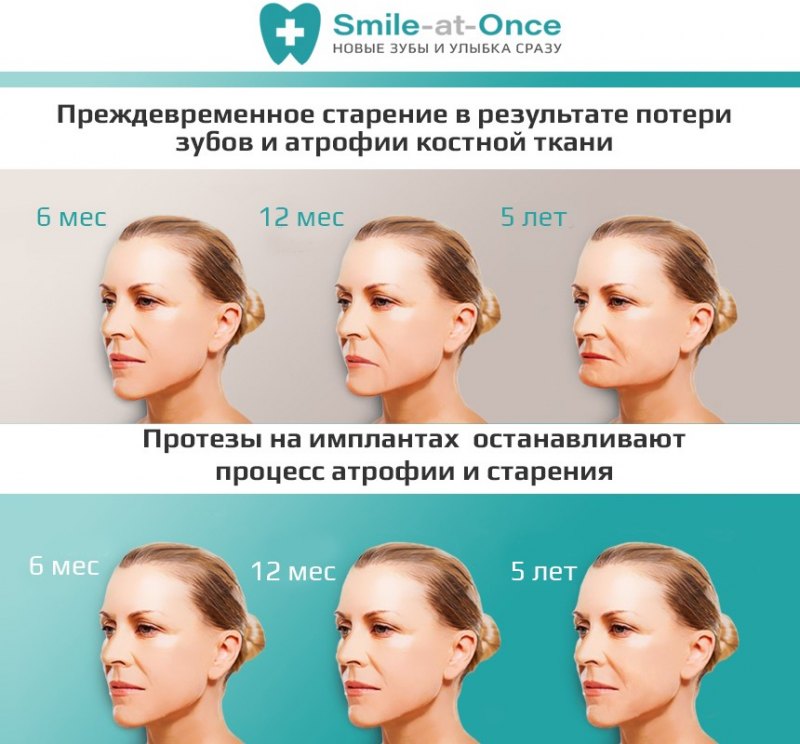
Последствия «расслабления» костной ткани
Атрофия альвеолярных отростков — проблема не только «местного» масштаба. Постепенно усиливаясь, процесс вызывает необратимые изменения:
- Меняется выражение лица. В зависимости от того, где расположен дефект, «укорачивается» верхняя или нижняя челюсть, западают губы, вокруг них формируются морщины. Лицо приобретает характерный «старческий» вид.
- Зубы начинают смещаться в сторону «пустого» пространства. Увеличивается вероятность потери и соседних зубов. Из-за того, что расположение зубов меняется, между ними задерживаются остатки пищи: ускоряется развитие кариеса. Да и само жевание становится менее эффективным, как результат — проблемы с ЖКТ.
И основная проблема, с которой сталкиваются пациенты стоматологических клиник, — невозможность имплантации зубов. По данным отечественных врачей, у 35% пациентов она невозможна без проведения реконструкции костной ткани челюсти [5] .
Как предотвратить процесс атрофии?
Поскольку атрофия костной ткани чаще всего развивается из-за удаления зуба (или нескольких зубов), очевидно, что для ее предотвращения следует как можно скорее восстановить зубы. Традиционно используются несколько методик:
- установка мостовидной конструкции;
- установка съемного протеза;
- имплантация.
Первые два метода относительно недороги. Но, к сожалению, они не восстанавливают нагрузку на кость в месте удаленных зубов. Нагрузка ложится на здоровые зубы, фиксирующие протез, в случае съемного моста — на десны. В результате атрофия продолжает развиваться. Часто она сводит на нет результаты протезирования — десна «проседает» вслед за костной тканью, под протезом появляется щель. Это не только неэстетично, но и опасно — в образовавшемся пространстве скапливаются остатки пищи, на которых активно размножаются микроорганизмы, провоцирующие воспаление.
Имплантация зубов, в отличие от других методик протезирования, позволяет сформировать нагрузку непосредственно на костную ткань в районе удаленного зуба. Таким образом, костная ткань продолжает работать в нормальном режиме, а значит, в ней сохраняются все необходимые обменные процессы. Это предупреждает истончение костной ткани челюсти.
Варианты восстановления зубного ряда при значительной атрофии
Но что же делать, если время упущено и степень атрофии костной ткани не позволяет имплантировать зубы? На сегодня есть две основные методики, позволяющие справиться с этой проблемой.
Восстановление костной ткани челюсти с последующей имплантацией с отложенной нагрузкой.
Это классическая методика, проверенная временем. Сначала проводится операция по увеличению объема костной ткани. Существуют разные методики: синус-лифтинг, расщепление альвеолярного отростка, подсадка костного трансплантата или искусственной ткани. Какая из них будет оптимальна в данном конкретном случае, может решить только лечащий врач. После операции потребуется от нескольких месяцев до полугода на восстановление костных структур, после чего в челюсть вживляются имплантаты, пока без коронок — и снова требуется около полугода для их приживления. Только после этого на титановое основание имплантатов устанавливаются коронки и челюсть, наконец, получает нагрузку.
Имплантация с немедленной нагрузкой
Это относительно новая методика стала возможной благодаря специальным имплантатам, которые фиксируются не в альвеолярной части челюсти, а глубже, в базальной ее части, которая состоит в основном из компактного вещества. Имплантаты подбирают исходя из индивидуальных особенностей челюсти пациента. Они требуют минимального времени для заживления — протез устанавливают уже на 3–5-й день после фиксации самого имплантата. Благодаря тому, что кость сразу же получает нагрузку, в ней сохраняется кровообращение, нормальный обмен веществ, что ускоряет регенерацию.
Для того чтобы орган сохранял свою структуру и функции, он должен работать. Это касается и костной ткани челюсти. Потеря зубов приводит к атрофии кости челюсти. Чтобы предупредить этот процесс, необходимо как можно быстрее после удаления зуба заменить его протезом. Имплантация зубов — самый приближенный к естественному способ их восстановления, позволяющий сохранить объем и плотность костной ткани.
Как выбрать стоматологическую клинику?
О том, на что обращать внимание, планируя имплантацию зубов, рассказывает Олег Владимирович Филимонов, врач-имплантолог центра дентальной имплантации SMILE-AT-ONCE:
«Как минимум поинтересуйтесь оборудованием, на котором работает клиника, материалы каких производителей она использует. Например, стоматология SMILE-AT-ONCE — официальный партнер известных производителей имплантатов: Nobel Biocare, Oneway Biomed, Straumann. На нашем сайте есть подробная информация об инструментах, оборудовании, программном обеспечении и технологиях, которые мы используем. Там же вы можете ознакомиться с нашими лицензиями, сертификатами и наградами.
Для успеха лечения важно, как долго клиника существует, каков опыт работы врачей, проходят ли они курсы повышения квалификации. Специалисты нашей клиники имеют более чем десятилетний стаж работы и регулярно участвуют в научно-практических конференциях, обучающих программах, других образовательных мероприятиях. Так, все имплантологи SMILE-AT-ONCE имеют действующие сертификаты Международного фонда имплантации (International Implant Foundation), что подтверждает их право работать в этой области. Клиника входит в международное сообщество имплантологов (International Team for Implantology. ITI), которое существует уже 30 лет. Мы осуществляем весь комплекс услуг по протезированию зубов с использованием имплантатов за семь дней и даем пожизненную гарантию на имплантаты, а также предлагаем удобную схему лечения как пациентам из Москвы, так и иногородним».
Лицензия № ЛО-77-01-013995 от 14 марта 2017г. выдана Департаментом здравоохранения города Москвы

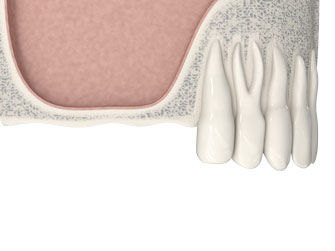
Предотвратить атрофию костной ткани можно, прибегнув к протезированию зубов с использованием имплантатов.
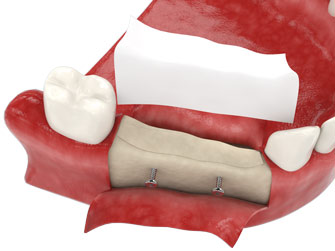
Протезирование зубов с использованием имплантатов часто рекомендуется, если значительно сократился объем костной ткани и если нельзя осуществить костную пластику.

Протезирование зубов с использованием имплантатов позволяет:
- остановить атрофию костной ткани;
- восстановить костную ткань;
- частично разгладить морщины вокруг рта за счет исправления формы челюсти.
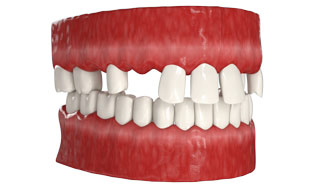
Протезирование зубов с использованием имплантатов возможно даже на последних стадиях развития пародонтита, а также при полной адентии и при значительном сокращении костной ткани.
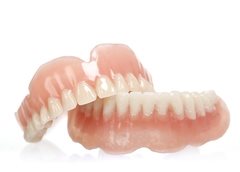
Ношение съемных протезов может вызывать дискомфорт и приводить к атрофии костной ткани и к проседанию десны.
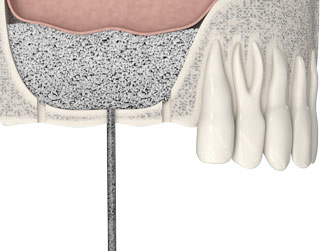
Протезирование зубов с использованием имплантатов не занимает много времени: обрести новую улыбку можно менее чем за одну неделю.
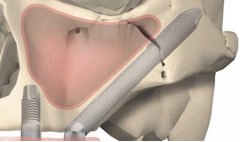
Протезирование зубов с использованием имплантатов может быть актуально для восстановления не только части жевательных зубов, но и всего зубного ряда верхней челюсти.
- 1 Биохимия соединительной ткани
- 2 Lars Schropp, A. Wenzel, L. Kostopoulos, et al. Bone Healing and Soft Tissue Contour Changes Following Single-Tooth Extraction:
A Clinical and Radiographic 12-Month Prospective Study. - 3 Соков, Л.П. Руководство по нейроортопедии. Л.П. Соков, Е.Л. Соков, С.Л. Соков. — М.: РУДН, 2002. — С. 74-75
- 4 Никольский В. Ю., Вельдяксова Л. В., Максютов А. Е. Оценка степени атрофии костной ткани челюстей после удаления зубов
в связи с дентальной имплантацией. Саратовский научно-медицинский журнал 2011. - 5 Клинические результаты использования различных костно- пластических материалов при синус-лифтинге /
С.Ю. Иванов, Э.А. Базикян, М.В. Ломакин [и др.] // Новое в стоматологии. — 1999. — № 5. — C. 75

Каадзе Анастасия Геннадьевна Ответственный редактор
Если вы решились на установку имплантатов или другой вид дентального протезирования, предварительно посетите пародонтолога. При выявлении патологий потребуется их устранение. Кроме того, необходима гигиеническая чистка зубодесневых карманов и зубов для устранения налета и зубного камня.
В настоящее время реставрации c опорой на дентальные имплантаты стали довольно распространенным методом лечения частичной и полной адентии. Более глубокие исследования способствовали разработке различных протоколов нагрузки и установки имплантатов, имплементации новых дизайнов протетических конструкций и общему пониманию биологически-механических механизмов остеоинтеграции. О все большей популярности метода дентальной имплантации говорят и данные продаж титановых внутрикостных опор. Gaviria и коллеги, анализируя данные Американской ассоциации оральных и челюстно-лицевых хирургов, сообщили, что количество установленных в год дентальных имплантатов достигает 100 000 - 300 000. По другим данным, полученным в Германии, за 2000 год было установлено около 200 000 имплантатов, и, согласно заявлениям научных сообществ, количество таковых в данное время возросло до 1,2 миллионов.
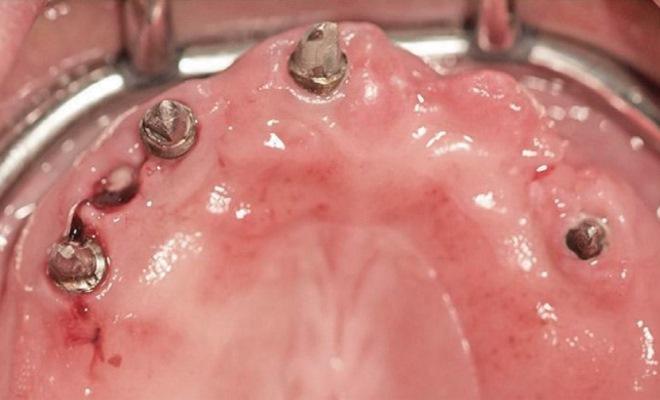
Периимплантит является одной из основных причин дезинтеграции имплантатов, представляя собой воспалительное поражение мягких и твердых тканей, которые окружают имплантат. 6-й Европейский семинар по пародонтологии определил, что основной причиной развития периимплантита является бактериальная бляшка, а другими ассоциированными факторами – плохая гигиена полости рта и наличие пародонтита в анамнезе. Несмотря на развитие хирургических подходов и специализированных технологий, установка имплантатов является той ятрогенной манипуляцией, которая обосновывает необходимость непрерывной учебы и совершенствования умений врачей-стоматологов для достижения еще лучших результатов реабилитации пациентов. Иными словами, установка имплантатов должна проводиться высококвалифицированным специалистами в своей отрасли. В данной статье описан подход хирургического и ортопедического лечения пародонтальных и периимплантитных ятрогенно-ассоциированных осложнений.
Клинический случай
55-летняя женщина, курильщик (4-6 сигарет/день), при отсутствии других соматических нарушений, обратилась за стоматологической помощью в нашу клинику в мае 2015 года с главной жалобой на сильную и острую боль в области обеих челюстей. Также женщина жаловалась на генерализованное спонтанное кровотечение и нагноение. Пациентка отказалась фотографироваться для регистрации исходной клинической ситуации в ходе первичного визита. Она также сообщила, что ее прежний стоматолог уже выполнил все необходимые подготовительные манипуляции.
Анамнез
В январе 2004 года у пациентки был диагностирован генерализованный тяжелый пародонтит с формированием глубоких карманов и симптомами выраженной подвижности зубов (фото 1 (а)). Пациентка не была проинформирована о наличии или необходимости лечения тяжелого пародонтита. В ходе прогрессирования заболевания в апреле 2004 года ей были удалены зубы № 21, № 29 и № 32, а в области зубов №18, № 20, № 30 и № 31/32 были установлены дентальные имплантаты (фото 1 (b)). Дефект костной ткани в области № 21 не был аугментирован, и дальнейшего лечения пародонтита не проводилось. В июле 2004 года имплантаты были нагружены частичными несъемными протезами (FPD) с опорой на № 22 и № 27 зубах (фото 2 (а)). Аугментации костного дефекта в области зуба № 21 не проводилось, в области имплантата, установленного на месте № 20, наблюдалась прогрессирующая потеря костной ткани, которая также никак не корректировалась. Сопутствующего лечения пародонтита также не проводилось.
Фото 1: Ортопантомограмма пациентки. (a) До начала лечения (январь 2004 г.). (b) После экстракции зубов на нижней челюсти и установки имплантатов (апрель 2004 г.).
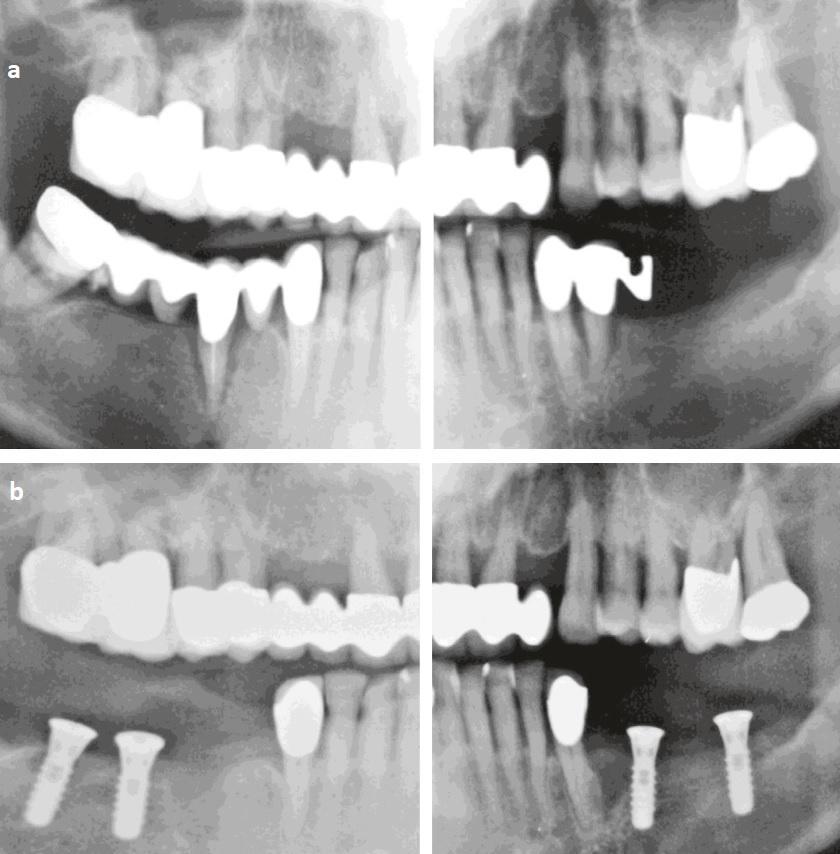
Фото 2: Ортопантомограмма пациентки. (a) После нагрузки имплантатов на нижней челюсти (июль 2004 г.). (b) После экстракции зуба № 15 (январь 2006 г.).
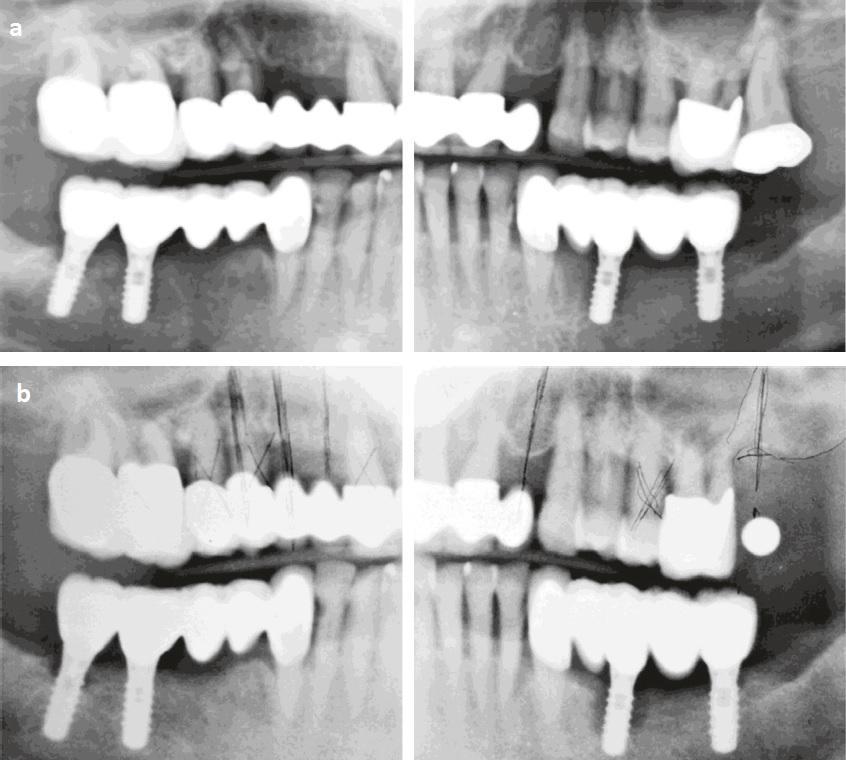
В январе 2006 года у пациентки было отмечено частичное заживление лунки удаленного зуба № 21, наличие костного дефекта с периапикальным поражением (зуб № 23) и двух периимплантатных дефектов (№ 20 и № 31;> 50% и
В настоящее время реставрации c опорой на дентальные имплантаты стали довольно распространенным методом лечения частичной и полной адентии. Более глубокие исследования способствовали разработке различных протоколов нагрузки и установки имплантатов, имплементации новых дизайнов протетических конструкций и общему пониманию биологически-механических механизмов остеоинтеграции. О все большей популярности метода дентальной имплантации говорят и данные продаж титановых внутрикостных опор. Gaviria и коллеги, анализируя данные Американской ассоциации оральных и челюстно-лицевых хирургов, сообщили, что количество установленных в год дентальных имплантатов достигает 100 000 - 300 000. По другим данным, полученным в Германии, за 2000 год было установлено около 200 000 имплантатов, и, согласно заявлениям научных сообществ, количество таковых в данное время возросло до 1,2 миллионов.

Периимплантит является одной из основных причин дезинтеграции имплантатов, представляя собой воспалительное поражение мягких и твердых тканей, которые окружают имплантат. 6-й Европейский семинар по пародонтологии определил, что основной причиной развития периимплантита является бактериальная бляшка, а другими ассоциированными факторами – плохая гигиена полости рта и наличие пародонтита в анамнезе. Несмотря на развитие хирургических подходов и специализированных технологий, установка имплантатов является той ятрогенной манипуляцией, которая обосновывает необходимость непрерывной учебы и совершенствования умений врачей-стоматологов для достижения еще лучших результатов реабилитации пациентов. Иными словами, установка имплантатов должна проводиться высококвалифицированным специалистами в своей отрасли. В данной статье описан подход хирургического и ортопедического лечения пародонтальных и периимплантитных ятрогенно-ассоциированных осложнений.
Клинический случай
55-летняя женщина, курильщик (4-6 сигарет/день), при отсутствии других соматических нарушений, обратилась за стоматологической помощью в нашу клинику в мае 2015 года с главной жалобой на сильную и острую боль в области обеих челюстей. Также женщина жаловалась на генерализованное спонтанное кровотечение и нагноение. Пациентка отказалась фотографироваться для регистрации исходной клинической ситуации в ходе первичного визита. Она также сообщила, что ее прежний стоматолог уже выполнил все необходимые подготовительные манипуляции.
Анамнез
В январе 2004 года у пациентки был диагностирован генерализованный тяжелый пародонтит с формированием глубоких карманов и симптомами выраженной подвижности зубов (фото 1 (а)). Пациентка не была проинформирована о наличии или необходимости лечения тяжелого пародонтита. В ходе прогрессирования заболевания в апреле 2004 года ей были удалены зубы № 21, № 29 и № 32, а в области зубов №18, № 20, № 30 и № 31/32 были установлены дентальные имплантаты (фото 1 (b)). Дефект костной ткани в области № 21 не был аугментирован, и дальнейшего лечения пародонтита не проводилось. В июле 2004 года имплантаты были нагружены частичными несъемными протезами (FPD) с опорой на № 22 и № 27 зубах (фото 2 (а)). Аугментации костного дефекта в области зуба № 21 не проводилось, в области имплантата, установленного на месте № 20, наблюдалась прогрессирующая потеря костной ткани, которая также никак не корректировалась. Сопутствующего лечения пародонтита также не проводилось.
Фото 1: Ортопантомограмма пациентки. (a) До начала лечения (январь 2004 г.). (b) После экстракции зубов на нижней челюсти и установки имплантатов (апрель 2004 г.).

Фото 2: Ортопантомограмма пациентки. (a) После нагрузки имплантатов на нижней челюсти (июль 2004 г.). (b) После экстракции зуба № 15 (январь 2006 г.).

В январе 2006 года у пациентки было отмечено частичное заживление лунки удаленного зуба № 21, наличие костного дефекта с периапикальным поражением (зуб № 23) и двух периимплантатных дефектов (№ 20 и № 31;> 50% и
З. Р. Галеева
соискатель кафедры терапевтической стоматологии ГБОУВПО «Казанский государственный медицинский университет» Минздравсоцразвития РФ
Л. Р. Мухамеджанова
д. м. н., доцент, научный консультант учебно-методического центра «Эксклюзив Дент» (Казань)
Оценка степени тяжести воспалительно-деструктивных поражений костной ткани периапикальной области, зоны фуркации и межзубных/межкорневых перегородок имеет ключевое значение при планировании этапов диагностики, лечения и реабилитации пациентов врачами-стоматологами любого профиля. Особенно много споров поставленная проблема вызывает при выборе ортопедических/ортодонтических конструкций, ограничении дизруптивной нагрузки, консервативной/хирургической тактике ведения пациентов, отягощенных эндопародонтальными очагами инфекции (ЭПО).
Эндопародонтальный очаг одонтогенной инфекции представляет собой сочетание воспалительно-деструктивных процессов в верхушечном периодонте и маргинальном пародонте. Учитывая агрессивность таких очагов хронической инфекции, уместно упомянуть о так называемом эндопародонтальном синдроме, при котором имеют место системные проявления микробной сенсибилизации организма: септический эндокардит, ревматизм, хронический пиелонефрит.
Вопросы этиопатогенеза ЭПО обсуждаются отечественными и зарубежными исследователями в течение нескольких десятилетий, однако вопрос первичности/вторичности вовлечения в воспалительный процесс тканей эндодонта/пародонта остается нерешенным.
На сегодняшний день постулировано, что пенетрация инфекционных агентов — микробов и их токсинов в системе эндодонт/пародонт происходит по сосудистой системе (васкулярным путем) и по основным корневым каналам, их ответвлениям, а также дентинным канальцам (тубулярным путем).
Сочетанные заболевания пульпы и пародонта являются причиной потери зубов более чем в 50 % случаев. Диагностика затрудняется тем, что эти заболевания ранее изучались как самостоятельные, а схожесть клинических симптомов зачастую выпадала из поля зрения специалистов при дифференцировании, что является одним из факторов неуспешного лечения пациентов с такой патологией.
Целью настоящего исследования явилась разработка алгоритма оценки степени тяжести поражений костной ткани у пациентов с эндопародонтальными очагами инфекции.
Нами было обследовано 98 пациентов с ЭПО (40 мужчин и 58 женщин в возрасте 22—72 лет), обратившихся в лечебно-хирургическое отделение стоматологической поликлиники Казанского медицинского университета с целью санации полости рта и последующего протезирования. Полный комплекс дифференциально-диагностических мероприятий включал в себя: анализ анамнестических данных, клинический осмотр пациента, рентгенологическое исследование (прицельная дентальная рентгенограмма, ортопантомограмма).
При сборе анамнеза выясняли жалобы, связанные с возникшими в полости рта изменениями (отек), время их появления, динамику развития, возможные причины и частоту обострений.
При осмотре полости рта обращали внимание на сохранность/нарушение целостности зубодесневого прикрепления, глубину кармана, характер над- и поддесневых зубных отложений, наличие/отсутствие грануляций в пародонтальном кармане и их характер (вялые, цианотичные/сочные, пролабирующие, кровоточащие), подвижность зуба, наличие свищей (периапикального или пародонтального генеза), выраженность/сглаженность феномена стиплинга, наличие/отсутствие экссудата (гнойный, серозный, геморрагический или их сочетания).
При анализе данных лучевого метода исследования оценивали степень тяжести деструктивного процесса в пародонте: при пародонтите легкой степени отмечалась начальная степень деструкции костной ткани межзубных перегородок (значительное разволокнение или исчезновение замыкательных пластинок, явления интракортикального, субкортикального и трабекулярного остеопороза, снижение высоты межзубных перегородок — менее 1/3 длины корня), для пародонтита средней степени характерна резорбция костной ткани межзубных перегородок от 1/3 до ½ длины корня, для тяжелого пародонтита — резорбция костной ткани на величину более 1/2 высоты межзубных перегородок (до полного рассасывания альвеолярной перегородки).
При анализе прицельных дентальных рентгенограмм оценивали степень деструктивного процесса в периапикальной области: размеры очага (продольный и поперечный), контуры (четкие/нечеткие), тенденцию к слиянию пародонтального и периапикального очагов деструкции.
В ходе проведенных исследований нами были выделены наиболее часто встречающиеся типы эндопародонтальных поражений (иллюстрация прицельными дентальными снимками или фрагментами ортопантомограмм) (рис. 1) .
Рис. 1. Сочетание хронического гранулирующего/гранулематозного периодонтита с двусторонней вертикальной деструкцией костной ткани.
Тип эндопародонтального очага, для которого характерны расширение периодонтальной щели на всем протяжении, вертикальная деструкция костной ткани альвеолы. Кортикальная пластинка частично сохранена, с явлениями субкортикального остеопороза; по периферии очага наблюдается истончение трабекул, расширение межтрабекулярных промежутков. Функциональная ориентация трабекул (вертикальная) частично сохранена. Высота альвеолярного гребня снижается.
Как правило, пародонтальные карманы узкие и глубокие (до 6—8 мм), выполнены сочными (часто пролабирующими) грануляциями. Подвижность 1—2-й степени. Изменение оси наклона зуба. Полагаем, что изменение направления дизруптивной нагрузки имеет существенное значение в формировании данного типа очага деструкции (рис. 2) .
Рис. 2. Сочетание хронического гранулематозного периодонтита (кистогранулемы) с вертикальным и горизонтальным типом деструкции кости межзубных/межкорневых перегородок.
Для данного типа эндопародонтального поражения характерно наличие очага деструкции кости в периапикальной области с четкими ровными контурами, округлой или овальной формы. Целостность кортикальной пластинки нарушена. Костные трабекулы по периферии очага сохраняют функциональную ориентацию (горизонтальную), отмечаются признаки снижения минеральной плотности кости. Высота альвеолярного отростка снижается за счет резорбции (по смешанному типу) трабекулярной кости альвеолы.
Наиболее часто встречается у многокорневых зубов. Фуркационные дефекты кости (не связанные с осложнениями эндодонтического вмешательства) расцениваются как прогностически неблагоприятные факторы. Как правило, изменения положения зуба в зубном ряду не изменяется. Пародонтальные карманы глубиной не более 5 мм, выполнены вялыми цианотичными грануляциями. В 25 % случаев выявляются свищи пародонтального и периапикального генеза (дифференциальная диагностика последних затруднена) (рис. 3) .
Рис. 3. Сочетание хронического гранулематозного периодонтита (кистогранулемы) с горизонтальным типом деструкции кости межзубных/межкорневых перегородок.
Характеризуется наличием очага деструкции кости с четкими ровными контурами; нередко по периферии очага наблюдаются явления усиления минеральной плотности кости. Классический горизонтальный тип деструкции кости формирует «широкие» пародонтальные карманы, глубина которых зависит от степени убыли кости. Карманы часто выполнены вялыми грануляциями.
На более поздних стадиях заболевания может измениться ось наклона зуба и усилиться подвижность. Усиление дизруптивной нагрузки может спровоцировать обострение заболевания. При преобладании внекостного рычага над внутрикостным прогноз неблагоприятный (рис. 4) .
Рис. 4. Сочетание хронического гранулирующего периодонтита с вертикальным типом деструкции кости межзубных/межкорневых перегородок.
Этот тип эндопародонтального очага характеризуется наличием деструктивных изменений кости с нечеткими неровными контурами; по периферии очага наблюдаются выраженные явления снижения минеральной плотности костной ткани. Часто при таком сочетании формируются фуркационные дефекты.
На более поздних стадиях заболевания очаг деструкции костной ткани в области септы, распространяющийся вдоль периодонтальной щели, сливается с очагом деструкции в периапикальной области, возможна резорбция цемента корня зуба, в более тяжелых случаях — дентина, чем обусловлена неровность контуров корня зуба. Изменяется ось наклона зуба, возможно усиление подвижности зуба даже на ранних стадиях заболевания. Пародонтальные карманы глубокие, достигающие верхушки корня зуба, выполнены обильными грануляциями. Усиление дизруптивной нагрузки ухудшает прогноз течения заболевания.
Сочетание хронического гранулирующего периодонтита со смешанным типом деструкции. Характеризуется наличием очага деструкции кости в периапикальной области с нечеткими неровными контурами; трабекулы по периферии очага истончены, функциональная ориентация их нарушена. Резорбция кости альвеолярного гребня по смешанному типу, однако в большинстве наблюдаемых случаев преобладает вертикальное направление. Прослеживается тенденция к слиянию пародонтального и периапикального очагов. Возможна резорбция цемента корня зуба. Пародонтальные карманы глубокие, часто широкие. Высота альвеолярного отростка снижается, подвижность зуба и изменение оси наклона возникают на ранних стадиях заболевания.
Для сочетания хронического гранулирующего периодонтита с горизонтальным типом деструкции кости межзубных/межкорневых перегородок характерно наличие очага резорбции в периапикальной области с неровными нечеткими контурами. По периферии костные трабекулы несколько истончены, функциональная ориентация не нарушена.
Контуры корня могут быть изменены за счет гиперцементоза (редко). Деструкция альвеолярного гребня по горизонтальному типу, периодонтальная щель расширена на всем протяжении (влияние функциональной перегрузки). Пародонтальные карманы широкие, на более поздних стадиях возможно слияние пародонтального и периапикального очагов деструкции. Высота альвеолярного отростка снижается, изменение положения оси зуба и усиление подвижности возможны на продвинутых стадиях заболевания (рис. 5) .
Рис. 5а. Сливной очаг пародонтальной и периапикальной деструкции костной ткани.
Рис. 5б. Сливной очаг пародонтальной и периапикальной деструкции костной ткани.
Рис. 5в. Сливной очаг пародонтальной и периапикальной деструкции костной ткани.
Рис. 5г. Сливной очаг пародонтальной и периапикальной деструкции костной ткани.]
Рис. 5д. Сливной очаг пародонтальной и периапикальной деструкции костной ткани.
Наиболее тяжелый и часто встречающийся вариант эндопародонтальных поражений представляет собой сливной очаг пародонтальной и периапикальной деструкции. В большинстве случаев возникает в условиях длительно действующей повышенной дизруптивной нагрузки (очаг травматической окклюзии). Характеризуется наличием значительного по объему очага деструкции, захватывающего костную ткань периапикальной области и костную ткань межзубных перегородок; последние часто полностью резорбируются. Неровность контуров корня обусловлена рассасыванием цемента (дентина). Пародонтальные карманы глубокие, достигающие апикальной части корня, подвижность зуба во всех направлениях.
Таким образом, маркерной рентгенологической особенностью эндопародонтального очага хронической инфекции является очаг деструкции костной ткани в перирадикулярной области однокорневых и многокорневых зубов в сочетании с вертикальным типом деструкции губчатой кости межкорневых перегородок.
Также возможно сочетание деструкции костной ткани в перирадикулярной области однокорневых и многокорневых зубов с горизонтальным типом деструкции губчатой кости межкорневых перегородок.
Слияние двух очагов инфекции в прогностическом плане является крайне неблагоприятным и определяет показания к удалению зуба.
Балин В. Н. Практическая периодонтология / В. Н. Балин, А. К. Иорданашвили, А. М. Ковалевский. — СПб.: Питер Пресс, 1995. — 272 с.
Барер Г. М. Терапевтическая стоматология / Г. М. Барер: учебник в 3 ч. — М.: Гэотар-Медиа, 2008. — Ч. 2. — Болезни пародонта. — 224 с.
Безрукова И. В., Грудянов А. И. Агрессивные формы пародонтита/ И. В. Безрукова, А. И. Грудянов. Руководство для врачей. — М.: МИА, 2002. — С. 126.
Бризено Б. Пародонтально-эндодонтические поражения / Б. Бризено. Клиническая стоматология. — 2001, № 2. — С. 24—29.
Боровский Е. В. Терапевтическая стоматология / Е. В. Боровский: учебник для студентов медицинских вузов. — М.: Медицинское информационное агентство, 2007. — 840 с.
Герберт Ф. Вольф. Пародонтология / Ф. Вольф Герберт, Эдит М. Ратецхак, Клаус Ратейцхак. Пер с нем. Под ред. проф. Г. М. Барера. — М.: Медпресс-информ, 2008. — 548 с.
Диеков Д. Регенеративное лечение пародонтитов и эндопародонтальной патологии с использованием купрала и купрал-депофореза / Д. Диеков. Маэстро стоматологии. — 2004, № 3. — С. 21—27.
Джеймс Л. Гутман. Решение проблем в эндодонтии: профилактика, диагностика и лечение / Л. Гутман Джеймс, С. Думша Том, Э. Ловдэл Пол. Пер. с англ. — М.: Медпресс-информ, 2008. — 592 с.
Коэн С. Эндодонтия. 8-е издание, переработанное и дополненное / С. Коэн, Р. Бернс. Русское издание под ред. д. м. н., профессора А. М. Соловьевой. Издательский дом STBOOK, 2007. — 1026 с.
Маланьин И. В. Закономерность влияния заболеваний пародонта на пульпу и апикальный периодонт / И. В. Маланьин. Кубанский научный медицинский вестник // 2004, № 5—6. — С. 71—72.
Течение болезни сопровождается повышением температуры, общей интоксикацией, множественными гнойными выделениями и другими симптомами.
Любая из форм остеомиелита требует немедленного лечения, включающего в себя, как медикаментозное, так и хирургическое вмешательство.
Причины возникновения остеомиелита челюсти
Стоматологи выделяют несколько классификаций причин, по которым у пациентов развивается та или иная форма остеомиелита челюсти. Все они группируются в первичные, травматические и патогенные факторы.
К первой группе относятся запущенные случаи и осложнения таких заболеваний, как:
- острый отит;
- ангина;
- конъюнктивит;
- лицевые фурункулы и карбункулы;
- периодонтит;
- зубная гранулема;
- хронический пульпит;
- киста зуба.
Второй блок причин – инфицирование, полученное из-за:
- перелома челюсти;
- ушибов носа и разрыва перегородки;
- огнестрельных ранений;
- неправильно удаленного зуба;
- занеснной инфекции при переливании крови или уколе.
Патогенными источниками развития остеомиелита служат десятки видов болезнетворных бактерий, попавших в кровь, на слизистую оболочку, проникших в небольшую ранку или в открытую кариозную полость, это:
- золотистый стафилококк;
- кишечная палочка;
- клебсиелла;
- стрептококк группы B;
- протей;
- фузобактерии;
- синегнойная палочка.
Также остеомиелит челюсти часто развивается на фоне общего снижения иммунитета как сопутствующее осложнение таких недугов, как:
- сахарный диабет;
- ревматизм;
- полиартрит;
- цирроз печени.
Симптомы и диагностика остеомиелита челюсти
Основные симптомы остеомиелита челюсти проявляются уже на ранних стадиях, позволяя своевременно диагностировать конкретный тип заболевания и назначить необходимое лечение. У большинства пациентов наблюдается резкое повышение температуры, слабость, бессонница, и постепенная нарастающая боль в области пораженного участка кости, сопровождающаяся отеком.
Как только остеомиелит переходит в острую фазу, симптоматика ухудшается в зависимости от вида инфекции, помимо сильной боли и зловонного запаха фиксируется:
- появление свищей с обильным выделением гноя;
- онемение нижней челюсти и затрудненное движение при открывании рта;
- увеличение лимфоузлов;
- высокая подвижность одного или нескольких зубов;
- боль при глотании;
- затрудненное носовое дыхание;
- гнойное воспаление глазниц.
Стоматолог на этом этапе смотрит на состояние челюстной кости, выявляет очаги воспаления и определяет необходимость оперативного вмешательства. Важным моментом будет исключить развитие туберкулезных проявлений, злокачественных образований, нагноений на альвеолах здоровых зубов, а также определить риски появления других очагов заболевания. Только после окончательного диагноза назначается комплексное лечение.
Разновидности остеомиелита челюсти
(в данном разделе разместить несколько фото пациентов с остеомиелитом)
Классификация остеомиелита челюсти делится по способу проникновения инфекции, локализации и типам возбудителя. Каждая из разновидностей имеет свою специфику лечения, диагностики и прогнозирования осложнений. Неправильно поставленный диагноз приводит к затяжным последствиям, которые провоцируют развитие других серьезных недугов.
Наиболее часто встречается одонтогенный остеомиелит, причинами которого стали недолеченные воспалительные заболевания, запущенный кариес и даже стоматит. Инфицирование происходит через кариозную полость, афтозную язву или открытую пульпу, распространяясь на мягкие ткани и далее – в челюстную кость. Из-за специфики в 70% случаев это остеомиелит нижней челюсти, так как на нее приходится основная жевательная нагрузка.
Травматический остеомиелит верхней челюсти, как и нижней, является последствием внешнего воздействия. Особую опасность представляют закрытые переломы и трещины, образовавшиеся в результате неправильного срастания костной ткани. Попадание возбудителя инфекции не всегда фиксируется в полости рта – в ряде случаев бактерии проникают через поврежденную скулу.
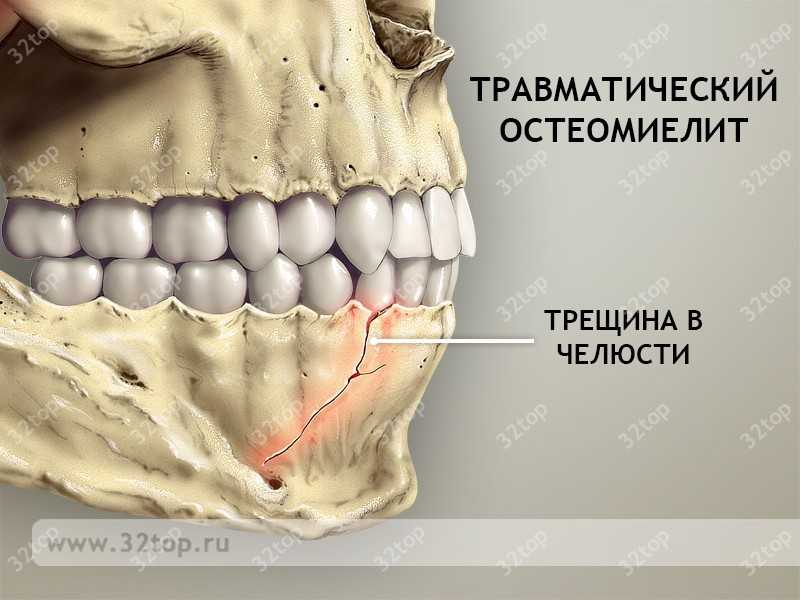
Частным случаем травматического типа является лучевой остеомиелит, представляющий собой поражение здоровой костной ткани злокачественной опухолью. Причиной заражения становится лучевая терапия, из-за которой раковые клетки нередко попадают в патогенную среду гнойного воспаления. На фоне ослабленного радиацией иммунитета развивается воспаление, причем темпы прогрессирования будут заметно выше, чем у других видов.
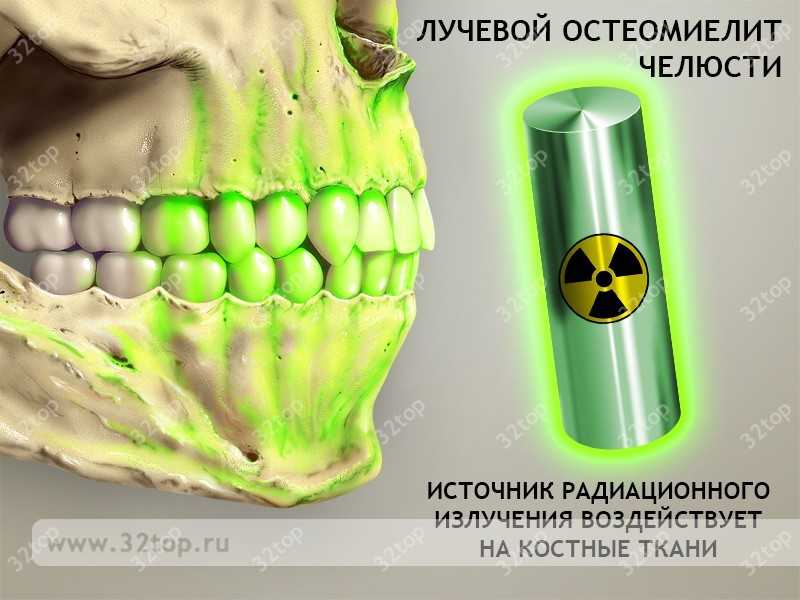
Отдельно выделяется остеомиелит после удаления зуба. Не до конца удаленная пульпа не является ошибкой стоматолога, по ряду показаний нервные окончания сохраняются, но могут беспокоить пациента в течение нескольких дней. Если боль не утихает дольше недели, то существуют риски возникновения симптомов остеомиелита, что требует повторного приема.
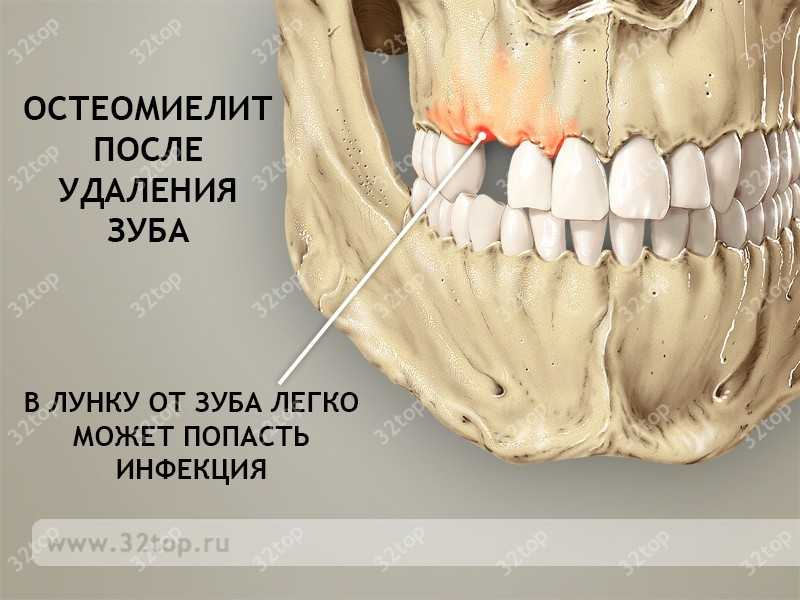
Гематогенный остеомиелит проявляется на фоне общего заражения крови. Спровоцировать его может любой порез, царапина и любая другая ранка в области кровотока. Отличается тип обратным патогенезом – страдает сразу челюстная ткань, а зубы при этом сохраняют все признаки здорового облика. Такая хронология опасна тем, что многие игнорируют первичные симптомы и обращаются за помощью врача, когда зуб уже невозможно сохранить. Не откладывайте лечение на потом и не запускайте болезнь. Вы можете выбрать наиболее подходящую вам клинику с хорошими отзывами и доступными ценами
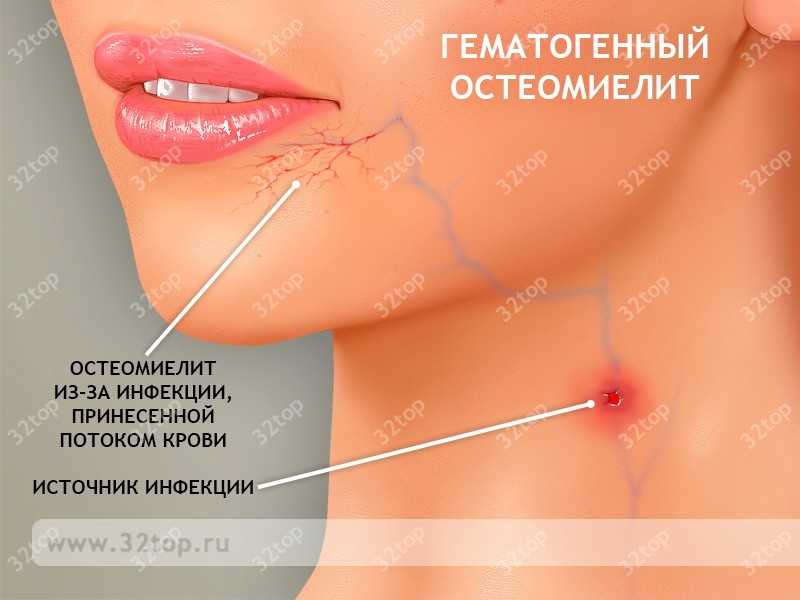
Хронический остеомиелит челюсти
Переход остеомиелита в хроническую фазу трудно контролируется даже в клинических условиях. Внешние признаки выздоровления часто говорят о временной ремиссии, которая длится от нескольких месяцев до нескольких лет, после чего острая фаза возвращается с усилением симптомов и более серьезными формами заболевания, имеющими свою классификацию:
- Мультифокальная рецидивирующая форма – частотный случай остеомиелита челюсти у детей. Гнойные выделения отсутствуют, но при этом образуются множественные очаги воспаления. Точная природа до сих пор не изучена, как и периодичность обострения.
- Остеомиелит Гарре (склерозирующая форма) – вялотекущие воспаления с незначительными нагноениями в костных полостях. Боль может не ощущаться, но специфический запах изо рта сохраняется постоянно. Вид диагностируется рентгеном по уплотнениям челюстной ткани.
- Абсцесс Броди – затяжной случай остеомиелита с образованием обширных полостей, заполненных жидким гноем. Болезненность минимальная, что позволяет обойтись без хирургического вмешательства.
- Остеомиелит Оллье – самая редкая разновидность, возбудителем которой являются стафилококки, образующие в тканях челюсти белковые выделения серозной жидкости. Выявление требует точной томографии, клинические симптомы отсутствуют.
- Дезморфиновый остеомиелит – диагностируется у наркозависимых пациентов. Вызывается нарушением кровоснабжения костных тканей и множественными гнойными поражениями, приводящими к деформации овала лица.
Лечение остеомиелита челюсти
В зависимости от стадии и формы заболевания, лечение остеомиелита челюсти начинается по-разному. Первейшим пунктом является удаление очага гнойного воспаления – пораженного зуба, либо дезинфекция и санация костного участка. На этом этапе важно полностью удалить весь гной, при необходимости – провести дренаж с одновременными пробами выделений на точное определение возбудителя. В крайнем случае, проводится шинирование подвижных зубов.
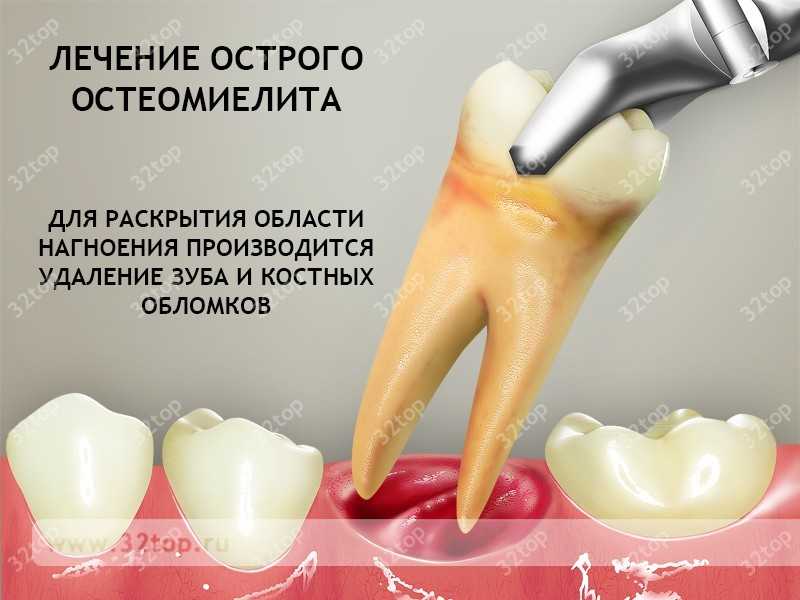
Ход лечения
После купирования острой фазы начинается общая терапия, которая может включать в себя лечение антибиотиками, противовирусными препаратами, назначение капельниц и шунтирования для оттока гнойной жидкости. Сюда же входит физиотерапия – УВЧ, ультразвук, плазмоферез и оксигенация. Цель – не только избавиться от симптомов, но и улучшить состояние организма для дальнейших процедур.
Как только пациенту становится лучше, встает вопрос секвестров – участков омертвевшей костной ткани, не способных к восстановлению. При незначительном поражении они разрушаются и выводятся наружу вместе с гноем. Если некроз обширный, их необходимо удалять хирургическим путем, иначе остеомиелит челюсти перейдет в хроническую форму и будет периодически возвращаться в острой фазе со всеми осложнениями.
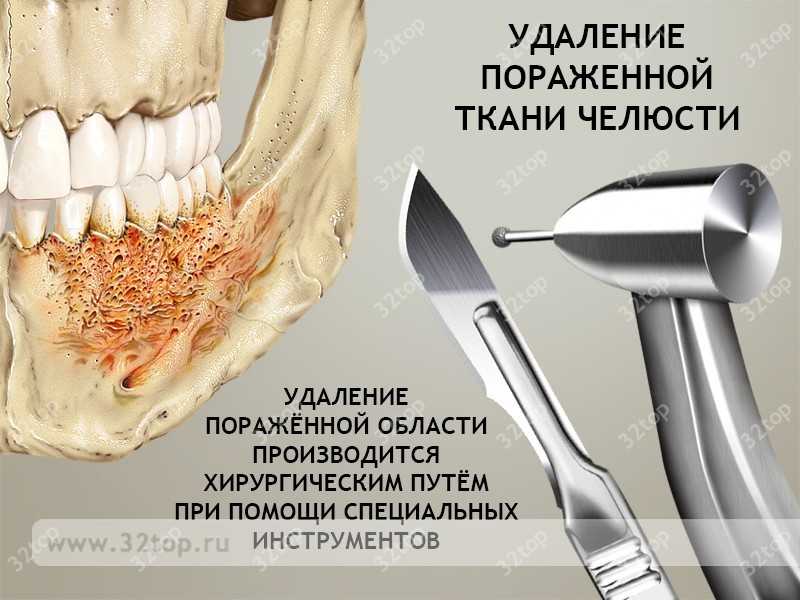
Любая форма заболевания требует стационарного лечения под постоянным наблюдением стоматолога, хирурга и терапевта. Консервативные методы, включая курс антибиотиков, длятся не более 25-30 дней, после чего пациента выписывают. Если же операция неизбежна, то госпитализация затягивается до 3-4 месяцев, пока челюстная кость не восстановится.
Лечение хронического остеомиелита
Курс сочетает в себе медикаменты и регулярную физиотерапию. Оперативное вмешательство зависит от глубины поражения челюстной ткани. Если секвестры находятся слишком глубоко, то стоматолог рекомендует периодические консультативные приемы, чтобы не травмировать кость еще сильнее и ликвидировать рецидивы остеомиелита на ранних стадиях.
Если же расположение омертвевших участков позволяет их удалить, то после окончательного выведения инфекции назначается повторная операция. Секвестр удаляют методом выскабливания, а образовавшуюся полость восстанавливают остеоиндуктивным материалом, по аналогии с протезированием и наращиванием челюстной кости.
Возможные последствия и профилактика
Прогноз остеомиелита челюсти напрямую зависит от оперативности поставленного диагноза и принятых мер по устранению болезни. При острой стадии и должном уровне оказанной помощи выздоровление наступает в минимальные сроки, но при этом существует риск возникновения серьезных осложнений в виде:
- приступов легочной недостаточности;
- симптомов менингита;
- сепсиса и септического шока;
- флебита лицевых вен.
Профилактические рекомендации стоматолога содержат следующие советы:
- Избегайте риска травм челюсти – малейшая трещина после ушиба может стать причиной развития тяжелейшей инфекции.
- Своевременно лечите кариес, пульпит и пародонтит – поражение дентина способствует распространению воспаления, как на мягкие ткани, так и на кость.
- Избегайте самолечения и народной медицины – гнойные выделения являются симптомами серьезных процессов в организме и требуют незамедлительного обращения к врачу.
- Не запускайте ОРЗ и ОРВИ заболевания – скопления гноя в носоглотке и гайморовых пазухах приводит к инфекциям всего челюстного аппарата.
- Посещайте стоматолога не реже двух раз в год.
Автор: д.м.н. А.М. Соловьева, Санкт-Петербургский Гос. Мед. Университет
Незавершенное формирование корней зубов требует особого подхода к тактике эндодонтического лечения. Это связано, в первую очередь, с морфологическим строением эндодонта:
- строение корня характеризуется сокращенной длиной, малой толщиной стенок, наличием выраженного слоя слабо минерализованного предентина;
- корневые каналы имеют широкий просвет, расширяющийся от устья к верхушке и оканчивающийся резким воронкообразным расширением в апикальной трети;
- отсутствует анатомическое апикальное сужение в области дентинно-цементной границы, что приводит к широкому сообщению канала с периодонтальным пространством.
Указанные особенности морфологического строения системы эндодонта затрудняют выполнение основных задач эндодонтического лечения, таких как полноценная очистка просвета и стенок корневого канала, придание просвету канала оптимальной конусообразной формы и герметичная конденсация пломбировочного материала с трехмерной обтурацией. В ходе лечения сохраняется повышенный риск выведения за пределы канала ирригационных растворов и пломбировочных материалов, обладающих раздражающими или токсическими свойствами.
Лечение затруднено и в связи с патоморфологическими особенностями развития воспаления периодонта у детей:
- склонность к хроническому пролиферативному характеру воспаления;
- врастание грануляций из периапикального очага в корневой канал, что затрудняет его очистку, остановку кровотечения и высушивание для постоянного пломбирования;
- большой объем поражения костной ткани из-за слабой минерализации и крупнопетлистой структуры;
- высокая частота развития наружной и внутренней резорбции тканей корня.
Перечисленные выше особенности определяют тактику консервативного эндодонтического лечения хронического периодонтита постоянных зубов у детей. Дополнительной задачей лечения постоянных зубов с незавершенным формированием корней является создание условий для завершения роста корня в длину или образования апикального барьера между эндодонтом и периодонтом, то есть замыкания просвета апикального отверстия и формирования апикального упора.
Завершение роста корня в длину возможно при сохранении жизнеспособности всей или части корневой пульпы и так называемой «ростковой зоны» корня. Для решения этой задачи применяются витальные методы эндодонтического лечения:
- биологический метод;
- витальная ампутация;
- глубокая витальная ампутация.
Однако при необратимых деструктивных изменениях в пульпе и гибели клеток Гертвиговского влагалища нормальное завершение процесса формирования корня невозможно. В подобных ситуациях необходимо использование методов лечения, направленных на образование барьера, разделяющего просвет канала и периодонт. Традиционным подходом является метод апексификации.
Апексификация – многофазное консервативное эндодонтическое лечение, создающее условия для естественного формирования минерализованного твердотканного «мостика» в области верхушки корня зуба. Метод основан на многократном повторном пломбировании корневых каналов временными пастами с высоким содержанием гидроксида кальция, Ca(OH)2.
Гидроксид кальция – сильное основание, благодаря присущей ему щелочной реакции обладает рядом лечебных свойств. Данное вещество характеризуется высокой антимикробной активностью в отношении подавляющего большинства микроорганизмов, выделенных из инфицированных корневых каналов (Соловьева А.М., 2000; Georgopoulou M. et al, 1993). Препарат проявляет выраженную способность к растворению некротизированных тканей. Это особенно ценно при лечении зубов с незавершенным формированием корней, поскольку их качественная инструментальная очистка затруднена (Hasselgren G. et al, 1988).
Клиницистам хорошо известны пластикостимулирующие свойства гидроксида кальция. В ходе экспериментальных исследований было показано, что при прямом контакте с жизнеспособной пульпой гидроксид кальция стимулирует образование «дентинного мостика» (Schr?der U., 1985). При контакте с периодонтом или грануляционной тканью гидроксид кальция индуцирует формирование остеоцементного апикального барьера в области апикального отверстия (Соловьева А.М., 1999; Andreasen J.O., Andreasen F.N., 1993). Минерализованный апикальный барьер представлен цементом, костной тканью и грубоволокнистой соединительной тканью с аморфным отложением минеральных солей (Cvek M. et al, 1974).
Основными требованиями к лечебной пасте на основе гидроксида кальция для временного пломбирования корневых каналов являются:
- высокощелочное значение рН;
- легкость введения в корневой канал;
- густая консистенция, обеспечивающая плотное заполнение просвета канала;
- легкость извлечения из канала.
Замена временной лечебной пасты в корневом канале первый раз должна быть проведена не позже чем через 1 месяц, а в дальнейшем – каждые 3 месяца. Для формирования стабильного твердотканного барьера требуется от 6 до 18 мес. После клинико-рентгенологического подтверждения образования апикального минерализованного барьера корневой канал пломбируют постоянным заполнителем (гуттаперчей).
По нашим данным, формирование сплошного апикального минерализованного барьера происходит более чем в 90% случаев применения методики. Однако следует учитывать, что наличие рентгенологически видимой тени не всегда сопровождается полным восстановлением костной ткани. Это определяет важность диспансерного наблюдения данной группы пациентов в отдаленные сроки после завершения лечения.
Клинический пример
Апексификация в области 31 зуба с явлениями хронического гранулематозного периодонтита и признаками наружной резорбции корня у пациента 8 лет
Жалоб пациент не предъявлял.
В анамнезе: травма зуба за 3 месяца до настоящего обращения.
При объективном обследовании: вертикальная трещина в области коронки 31, подвижность зуба I степени, инъекция сосудов слизистой альвеолярного отростка в проекции верхушки корня.
На рентгенограмме: верхушка корня не сформирована, признаки наружной резорбции корня в области верхушки и в коронковой трети. Очаг деструкции костной ткани в периапикальной области (Рис. 1).
Лечение: хемо-механическая обработка корневого канала, апексификация с помощью пасты Calasept на основе гидроксида кальция (Nordiska Dental, Angelholm, Sweden). Общая продолжительность апексификации – 8 мес. Постоянное пломбирование методом латеральной конденсации гуттаперчи (Рис. 2-5).
Результаты проведения апексификации: облитерация апикальной части канала, ликвидация очага деструкции кости, восстановление нормальной ширины периодонтальной щели, прекращение (арест) наружной резорбции корня в коронковой трети.
Читайте также:

